Clear Sky Science · es
Desplazamientos temporales del microambiente inmunitario en la endometriosis: de la evasión inmune al agotamiento inmunológico
Por qué importan las defensas del organismo en la endometriosis
La endometriosis es una dolencia dolorosa en la que tejido similar al revestimiento del útero crece donde no corresponde, provocando con frecuencia calambres intensos, dolor pélvico persistente y dificultades para concebir. Este artículo explora un aspecto menos conocido de la enfermedad: cómo el propio sistema defensivo del cuerpo, el sistema inmunitario, primero no elimina estas células desplazadas y luego se va desgastando. Comprender este “paisaje inmunitario” cambiante podría ayudar a explicar por qué la endometriosis persiste, empeora con el tiempo y con frecuencia reaparece incluso después de una cirugía.
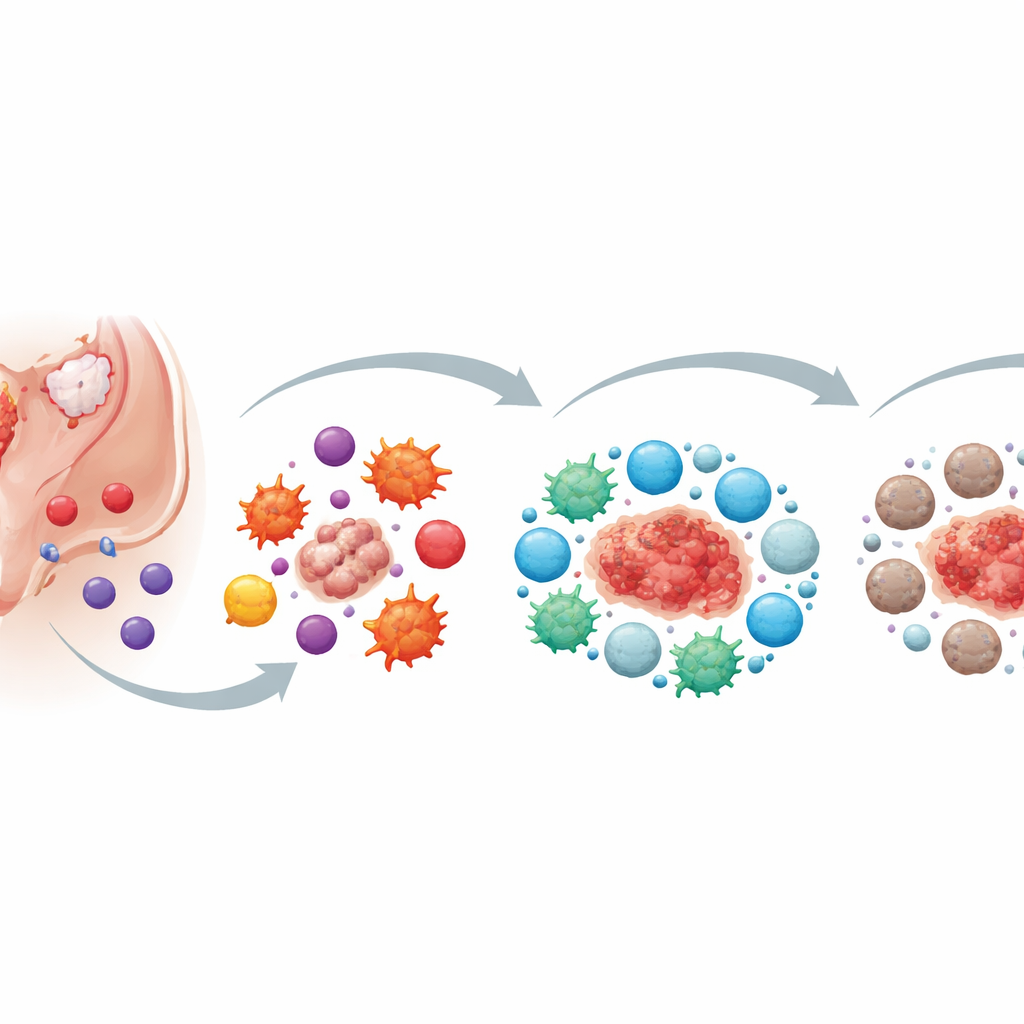
Primeros pasos: cómo las células problemáticas se escapan de las defensas
Los autores describen la fase más temprana como una “evasión inmune”. Normalmente, leucocitos especializados patrullan el organismo y eliminan células anómalas. En la endometriosis, las células endometriales ectópicas (CEE) acaban en la cavidad abdominal, pero las células “asesinas” clave —células NK (natural killer), ciertos linfocitos T y macrófagos— no las eliminan de forma eficaz. Estas células citotóxicas están presentes, pero su capacidad de ataque está debilitada. Sus interruptores activadores están bajados, los inhibidores aumentados, y tienen menor movilidad para llegar al lugar y momento adecuados. Las CEE contribuyen activamente a este fallo liberando mensajeros químicos y pequeñas vesículas de membrana (exosomas) que atenúan la actividad de las células asesinas y reducen la capacidad de los macrófagos para “devorar” células no deseadas.
Ciclos menstruales, ayudantes aparentemente amistosos y una tormenta de inflamación
Cuando la sangre y tejido menstrual refluyen hacia la cavidad abdominal, otros componentes del periodo se incorporan a la historia. Las plaquetas y los productos derivados de la degradación de los glóbulos rojos reducen aún más el poder de ataque de las células NK y de los macrófagos. En lugar de eliminar el tejido desplazado, lo ayudan a adherirse, invadir y crecer. En este punto, el entorno inmune es fuertemente inflamatorio: muchas células liberan señales de alarma que, en teoría, deberían ayudar a combatir el tejido anómalo. Sin embargo, estas mismas señales también fomentan el crecimiento de vasos sanguíneos, la división celular y la invasión por parte de las lesiones endometriósicas. La inflamación se convierte en una espada de doble filo: demasiado débil para eliminar las lesiones, pero lo bastante intensa para alimentar su expansión y el dolor que provocan.
De una inflamación intensa a una calma aparentemente protectora pero dañina
Con el tiempo, el equilibrio de las células inmunitarias alrededor de las lesiones cambia. Al principio predominan macrófagos “atacantes” y linfocitos T colaboradores que liberan señales agresivas que promueven la inflamación. A medida que las lesiones aumentan de tamaño y sangran repetidamente, empiezan a atraer y reconfigurar a otro repertorio de células inmunes —aquellas que apaciguan las respuestas y limitan el daño. Macrófagos antiinflamatorios, células T reguladoras y otros tipos celulares calmantes aumentan en número, atraídos por quimiocinas y moléculas “alarmina” liberadas durante los sangrados repetidos. Las plaquetas y hormonas locales, como el estrógeno, también empujan el sistema hacia un estado más silencioso y antiinflamatorio. Aunque este ambiente más tranquilo protege a los tejidos circundantes de una inflamación crónica y descontrolada, al mismo tiempo protege a las lesiones, favorece la formación de nuevos vasos sanguíneos y estimula la acumulación de tejido fibrótico semejante a cicatriz.
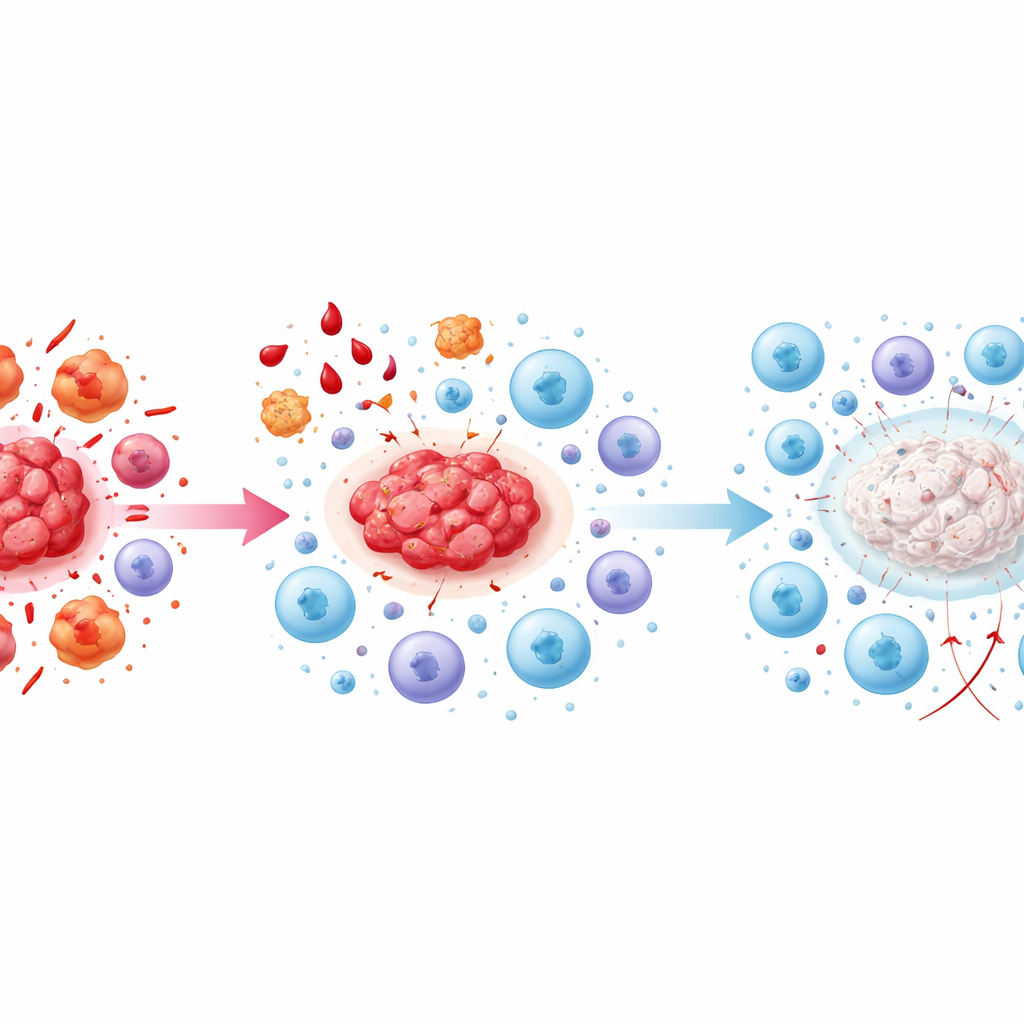
Cuando las células asesinas se quedan sin energía
En fases avanzadas, el artículo describe un estado de “agotamiento inmunitario”. Las células asesinas que en principio podrían atacar las lesiones están ahora crónicamente sobreestimuladas y continuamente suprimidas por señales antiinflamatorias. Comienzan a expresar marcadores de superficie típicos de células fatigadas e ineficaces, y disminuye su producción de moléculas clave de ataque. Señales como TGF-beta e IL-10, producidas por células antiinflamatorias y plaquetas, refuerzan este agotamiento. Mientras tanto, los puntos de control inmunitarios —frenos moleculares que normalmente evitan reacciones excesivas— están cada vez más activados, silenciando aún más la respuesta. El resultado es una situación autosostenida en la que las lesiones persisten, reciben abundante irrigación sanguínea y se vuelven fibróticas, mientras que las propias células que deberían controlarlas están presentes pero en gran medida impotentes.
Qué implica esto para tratamientos futuros
Para un no especialista, la conclusión es que la endometriosis no es solo un problema de tejido desplazado, sino de sincronía y equilibrio en las defensas del organismo. La revisión propone que la enfermedad atraviesa cuatro fases inmunitarias: evasión, inflamación temprana, antiinflamación tardía y, finalmente, agotamiento inmune. Dado que cada fase involucra mezclas distintas de células y señales, los tratamientos que funcionan en un momento pueden fallar en otro. Estrategias que potencien con precisión la actividad de las células asesinas, fomenten el tipo adecuado de inflamación o interrumpan la asociación perjudicial entre plaquetas, hormonas y células inmunes calmantes podrían algún día ralentizar o incluso revertir el crecimiento de las lesiones. Al cartografiar esta línea temporal inmunitaria, los autores buscan orientar terapias más precisas y adaptadas a la fase, y subrayar por qué la simple extracción de lesiones a menudo no es suficiente por sí sola.
Cita: Fan, W., Fengting, Z. & Ruihua, Z. Endometriosis immune microenvironment timing shifts: from immune escape to immune exhaustion. Cell Death Discov. 12, 125 (2026). https://doi.org/10.1038/s41420-026-02965-8
Palabras clave: endometriosis, microambiente inmunitario, inflamación crónica, agotamiento inmunitario, salud de la mujer