Clear Sky Science · zh
EpCAM通过Eomes促进胚胎干细胞退出多能性
从空白细胞到跳动的心脏组织
在发育早期,一小团胚胎细胞具有令人惊讶的能力,能够分化为机体中的任何组织。本研究探讨了这样的“空白”小鼠干细胞如何决定离开那种可塑状态并承诺成为心肌。研究人员关注一种称为EpCAM的细胞表面分子,揭示了它如何帮助触发一个关键的内部基因开关Eomes,引导细胞退出多能性并走向会跳动的心肌细胞。理解这一控制系统可能有助于改进基于干细胞的心脏修复策略,也阐明了早期胚胎如何组织其最初的组织。
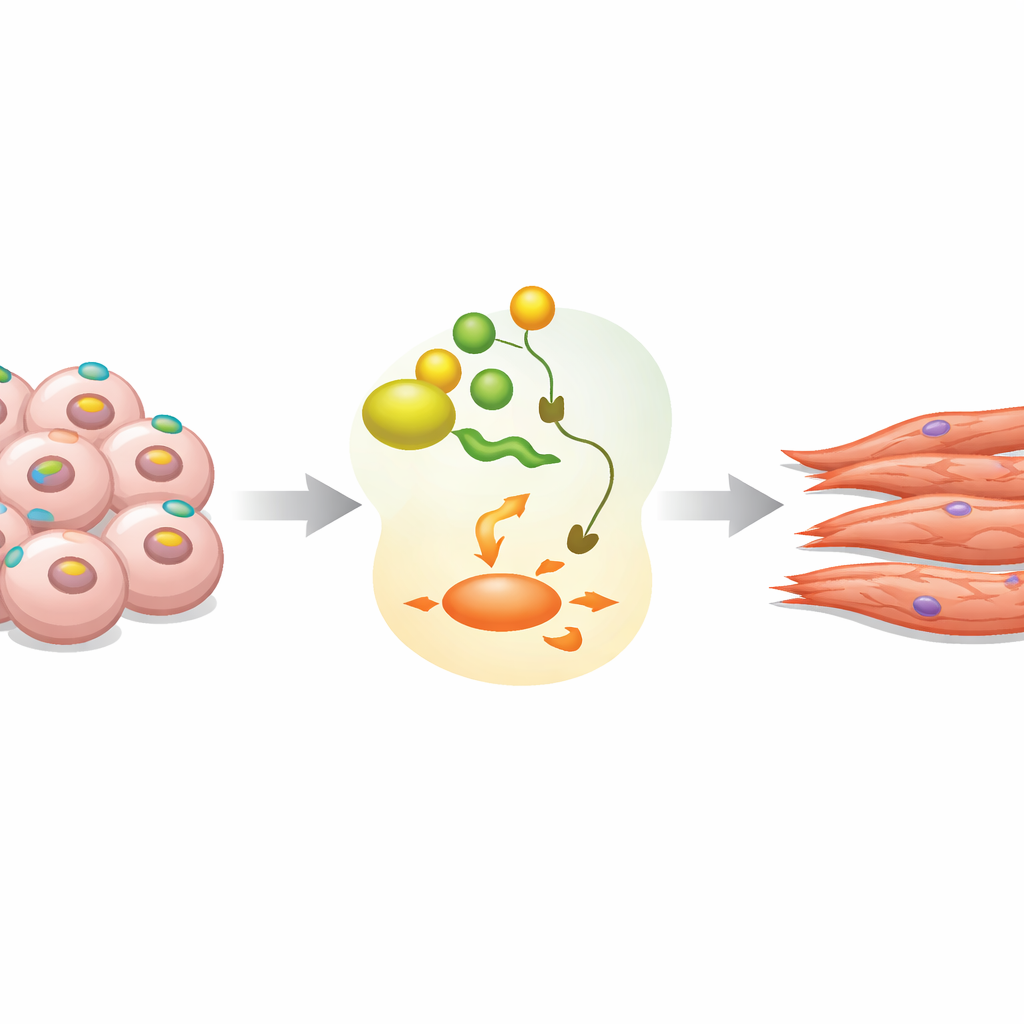
一个表面标志的隐藏企图
EpCAM最为人所知的是作为许多癌症和未成熟干细胞上的标志,但它在早期发育中的确切作用一直不清楚。在以“三维团块”形式培养的胚胎干细胞(称为胚状体)中,研究团队观察到EpCAM几乎出现在初始多能状态的所有细胞上。随着分化开始,EpCAM水平短暂上升,随后在许多细胞中急剧下降,这种模式与真实小鼠和人类胚胎中观察到的相似。早期工作表明,EpCAM过多或过少都会扰乱正常发育,暗示其时序和位置必须精确受控。
缺失EpCAM会发生什么?
为了探究EpCAM的功能,研究人员使用CRISPR构建了缺失Epcam基因的小鼠干细胞系。当这些改造后的细胞在没有额外生长因子的情况下进行分化时,它们形成的胚状体很少产生收缩的心肌。心肌标记物(例如α-心肌肌动蛋白)显著减少。以受控、限时的方式重新引入EpCAM在很大程度上恢复了跳动区域和心脏特异基因的出现,但仅当其表达模式模拟正常的早期脉冲随后消失时才有效。这表明EpCAM不仅是一个被动的标签:它积极支持细胞退出多能性并成为心脏组织的能力。
将EpCAM与内部基因开关连接起来
通过在分化的几天内进行总体和单细胞RNA测序,团队比较了正常细胞与缺失EpCAM的细胞。他们发现,在分化刚开始后不久,缺失EpCAM的细胞无法恰当地激活一组决定谱系的转录因子,包括Eomes、Foxa2和Gata6。其中,Eomes显现为核心因子:已知它驱动早期中胚层和确定性内胚层的形成,这些组织最终形成心脏和肠道等结构。在正常细胞中,Epcam和Eomes在上胚层和类原条(primitive streak)细胞以及早期中胚层中共表达,无论是在胚状体中还是在来自真实小鼠和人类胚胎的公共数据集中均可见。在EpCAM敲除细胞中,Eomes的协同上升被抑制,多能性因子如Nanog比应有的持续时间更长。
一个信号中继:EpCAM、Wnt与Eomes
为了解表面蛋白EpCAM如何影响像Eomes这样的内部调控因子,研究人员考察了主要信号通路。基因集合分析强烈指向Wnt信号,这是一条众所周知在塑造早期体轴和心脏形成中发挥作用的通路。在正常细胞中,Wnt活性随着细胞穿越原条走向心脏命运而增加,这与EpCAM和Eomes的变化同步。在缺失EpCAM的细胞中,这一激增被削弱。在分化最早几天中药理学增强Wnt相关活性可以部分挽救跳动心肌的形成并恢复心脏基因表达。在报告实验中,重新表达EpCAM直接增强了Eomes启动子活性,而阻断Wnt降低了这一效应,支持了EpCAM通过依赖Wnt的途径推动Eomes的模型。
挽救心脏通路及其意义
最后,作者询问是否仅重新开启Eomes就足以绕过EpCAM的缺失。当他们在EpCAM缺失的干细胞中短暂重新表达Eomes时,心肌形成和收缩率显著改善,接近正常细胞的水平。相比之下,仅恢复Foxa2或Gata6并不能可靠地修复缺陷。综合这些结果,EpCAM被定位为一个上游调控因子,在恰当的时刻提升Wnt信号和Eomes,使干细胞能够关闭其可塑的多能程序并承诺成为心肌。对普通读者来说,结论是:一种长期被视为细胞表面简单标签的分子实际上更像一个定时装置——它告诉早期胚胎细胞何时停止成为“任何东西”,开始成为“某种东西”,在本例中即心脏的跳动细胞。
引用: Gong, N., Gouda, M., Balaz, A.M. et al. EpCAM supports exit from pluripotency of embryonic stem cells via Eomes. Cell Death Dis 17, 389 (2026). https://doi.org/10.1038/s41419-026-08734-w
关键词: 胚胎干细胞, EpCAM, Wnt信号, Eomes, 心肌细胞分化