Clear Sky Science · es
EpCAM facilita la salida de la pluripotencia de células madre embrionarias a través de Eomes
De células en blanco a tejido cardíaco palpitante
Al inicio del desarrollo, un pequeño grupo de células embrionarias tiene la notable capacidad de convertirse en cualquier tejido del organismo. Este estudio explora cómo esas células madre de ratón, en estado de "lienzo en blanco", deciden abandonar ese estado flexible y comprometerse a convertirse en músculo cardíaco. Los investigadores se centran en una molécula de superficie llamada EpCAM y descubren cómo ayuda a activar un interruptor genético interno clave, Eomes, guiando a las células fuera de la pluripotencia y hacia cardiomiocitos palpitantes. Entender este sistema de control puede mejorar las estrategias basadas en células madre para reparar el corazón y clarifica cómo los embriones tempranos organizan sus primeros tejidos.
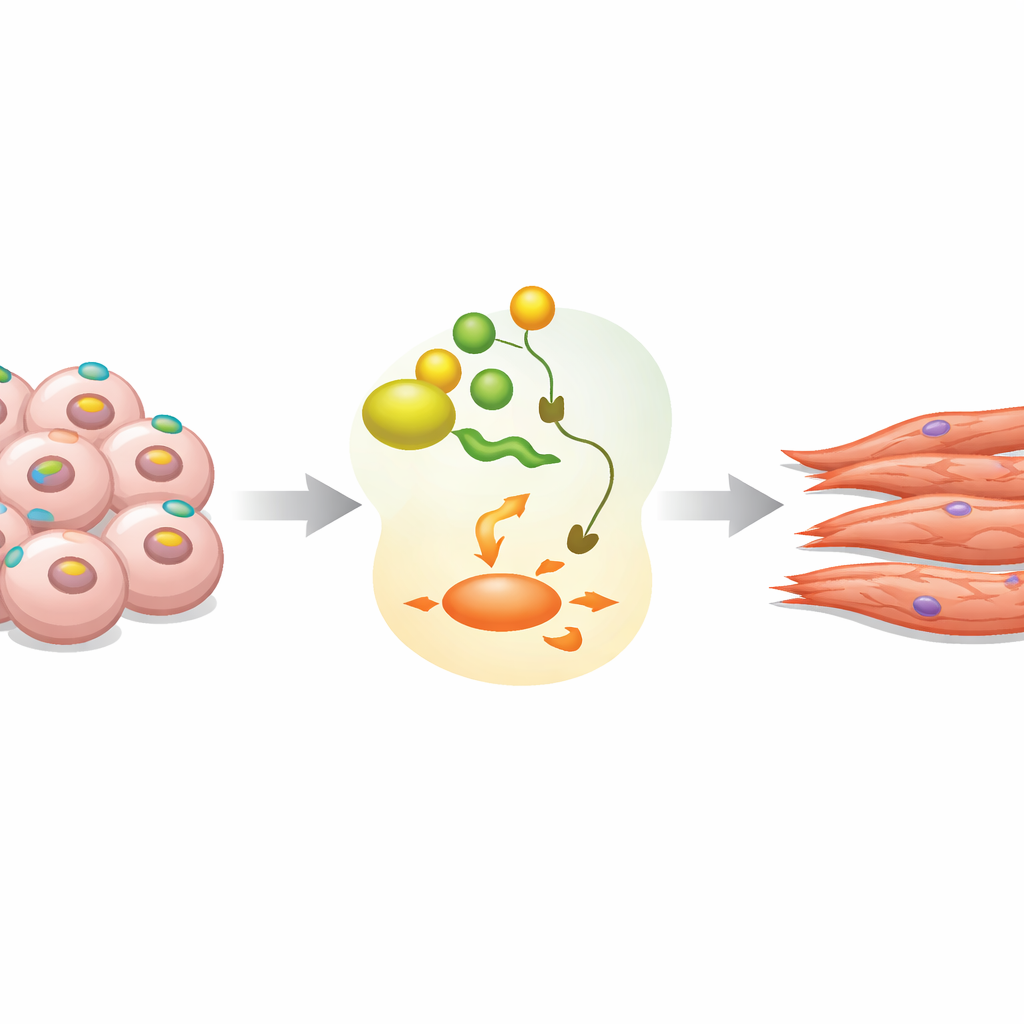
Un marcador de superficie con una agenda oculta
EpCAM es más conocido como un marcador presente en muchos cánceres y en células madre inmaduras, pero su papel exacto durante el desarrollo temprano no quedaba claro. En células madre embrionarias de ratón cultivadas como agregados tridimensionales denominados cuerpos embrioides, el equipo observó que EpCAM aparece en casi todas las células en el estado pluripotente inicial. Cuando comienza la diferenciación, los niveles de EpCAM aumentan brevemente y luego caen bruscamente en muchas células, reflejando patrones observados en embriones reales de ratón y humano. Trabajos anteriores habían mostrado que un exceso o una carencia de EpCAM interfiere con el desarrollo normal, lo que sugiere que su momento y localización deben estar controlados con precisión.
¿Qué sucede cuando falta EpCAM?
Para indagar la función de EpCAM, los investigadores usaron CRISPR para crear líneas de células madre de ratón sin el gen Epcam. Cuando estas células modificadas se dejaron diferenciar sin factores de crecimiento añadidos, formaron cuerpos embrioides que rara vez produjeron músculo cardíaco contratil. Los marcadores de cardiomiocitos, como la alfa-actina cardíaca, se redujeron de forma notable. Reintroducir EpCAM de manera controlada y limitada en el tiempo restauró en gran medida la aparición de zonas palpitantes y de genes específicos del corazón, pero solo cuando el patrón de expresión imitaba el pulso temprano seguido de pérdida que se observa normalmente. Esto demostró que EpCAM no es solo una etiqueta pasiva: apoya activamente la salida de las células de la pluripotencia y su capacidad para formar tejido cardíaco.
Vinculando EpCAM con interruptores génicos internos
Mediante secuenciación de ARN global y a nivel de célula única a lo largo de varios días de diferenciación, el equipo comparó células normales y carentes de EpCAM. Encontraron que, poco después de iniciarse la diferenciación, las células sin EpCAM no activan correctamente un conjunto de factores de transcripción que definen linajes, incluidos Eomes, Foxa2 y Gata6. Entre ellos, Eomes emergió como un actor central: se sabe que impulsa la formación del mesodermo temprano y del endodermo definitivo, tejidos que dan lugar a estructuras como el corazón y el intestino. En células normales, Epcam y Eomes se coexpresan en epiblasto y en células parecidas a la línea primitiva y en el mesodermo temprano, tanto en los cuerpos embrioides como en conjuntos de datos públicos de embriones reales de ratón y humano. En los clones nulos para EpCAM, este incremento coordinado de Eomes está atenuado, y factores de pluripotencia como Nanog perduran más tiempo del debido.
Un relevo de señalización: EpCAM, Wnt y Eomes
Para descubrir cómo una proteína de superficie como EpCAM puede influir en un regulador interno como Eomes, los investigadores examinaron las principales vías de señalización. Los análisis de conjuntos de genes señalaron con fuerza a la señalización Wnt, una vía bien conocida por moldear los ejes corporales tempranos y la formación del corazón. En células normales, la actividad de Wnt aumenta a medida que las células atraviesan la línea primitiva hacia destinos cardíacos, al compás de EpCAM y Eomes. En las células carentes de EpCAM, este aumento está atenuado. Potenciar farmacológicamente la actividad relacionada con Wnt durante los primeros días de diferenciación rescató parcialmente la formación de cardiomiocitos palpitantes y restauró la expresión de genes cardíacos. En experimentos con reporteros, la reexpresión de EpCAM aumentó directamente la actividad del promotor de Eomes, y bloquear Wnt redujo este efecto, lo que apoya un modelo en el que EpCAM ayuda a impulsar Eomes a través de rutas dependientes de Wnt.
Rescatando la vía cardíaca y su significado
Finalmente, los autores se preguntaron si volver a activar Eomes basta para sortear la pérdida de EpCAM. Cuando reexpresaron transitoriamente Eomes en células madre nulas para EpCAM, la formación de cardiomiocitos y las tasas de contracción mejoraron drásticamente, acercándose mucho a las de las células normales. En contraste, restaurar Foxa2 o Gata6 por sí solos no solucionó de forma fiable el defecto. En conjunto, estos resultados sitúan a EpCAM como un regulador ascendente que, en el momento adecuado, potencia la señalización Wnt y Eomes, permitiendo que las células madre apaguen su programa flexible de pluripotencia y se comprometan con el músculo cardíaco. Para un lector general, la conclusión es que una molécula largamente vista como una simple etiqueta en la superficie celular en realidad funciona como un dispositivo de temporización: ayuda a decirles a las células embrionarias tempranas cuándo dejar de ser "cualquier cosa" y empezar a ser "algo", en este caso, las células palpitantes del corazón.
Cita: Gong, N., Gouda, M., Balaz, A.M. et al. EpCAM supports exit from pluripotency of embryonic stem cells via Eomes. Cell Death Dis 17, 389 (2026). https://doi.org/10.1038/s41419-026-08734-w
Palabras clave: células madre embrionarias, EpCAM, señalización Wnt, Eomes, diferenciación a cardiomiocitos