Clear Sky Science · de
EpCAM unterstützt den Ausstieg aus der Pluripotenz embryonaler Stammzellen über Eomes
Von blanken Zellen zum schlagenden Herzgewebe
Früh in der Entwicklung besitzt eine winzige Zellmasse der Embryonen die bemerkenswerte Fähigkeit, sich in jedes Gewebe des Körpers zu verwandeln. Diese Studie untersucht, wie solche „Blanko“-Mausstammzellen entscheiden, diesen flexiblen Zustand zu verlassen und sich zum Herzmuskel zu verpflichten. Die Forschenden konzentrieren sich auf ein Oberflächenmolekül namens EpCAM und zeigen, wie es hilft, einen wichtigen internen genetischen Schalter, Eomes, umzulegen und so die Zellen aus der Pluripotenz in Richtung schlagender Kardiomyozyten zu führen. Das Verständnis dieses Steuerungssystems könnte Stammzellstrategien zur Herzreparatur verbessern und klärt, wie frühe Embryonen ihre ersten Gewebe organisieren.
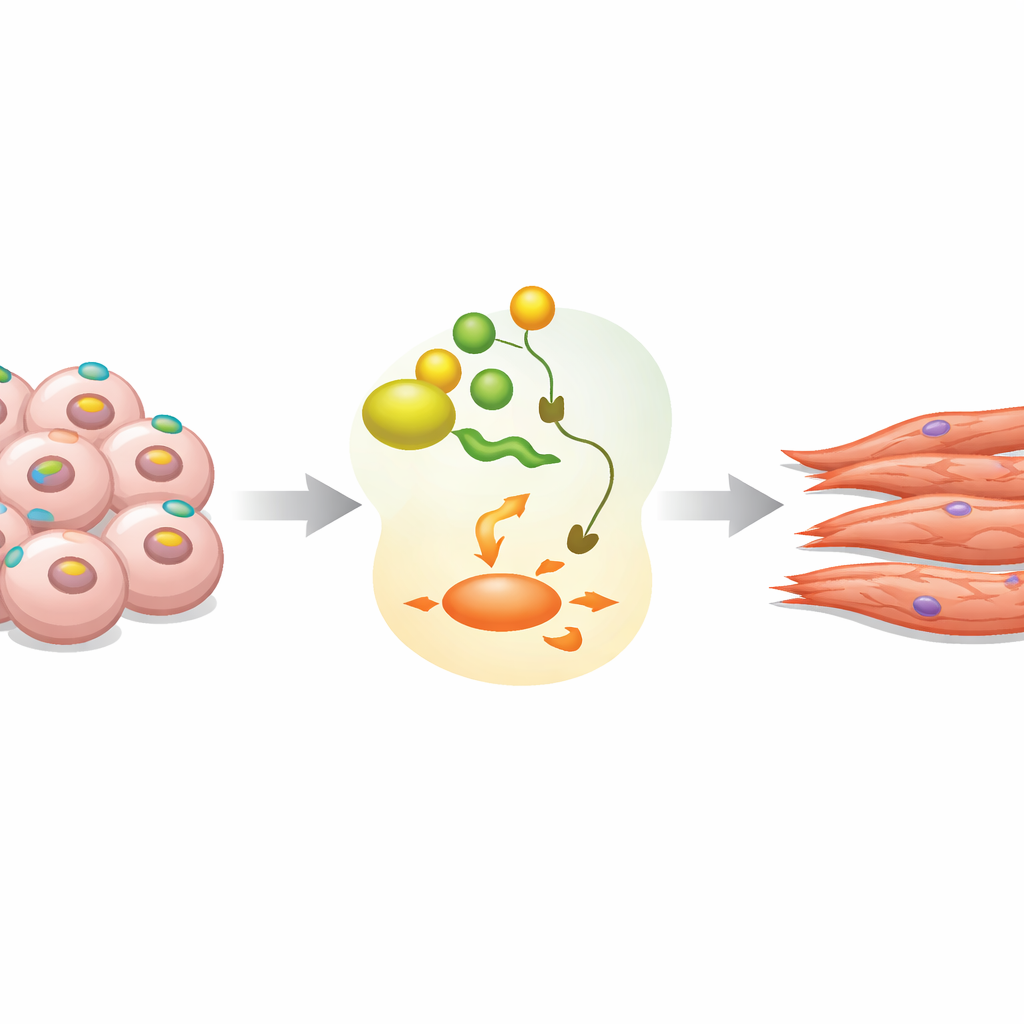
Ein Oberflächenmarker mit verstecktem Plan
EpCAM ist vor allem als Marker bekannt, der auf vielen Krebszellen und auf unreifen Stammzellen vorkommt, doch seine genaue Rolle in der frühen Entwicklung war unklar. In Maus-embryonalen Stammzellen, die als dreidimensionale Klumpen (Embryoid Bodies) kultiviert wurden, beobachtete das Team, dass EpCAM in fast allen Zellen im initialen pluripotenten Zustand vorkommt. Wenn die Differenzierung beginnt, steigen die EpCAM-Spiegel kurz an und fallen dann in vielen Zellen stark ab, ein Muster, das auch in echten Maus- und Humanembryonen zu sehen ist. Frühere Arbeiten hatten gezeigt, dass zu viel oder zu wenig EpCAM die normale Entwicklung stört, was darauf hindeutet, dass Zeitpunkt und Ort seiner Expression genau reguliert werden müssen.
Was passiert, wenn EpCAM fehlt?
Um die Funktion von EpCAM zu untersuchen, nutzten die Forschenden CRISPR, um Mausstammzelllinien zu erzeugen, denen das Epcam-Gen fehlt. Wenn diese veränderten Zellen ohne zusätzliche Wachstumsfaktoren differenziert wurden, bildeten sich Embryoid Bodies, die selten kontrahierenden Herzmuskel erzeugten. Marker von Kardiomyozyten, wie alpha-cardiac actin, waren deutlich reduziert. Die kontrollierte, zeitlich begrenzte Wiedereinführung von EpCAM stellte das Auftreten schlagender Bereiche und herz-spezifischer Gene weitgehend wieder her, allerdings nur, wenn das Expressionsmuster dem normalen frühen Puls gefolgt von Verlust nachgeahmt wurde. Das zeigte, dass EpCAM nicht nur ein passives Etikett ist: Es unterstützt aktiv den Ausstieg aus der Pluripotenz und die Fähigkeit, Herzgewebe zu bilden.
Verknüpfung von EpCAM mit internen Gen-Schaltern
Mithilfe von Bulk- und Einzelzell-RNA-Sequenzierung über mehrere Tage der Differenzierung verglich das Team normale und EpCAM-defiziente Zellen. Sie fanden heraus, dass Zellen ohne EpCAM kurz nach Beginn der Differenzierung eine Reihe linien-definierender Transkriptionsfaktoren nicht richtig aktivieren, darunter Eomes, Foxa2 und Gata6. Unter diesen erwies sich Eomes als zentraler Akteur: Es ist bekannt dafür, die Bildung des frühen Mesoderms und des definitiven Endoderms zu fördern, also der Gewebe, aus denen Strukturen wie Herz und Darm entstehen. In normalen Zellen werden Epcam und Eomes gemeinsam im Epiblast, in primitiven Streifen-ähnlichen Zellen und im frühen Mesoderm exprimiert, sowohl in den Embryoid Bodies als auch in öffentlichen Datensätzen echter Maus- und Humanembryonen. In EpCAM-Knockouts bleibt dieser koordinierte Anstieg von Eomes abgeschwächt, und Pluripotenzfaktoren wie Nanog verharren länger als vorgesehen.
Eine Signalkette: EpCAM, Wnt und Eomes
Um zu klären, wie ein Oberflächenprotein wie EpCAM einen internen Regulator wie Eomes beeinflussen kann, untersuchten die Forschenden wichtige Signalwege. Genmengen-Analysen wiesen stark auf die Wnt-Signalgebung hin, einen Weg, der für die Formung früher Körperachsen und die Herzbildung bekannt ist. In normalen Zellen nimmt die Wnt-Aktivität zu, wenn Zellen den primitiven Streifen Richtung kardialer Schicksale durchlaufen, parallel zu EpCAM und Eomes. In EpCAM-defizienten Zellen fällt dieser Anstieg gedämpft aus. Das pharmakologische Anheben der Wnt-ähnlichen Aktivität in den ersten Tagen der Differenzierung rettete teilweise die Bildung schlagender Kardiomyozyten und stellte die Expression herzbezogener Gene wieder her. In Reporter-Experimenten erhöhte die Wiederexpression von EpCAM direkt die Aktivität des Eomes-Promotors, und das Blockieren von Wnt verringerte diesen Effekt, was ein Modell stützt, in dem EpCAM über Wnt-abhängige Wege zur Aktivierung von Eomes beiträgt.
Wiederherstellung des Herzwegs und seine Bedeutung
Schließlich fragten die Autorinnen und Autoren, ob die Reaktivierung von Eomes ausreicht, um den Verlust von EpCAM zu umgehen. Als sie Eomes transient in EpCAM-null Stammzellen wiederausdrückten, verbesserten sich die Bildung von Kardiomyozyten und die Kontraktionsraten deutlich und näherten sich denen normaler Zellen an. Im Gegensatz dazu reparierte die alleinige Wiederherstellung von Foxa2 oder Gata6 den Defekt nicht zuverlässig. Zusammengenommen positionieren diese Ergebnisse EpCAM als einen upstream-Regulator, der im richtigen Moment Wnt-Signalgebung und Eomes ankurbelt, wodurch Stammzellen ihr flexibles, pluripotentes Programm abschalten und sich zum Herzmuskel verpflichten können. Für die breite Leserschaft lautet die Quintessenz: Ein Molekül, das lange als einfaches Oberflächenetikett betrachtet wurde, wirkt tatsächlich wie ein Zeitgeber: Es hilft frühen embryonalen Zellen zu sagen, wann sie aufhören sollen, „irgendetwas“ zu sein, und anfangen sollen, „etwas“ zu werden — in diesem Fall die schlagenden Zellen des Herzens.
Zitation: Gong, N., Gouda, M., Balaz, A.M. et al. EpCAM supports exit from pluripotency of embryonic stem cells via Eomes. Cell Death Dis 17, 389 (2026). https://doi.org/10.1038/s41419-026-08734-w
Schlüsselwörter: embryonale Stammzellen, EpCAM, Wnt-Signalgebung, Eomes, Kardiomyozyten-Differenzierung