Clear Sky Science · tr
EpCAM, Eomes aracılığıyla embriyonik kök hücrelerin çok yönlülükten çıkmasını destekliyor
Boş Bir Sayfadan Atan Kalp Dokusuna
Gelişimin erken döneminde, küçük bir embriyonik hücre kümesi vücuttaki herhangi bir dokuya dönüşme yeteneğine sahiptir. Bu çalışma, fare “boş sayfa” kök hücrelerinin bu esnek durumdan çıkıp kalp kası olmaya nasıl karar verdiğini araştırıyor. Araştırmacılar, EpCAM adında bir yüzey molekülüne odaklanıyor ve bunun, hücreleri çok yönlülükten çıkarıp Eomes adlı önemli bir içsel gen anahtarını nasıl açtığını ortaya koyuyor; böylece hücreler atıyor ve atan kardiyomiyositlere doğru yönlendiriliyor. Bu kontrol sistemini anlamak, kalp onarımına yönelik kök hücre bazlı stratejileri geliştirebilir ve erken embriyoların ilk dokularını nasıl organize ettiğini açıklığa kavuşturabilir.
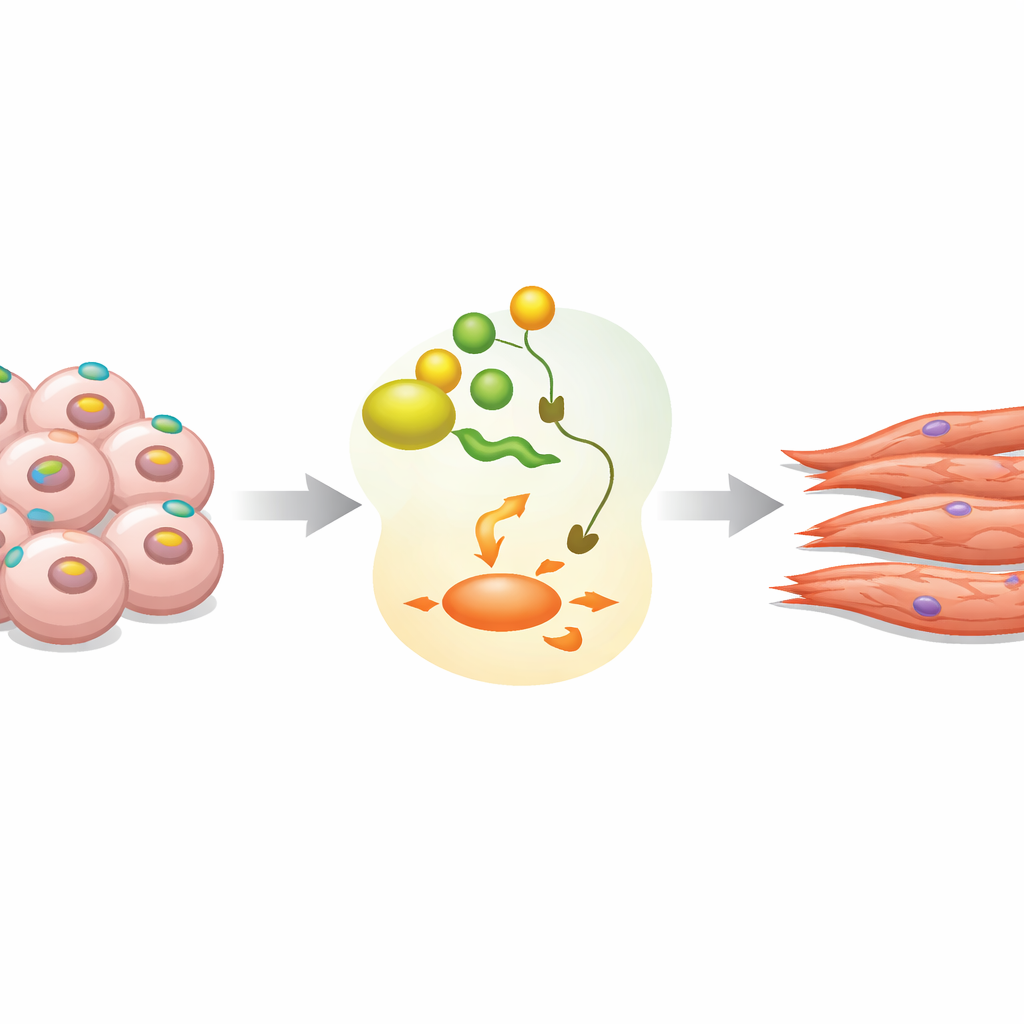
Gizli Bir Amacı Olan Bir Yüzey İşareti
EpCAM en çok birçok kanser hücresinde ve olgunlaşmamış kök hücrelerde bulunan bir belirteç olarak bilinir, ancak erken gelişimdeki kesin rolü belirsiz kalmıştı. Embriyo benzeri üç boyutlu kümeler olan embriyo cisimleri içinde yetiştirilen fare embriyonik kök hücrelerinde araştırma ekibi, EpCAM’in başlangıçtaki çok yönlü durumda neredeyse tüm hücrelerde göründüğünü gözlemledi. Farklılaşma başladığında EpCAM düzeyleri kısa süreliğine yükseliyor, ardından birçok hücrede hızlıca düşüyor; bu, gerçek fare ve insan embriyolarında görülen desenleri yansıtıyor. Önceki çalışmalar, EpCAM’in gereğinden fazla veya az olmasının normal gelişimi bozduğunu göstermişti; bu da zamanlamasının ve konumunun hassas biçimde kontrol edilmesi gerektiğine işaret ediyor.
EpCAM Eksik Olunca Ne Oluyor?
EpCAM’in işlevini araştırmak için araştırmacılar, Epcam geninden yoksun fare kök hücre hatları oluşturmak üzere CRISPR kullandı. Bu değiştirilmiş hücreler ek büyüme faktörü verilmeden farklılaştırılmaya bırakıldığında, nadiren kasılan kalp kası üreten embriyo cisimleri oluşturdu. Alfa-kardiyak aktin gibi kardiyomiyosit belirteçleri güçlü şekilde azaldı. EpCAM’i kontrollü, zaman sınırlı olarak yeniden ifade etmek, erken atıma benzeyen normal ifade düzeni taklit edildiğinde, kasılan alanların ve kalbe özgü genlerin görünümünü büyük ölçüde geri getirdi. Bu, EpCAM’in yalnızca pasif bir etiket olmadığını; hücrelerin çok yönlülükten çıkmasını ve kalp dokusu olabilme yeteneğini etkin biçimde desteklediğini gösterdi.
EpCAM’i İçsel Gen Anahtarlarına Bağlamak
Çok günlük farklılaşma boyunca toplu ve tek hücre RNA dizileme kullanarak, ekip normal ve EpCAM eksik hücreleri karşılaştırdı. Farklılaşma başladıktan kısa bir süre sonra, EpCAM olmayan hücrelerin Eomes, Foxa2 ve Gata6 dahil olmak üzere soy belirleyici transkripsiyon faktörleri setini düzgün şekilde aktive edemediğini buldular. Bunlar arasında Eomes merkezi bir rol olarak öne çıktı: erken mezoderm ve belirgin endoderm oluşumunu yönlendirdiği biliniyor; bu dokular kalp ve bağırsak gibi yapıları oluşturur. Normal hücrelerde Epcam ve Eomes, embriyo cisimlerinde ve gerçek fare ve insan embriyolarından alınan açık veri setlerinde epiblast ve ilkel çizgi benzeri hücrelerde ve erken mezodermde birlikte ifade ediliyor. EpCAM eksiklerindeyse Eomes’in bu koordineli yükselişi zayıflıyor ve Nanog gibi çok yönlülük faktörleri olması gerektiğinden daha uzun süre kalıyor.
Bir Sinyal Rölesi: EpCAM, Wnt ve Eomes
Bir yüzey proteini olan EpCAM’in Eomes gibi içsel bir düzenleyiciyi nasıl etkileyebileceğini ortaya çıkarmak için araştırmacılar önemli sinyal yollarını inceledi. Gen-set analizleri, erken vücut eksenlerini ve kalp oluşumunu şekillendirmesiyle iyi bilinen Wnt sinyalizasyonuna güçlü bir şekilde işaret etti. Normal hücrelerde Wnt aktivitesi, hücreler ilkel çizgiyi geçip kardiyak kaderlere ilerledikçe EpCAM ve Eomes ile eş zamanlı olarak artıyor. EpCAM eksik hücrelerde bu yükseliş sönük kalıyor. Farklılaşmanın ilk günlerinde Wnt ilişkili aktiviteyi farmakolojik olarak artırmak, kasılan kardiyomiyositlerin oluşumunu kısmen kurtardı ve kalp-geni ifadesini restore etti. Raporlayıcı deneylerde EpCAM’in yeniden ifade edilmesi doğrudan Eomes promotör aktivitesini artırdı ve Wnt engellenmesi bu etkiyi azalttı; bu da EpCAM’in Eomes’i Wnt-bağımlı yollarla desteklediği modelini güçlendiriyor.
Kalp Yolunu Kurtarmak ve Anlamı
Son olarak, yazarlar Eomes’i geri açmanın EpCAM kaybını atlamaya yeterli olup olmadığını sordular. EpCAM-noksan kök hücrelerde Eomes’i geçici olarak yeniden ifade ettiklerinde, kardiyomiyosit oluşumu ve kasılma oranları dramatik şekilde iyileşti ve normal hücrelere yakın seviyelere ulaştı. Oysa yalnızca Foxa2 veya Gata6’nın geri verilmesi kusuru güvenilir şekilde düzeltmedi. Birlikte, bu sonuçlar EpCAM’i uygun zamanda Wnt sinyalizasyonunu ve Eomes’i destekleyen üst akışta bir düzenleyici olarak konumlandırıyor; böylece kök hücrelerin esnek, çok yönlü programlarını kapatıp kalp kasına yönelmelerine izin veriyor. Genel okuyucu için çıkarım şudur: uzun süredir hücre yüzeyindeki basit bir etiket olarak görülen bir molekül aslında zamanlama sağlayıcısı gibi davranıyor; erken embriyonik hücrelere ne zaman “her şey” olmayı bırakıp belirli bir şeye—bu durumda kalbin atan hücreleri—dönüşmeye başlamaları gerektiğini söylüyor.
Atıf: Gong, N., Gouda, M., Balaz, A.M. et al. EpCAM supports exit from pluripotency of embryonic stem cells via Eomes. Cell Death Dis 17, 389 (2026). https://doi.org/10.1038/s41419-026-08734-w
Anahtar kelimeler: embriyonik kök hücreler, EpCAM, Wnt sinyalizasyonu, Eomes, kardiyomiyosit farklılaşması