Clear Sky Science · ru
EpCAM способствует выходу эмбриональных стволовых клеток из плюрипотентности через Eomes
От клеток-«чистого листа» до бьющейся тканевой массы сердца
На ранних стадиях развития небольшая группа эмбриональных клеток обладает поразительной способностью превращаться в любую ткань организма. В этом исследовании изучают, как такие «чистые» стволовые клетки мыши решают покинуть это гибкое состояние и обязаться стать сердечной мышцей. Исследователи сосредоточились на молекуле на поверхности клетки, называемой EpCAM, и выяснили, как она помогает активировать ключевой внутриклеточный генетический переключатель Eomes, направляя клетки из плюрипотентности к бьющимся кардиомиоцитам. Понимание этой системы управления может улучшить методы лечения сердца на основе стволовых клеток и прояснить, как ранний эмбрион организует свои первые ткани.
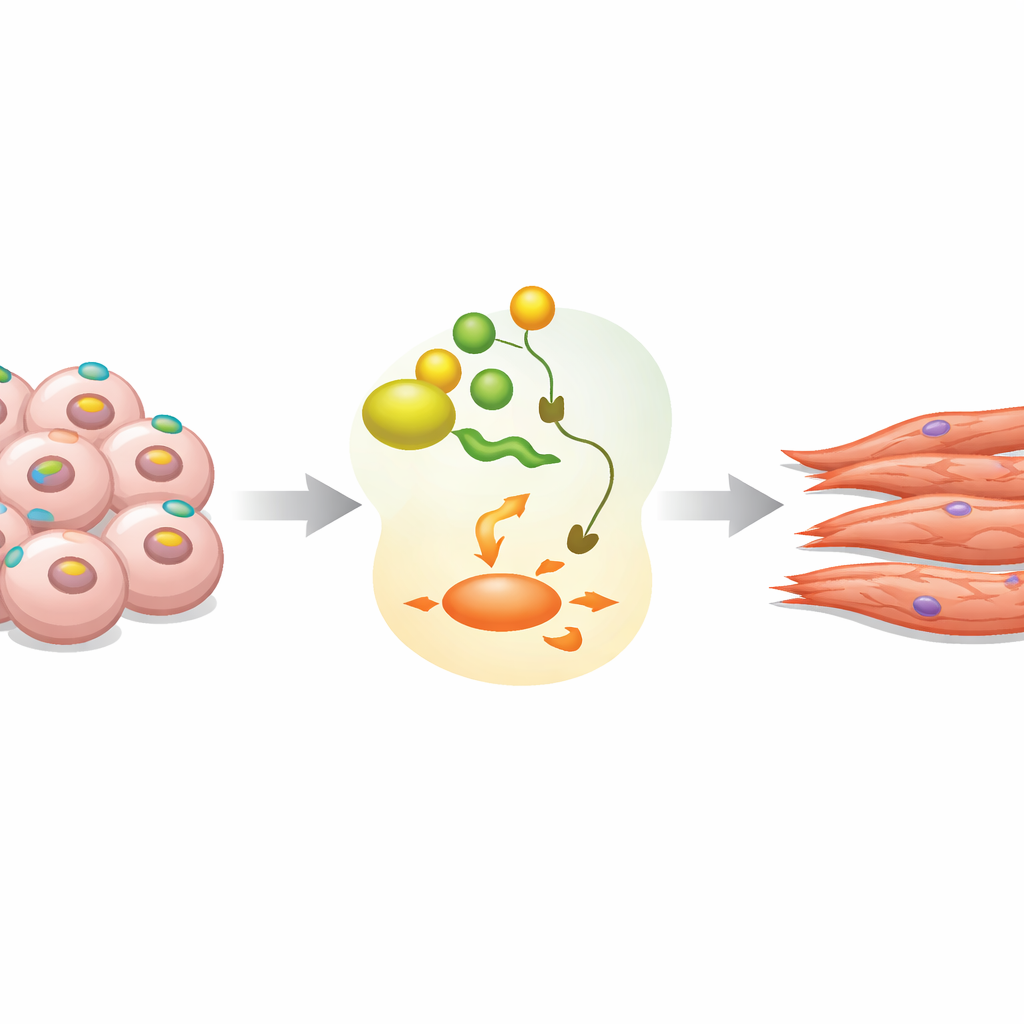
Маркер на поверхности с потайным замыслом
EpCAM наиболее известен как маркер, присутствующий во многих опухолях и на незрелых стволовых клетках, но его точная роль в раннем развитии долго оставалась неясной. В эмбриональных стволовых клетках мыши, выращиваемых в виде трёхмерных скоплений, называемых эмбриоидными телами, исследователи заметили, что EpCAM присутствует почти во всех клетках на начальном плюрипотентном этапе. По мере начала дифференцировки уровни EpCAM кратковременно повышаются, а затем резко снижаются во многих клетках, повторяя рисунки, наблюдаемые в реальных эмбрионах мыши и человека. Предыдущие работы показали, что избыток или недостаток EpCAM нарушает нормальное развитие, что указывает на необходимость точной временной и пространственной регуляции его экспрессии.
Что происходит, когда EpCAM отсутствует?
Чтобы выяснить функцию EpCAM, исследователи использовали CRISPR для создания линий мышиных стволовых клеток с нокаутом гена Epcam. Когда эти модифицированные клетки позволили дифференцироваться без добавления факторов роста, они формировали эмбриоидные тела, которые редко давали сокращающуюся сердечную мышцу. Маркеры кардиомиоцитов, такие как альфа-кардиальный актин, были значительно снижены. Возврат EpCAM в контролируемой, временно ограниченной манере в значительной степени восстановил появление бьющихся областей и экспрессию генов, специфичных для сердца, но только когда модель экспрессии имитировала нормальный ранний импульс с последующей утратой. Это показало, что EpCAM не просто пассивный маркер: он активно способствует выходу клеток из плюрипотентности и их способности становиться сердечной тканью.
Связывание EpCAM с внутренними генетическими переключателями
Используя массовый и одноклеточный РНК‑секвенсинг в течение нескольких дней дифференцировки, команда сравнила нормальные и лишённые EpCAM клетки. Они обнаружили, что вскоре после начала дифференцировки клетки без EpCAM не в состоянии должным образом активировать комплект транскрипционных факторов, определяющих линии развития, включая Eomes, Foxa2 и Gata6. Среди них Eomes проявил себя как центральный игрок: известно, что он стимулирует формирование раннего мезодерма и окончательного энтодерма — тканей, дающих начало таким структурам, как сердце и кишечник. В нормальных клетках Epcam и Eomes ко-экспрессируются в эпибласте и клетках, напоминающих первичную борозду, а также в раннем мезодерме — как в эмбриоидных телах, так и в общедоступных наборах данных реальных эмбрионов мыши и человека. В нокаутах EpCAM согласованное повышение Eomes подавлено, а факторы плюрипотентности, такие как Nanog, сохраняются дольше, чем следует.
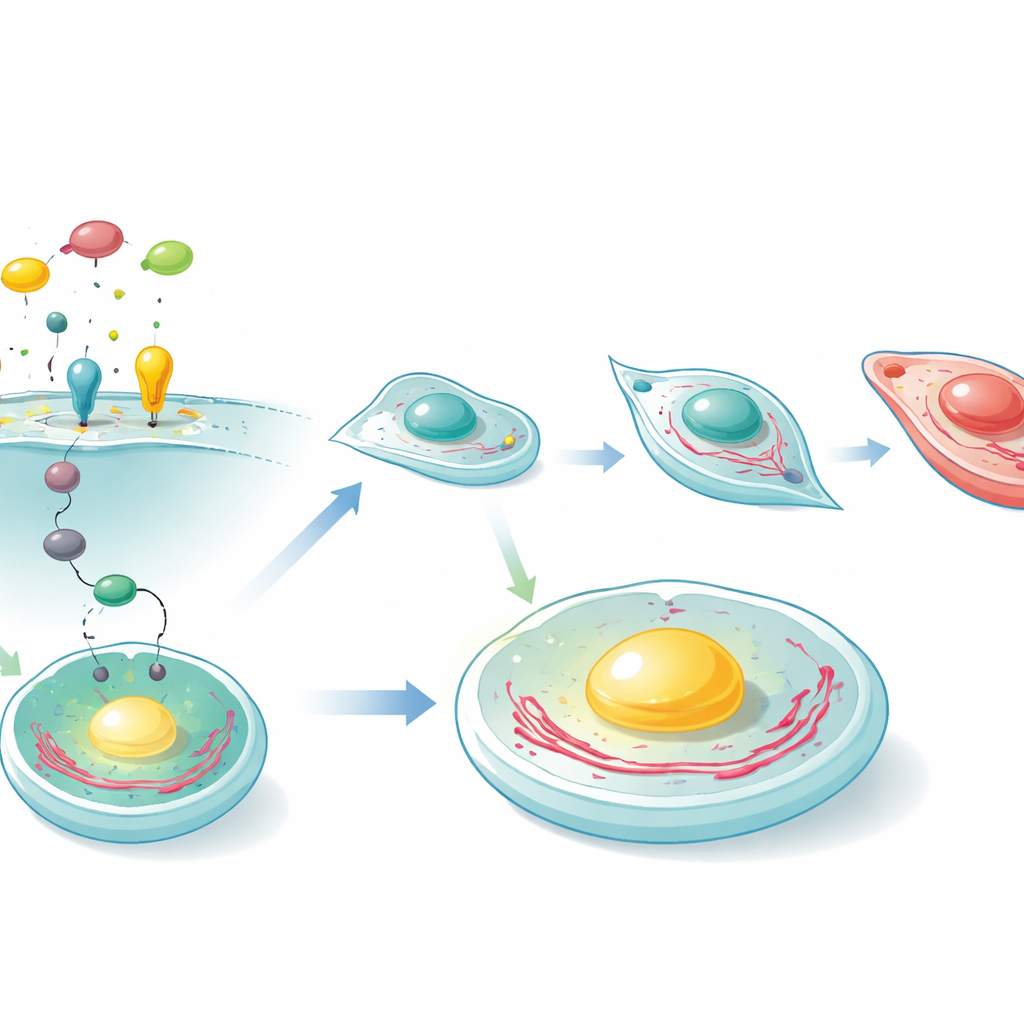
Сигнальная передача: EpCAM, Wnt и Eomes
Чтобы выяснить, как поверхностный белок EpCAM может влиять на внутриклеточный регулятор такой как Eomes, исследователи изучили основные сигнальные пути. Анализы наборов генов сильно указывали на Wnt‑сигнализацию — путь, хорошо известный своей ролью в формировании ранних осей тела и в развитии сердца. У нормальных клеток активность Wnt увеличивается по мере продвижения клеток через структуру, подобную первичной борозде, в направлении кардиальных судьб, синхронно с EpCAM и Eomes. В клетках без EpCAM этот всплеск ослаблен. Фармакологическое усиление Wnt‑связанной активности в первые дни дифференцировки частично спасало образование бьющихся кардиомиоцитов и восстанавливало экспрессию сердечных генов. В эксперименте с репортерами повторная экспрессия EpCAM прямо усиливала активность промотора Eomes, а блокада Wnt уменьшала этот эффект, поддерживая модель, согласно которой EpCAM способствует активации Eomes через Wnt‑зависимые пути.
Восстановление сердечного пути и его значение
Наконец, авторы спросили, достаточно ли повторно включить Eomes, чтобы обойти потерю EpCAM. Когда они временно восстановили экспрессию Eomes в стволовых клетках без EpCAM, образование кардиомиоцитов и частота их сокращений значительно улучшились, приближаясь к показателям нормальных клеток. Напротив, восстановление только Foxa2 или Gata6 надёжно дефект не исправляло. В совокупности эти результаты позиционируют EpCAM как верхний регулятор, который в нужный момент усиливает Wnt‑сигнализацию и Eomes, позволяя стволовым клеткам отключить гибкую программу плюрипотентности и обязаться стать сердечной мышцей. Для непрофессионального читателя вывод таков: молекула, долго воспринимаемая как простой маркер на поверхности клетки, фактически ведёт себя как устройство отсчёта времени — она помогает сказать ранним эмбриональным клеткам, когда перестать быть «кем‑угодно» и начать становиться «чем‑то» — в данном случае бьющимися клетками сердца.
Цитирование: Gong, N., Gouda, M., Balaz, A.M. et al. EpCAM supports exit from pluripotency of embryonic stem cells via Eomes. Cell Death Dis 17, 389 (2026). https://doi.org/10.1038/s41419-026-08734-w
Ключевые слова: эмбриональные стволовые клетки, EpCAM, Wnt-сигнализация, Eomes, дифференцировка в кардиомиоциты