Clear Sky Science · sv
EpCAM stödjer utträde från pluripotens hos embryonala stamceller via Eomes
Från blanka celler till bultande hjärtmuskel
Tidigt i utvecklingen har en liten klump embryonala celler förmågan att förvandlas till vilken vävnad som helst i kroppen. Den här studien undersöker hur sådana ”blanka” musstamceller beslutar sig för att lämna det flexibla tillståndet och åta sig att bli hjärtmuskel. Forskarna fokuserar på ett ytmolekyl kallat EpCAM och kartlägger hur det hjälper till att slå på en viktig intern genetisk brytare, Eomes, vilket styr celler ut ur pluripotens och mot bultande kardiomyocyter. Att förstå detta kontrollsystem kan förbättra stamcellsbaserade strategier för att reparera hjärtat och förtydliga hur tidiga embryo organiserar sina första vävnader.
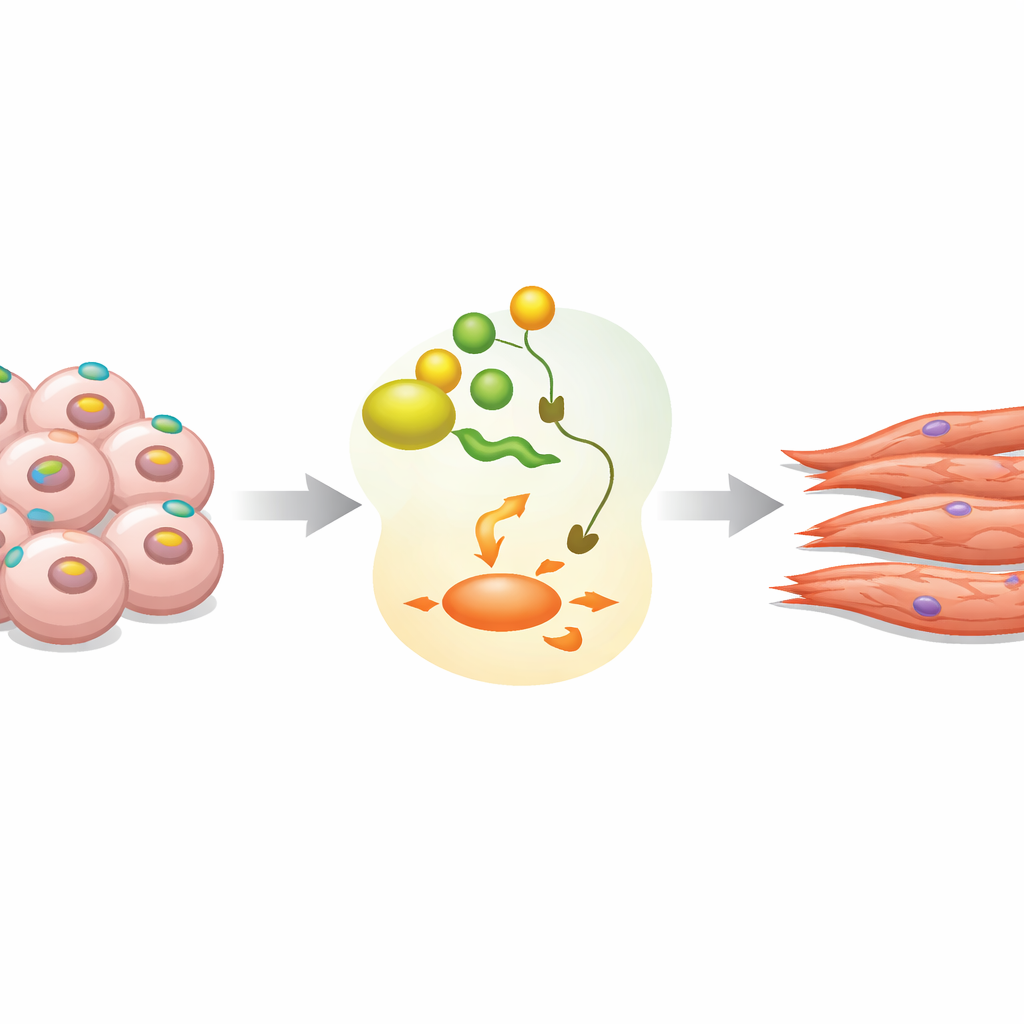
En ytmarkör med en dold agenda
EpCAM är mest känt som en markör som finns på många tumörer och på omogna stamceller, men dess exakta roll under tidig utveckling har varit oklar. I musens embryonala stamceller odlade som tredimensionella kluster, så kallade embryoid bodies, observerade teamet att EpCAM syns på nästan alla celler i det initiala pluripotenta tillståndet. När differentieringen börjar ökar EpCAM-nivåerna kortvarigt för att sedan falla kraftigt i många celler, en förändring som speglar mönster som ses i verkliga mus- och humana embryon. Tidigare arbete har visat att för mycket eller för lite EpCAM stör normal utveckling, vilket antyder att dess timing och lokalisering måste vara noggrant reglerade.
Vad händer när EpCAM saknas?
För att undersöka EpCAMs funktion använde forskarna CRISPR för att skapa musstamcellinjer utan Epcam-genen. När dessa modifierade celler tilläts differentiera utan tillsatta tillväxtfaktorer bildade de embryoid bodies som sällan producerade kontraherande hjärtmuskel. Markörer för kardiomyocyter, såsom alfa-kardiak aktin, var starkt reducerade. Att återintroducera EpCAM i en kontrollerad, tidsbegränsad form återställde i stor utsträckning framkomsten av bultande områden och hjärtspecifika gener, men endast när uttrycksmönstret efterliknade den normala tidiga pulsen följt av förlust. Detta visade att EpCAM inte bara är en passiv etikett: det stödjer aktivt cellernas utträde från pluripotens och deras kapacitet att bli hjärtvävnad.
Koppla EpCAM till interna genetiska brytare
Genom att använda bulk- och enskildcells-RNA-sekvensering över flera dagar av differentiering jämförde teamet normala och EpCAM-defekta celler. De fann att kort efter differentieringens början misslyckas celler utan EpCAM med att korrekt aktivera en svit av linjedefinierande transkriptionsfaktorer, inklusive Eomes, Foxa2 och Gata6. Bland dessa framträdde Eomes som en central spelare: den är känd för att driva bildandet av tidig mesoderm och definitivt endoderm, vävnader som ger upphov till strukturer som hjärta och tarm. I normala celler är Epcam och Eomes samuttryckta i epiblast- och primitive streak-liknande celler samt i tidig mesoderm, både i embryoid bodies och i publika dataset från verkliga mus- och humana embryon. I EpCAM-knockouter är denna koordinerade ökning av Eomes dämpad, och pluripotensfaktorer som Nanog kvarstår längre än de borde.
En signaleringskedja: EpCAM, Wnt och Eomes
För att avgöra hur ett ytprotein som EpCAM kan påverka en intern regulator som Eomes undersökte forskarna stora signalvägar. Gen-setsanalyser pekade starkt mot Wnt-signalering, en väg väl känd för att forma tidiga kroppslinjer och hjärtbildning. I normala celler ökar Wnt-aktiviteten när celler rör sig genom primitive streak mot kardiella öden, i takt med EpCAM och Eomes. I EpCAM-defekta celler är denna ökning dämpad. Farmakologiskt somat Wnt-relaterad aktivitet under de tidigaste dagarna av differentiering räddade delvis bildandet av bultande kardiomyocyter och återställde hjärtgenesuttryck. I rapportorexperiment förbättrade återuttryck av EpCAM direkt Eomes-promotoraktivitet, och blockering av Wnt minskade denna effekt, vilket stöder en modell där EpCAM bidrar till att driva Eomes via Wnt-beroende vägar.
Rädda hjärtvägen och vad det betyder
Slutligen frågade författarna om att återaktivera Eomes är tillräckligt för att kompensera förlusten av EpCAM. När de tillfälligt återuttryckte Eomes i EpCAM-negativa stamceller förbättrades bildandet av kardiomyocyter och kontraktionsfrekvensen dramatiskt, så att de kom nära nivåerna hos normala celler. I kontrast reparerade återställandet av Foxa2 eller Gata6 ensamt inte felet på ett tillförlitligt sätt. Tillsammans placerar dessa resultat EpCAM som en upstream-regulator som, vid rätt ögonblick, förstärker Wnt-signalering och Eomes, vilket tillåter stamceller att stänga ner sitt flexibla, pluripotenta program och åta sig hjärtmuskel. För en allmän läsare är slutsatsen att en molekyl som länge setts som en enkel märkning på cellens yta faktiskt fungerar som en tidpunktssignal: den hjälper till att berätta för tidiga embryonala celler när de ska sluta vara ”vad som helst” och börja bli ”något” — i det här fallet hjärtats bultande celler.
Citering: Gong, N., Gouda, M., Balaz, A.M. et al. EpCAM supports exit from pluripotency of embryonic stem cells via Eomes. Cell Death Dis 17, 389 (2026). https://doi.org/10.1038/s41419-026-08734-w
Nyckelord: embryonala stamceller, EpCAM, Wnt-signalering, Eomes, differentiering till kardiomyocyter