Clear Sky Science · it
EpCAM favorisce l’uscita dalla pluripotenza delle cellule staminali embrionali tramite Eomes
Dalle cellule tabula rasa al tessuto cardiaco che batte
All’inizio dello sviluppo, una piccola massa di cellule embrionali possiede la straordinaria capacità di trasformarsi in qualsiasi tessuto del corpo. Questo studio esplora come tali cellule staminali murine «tabula rasa» decidano di abbandonare quello stato flessibile e impegnarsi a diventare muscolo cardiaco. I ricercatori si concentrano su una molecola di superficie chiamata EpCAM e rivelano come essa contribuisca a attivare un interruttore genetico interno chiave, Eomes, guidando le cellule fuori dalla pluripotenza verso cardiomiociti battenti. Comprendere questo sistema di controllo potrebbe migliorare le strategie basate su cellule staminali per riparare il cuore e chiarire come gli embrioni precoci organizzino i loro primi tessuti.
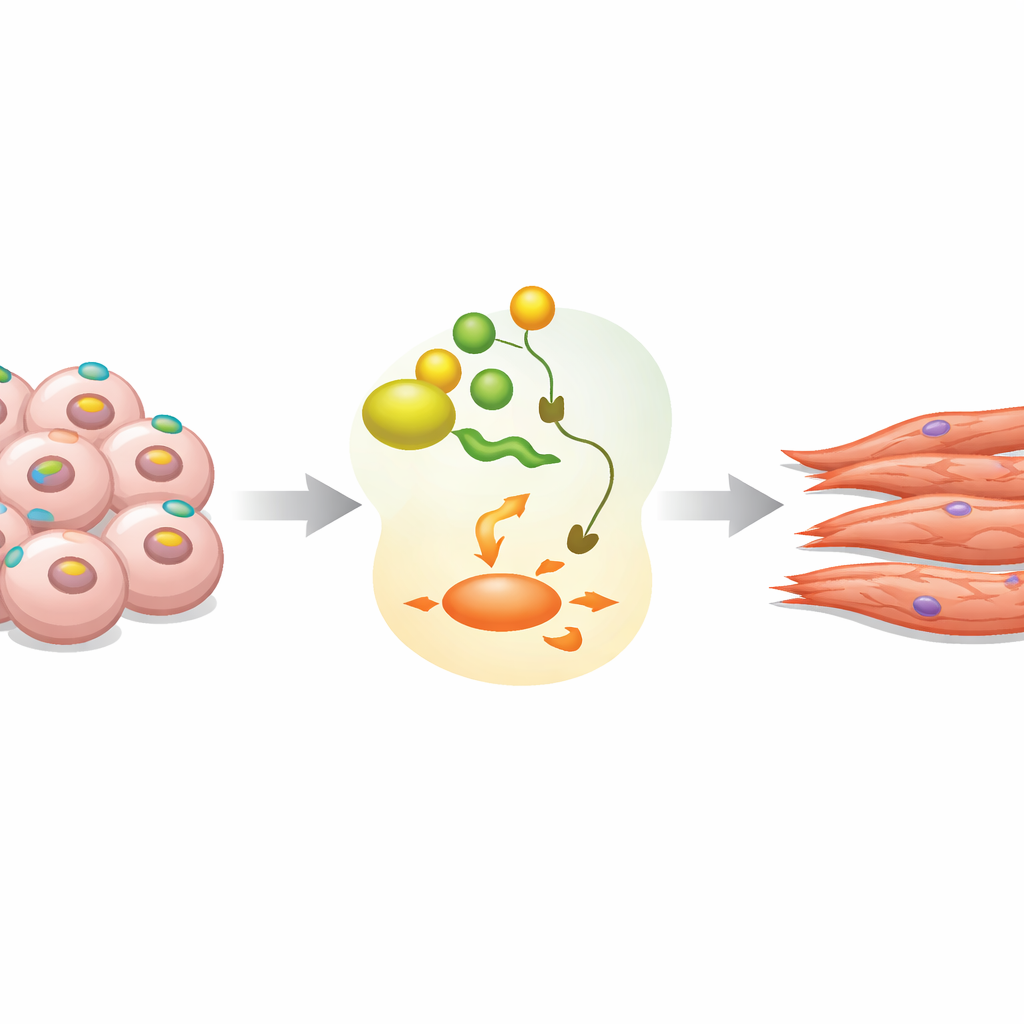
Un marcatore di superficie con un’agenda nascosta
EpCAM è più noto come marcatore presente in molti tumori e nelle cellule staminali immature, ma il suo ruolo esatto durante lo sviluppo precoce è stato poco chiaro. Nelle cellule staminali embrionali murine coltivate come aggregati tridimensionali detti corpi embrionali, il gruppo ha osservato che EpCAM compare in quasi tutte le cellule nello stato pluripotente iniziale. Quando inizia la differenziazione, i livelli di EpCAM aumentano brevemente e poi calano drasticamente in molte cellule, rispecchiando pattern osservati in embrioni di topo e umani reali. Lavori precedenti avevano mostrato che un eccesso o una carenza di EpCAM compromette lo sviluppo normale, suggerendo che il suo timing e la sua localizzazione debbano essere controllati con precisione.
Cosa succede quando EpCAM manca?
Per sondare la funzione di EpCAM, i ricercatori hanno usato CRISPR per creare linee di cellule staminali murine prive del gene Epcam. Quando queste cellule modificate sono state lasciate differenziare senza fattori di crescita aggiunti, hanno formato corpi embrionali che raramente producevano muscolo cardiaco contrattile. I marcatori dei cardiomiociti, come l’alpha-actina cardiaca, risultavano fortemente ridotti. Reinserire EpCAM in modo controllato e temporaneo ha ripristinato in gran parte la comparsa di aree battenti e l’espressione di geni cardiaci, ma solo quando il profilo di espressione imitava il normale impulso iniziale seguito dalla perdita. Ciò dimostra che EpCAM non è solo un’etichetta passiva: sostiene attivamente l’uscita delle cellule dalla pluripotenza e la loro capacità di diventare tessuto cardiaco.
Collegare EpCAM agli interruttori genetici interni
Attraverso RNA-seq bulk e a singola cellula in diversi giorni di differenziazione, il gruppo ha confrontato cellule normali e prive di EpCAM. Hanno scoperto che, poco dopo l’inizio della differenziazione, le cellule senza EpCAM non riescono ad attivare correttamente una serie di fattori di trascrizione definitori di linea, tra cui Eomes, Foxa2 e Gata6. Tra questi, Eomes è emerso come un attore centrale: è noto per promuovere la formazione del mesoderma precoce e dell’endoderma definito, tessuti che danno origine a strutture come cuore e intestino. Nelle cellule normali, Epcam ed Eomes sono co‑espressi in cellule epiblastiche e simili allo strato primitivo e nel mesoderma precoce, sia nei corpi embrionali sia nei dataset pubblici di embrioni murini e umani reali. Nei knockout di EpCAM, questo aumento coordinato di Eomes è attenuato e fattori di pluripotenza come Nanog permangono più a lungo del dovuto.
Un relè di segnalazione: EpCAM, Wnt ed Eomes
Per capire come una proteina di superficie come EpCAM possa influenzare un regolatore interno come Eomes, i ricercatori hanno esaminato le principali vie di segnalazione. Le analisi di insiemi genici hanno indicato con forza la via Wnt, nota per modellare gli assi corporei precoci e la formazione del cuore. Nelle cellule normali, l’attività Wnt aumenta mentre le cellule attraversano lo strato primitivo verso destini cardiaci, in sincronia con EpCAM ed Eomes. Nelle cellule prive di EpCAM, questo aumento è attenuato. Potenziare farmacologicamente l’attività correlata a Wnt durante i primi giorni di differenziazione ha in parte salvato la formazione di cardiomiociti battenti e ripristinato l’espressione dei geni cardiaci. In esperimenti con reporter, la riespressione di EpCAM ha aumentato direttamente l’attività del promotore di Eomes, e il blocco di Wnt ha ridotto questo effetto, supportando un modello in cui EpCAM contribuisce a stimolare Eomes attraverso rotte dipendenti da Wnt.
Ripristinare il percorso cardiaco e il suo significato
Infine, gli autori si sono chiesti se riattivare Eomes fosse sufficiente a bypassare la perdita di EpCAM. Quando hanno riespresso transitoriamente Eomes in cellule staminali prive di EpCAM, la formazione dei cardiomiociti e i tassi di contrazione sono migliorati drasticamente, avvicinandosi molto a quelli delle cellule normali. Al contrario, ripristinare solo Foxa2 o Gata6 non ha risolto in modo affidabile il difetto. Complessivamente, questi risultati pongono EpCAM come un regolatore a monte che, al momento giusto, potenzia la segnalazione Wnt e Eomes, permettendo alle cellule staminali di spegnere il loro programma flessibile di pluripotenza e impegnarsi nel muscolo cardiaco. Per il lettore generale, la conclusione è che una molecola a lungo vista come una semplice etichetta sulla superficie cellulare si comporta in realtà come un dispositivo di temporizzazione: aiuta a dire alle cellule embrionali precoci quando smettere di essere “qualsiasi cosa” e iniziare a diventare “qualcosa” — in questo caso, le cellule battenti del cuore.
Citazione: Gong, N., Gouda, M., Balaz, A.M. et al. EpCAM supports exit from pluripotency of embryonic stem cells via Eomes. Cell Death Dis 17, 389 (2026). https://doi.org/10.1038/s41419-026-08734-w
Parole chiave: cellule staminali embrionali, EpCAM, segnalazione Wnt, Eomes, differenziazione in cardiomiociti