Clear Sky Science · zh
Mitofusin-2通过EGFR/STAT3介导的PD-L1转录抑制肿瘤免疫逃避
为什么我们的细胞有时会忽视癌症
利用免疫系统的癌症治疗已经改变了许多患者的治疗前景,但肿瘤常常学会“明目张胆”地隐藏起来。本研究探讨了癌细胞内一个鲜为人知的守门蛋白,它参与决定免疫细胞是否能识别并攻击肿瘤。理解这一内部开关的工作原理,可能为提高现有免疫治疗的疗效并扩大适应人群提供新思路。
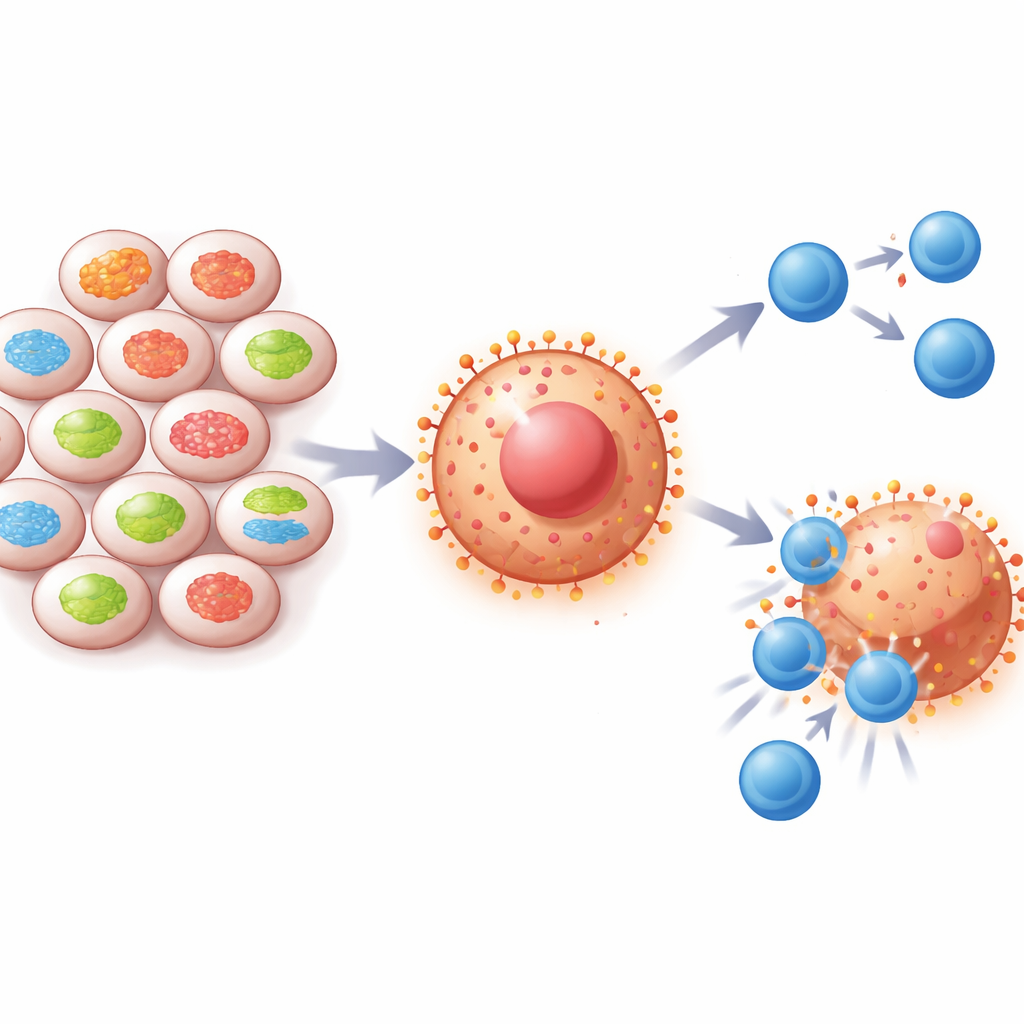
细胞能量中心与肿瘤防御之间的隐秘联系
在每个细胞内部,名为线粒体的小结构既是能量工厂也是通讯枢纽。蛋白质Mitofusin-2(MFN2)帮助线粒体保持连接和健康。研究人员注意到,肺癌和肾癌中MFN2水平常常偏低,且MFN2较少的患者总体生存期倾向较短。与此同时,这些肿瘤显示出较高的PD-L1水平——一种会关闭免疫细胞的“请勿攻击”信号。通过分析患者样本和大型癌症数据库,团队发现当MFN2水平低时,PD-L1通常较高,提示这一线粒体蛋白在某种程度上限制了肿瘤隐藏免疫系统的能力。
肿瘤如何降低MFN2以逃避免疫攻击
为验证这一假设,科学家在多种体外培养的癌细胞(包括肺癌、肾癌和乳腺癌)中改变了MFN2的水平。当他们降低MFN2时,细胞产生更多PD-L1并在细胞表面显示更多,即使在低氧或营养匮乏等模拟肿瘤内部的应激条件下亦是如此。恢复MFN2后,PD-L1水平又回落。在小鼠模型中,缺乏MFN2的肿瘤生长更快,肿瘤内的抗癌CD8 T细胞数量更少。患者的临床样本也呈现类似模式:MFN2丰富的肿瘤含有更多CD8 T细胞,且这些患者对阻断PD-1或PD-L1的药物反应更好。
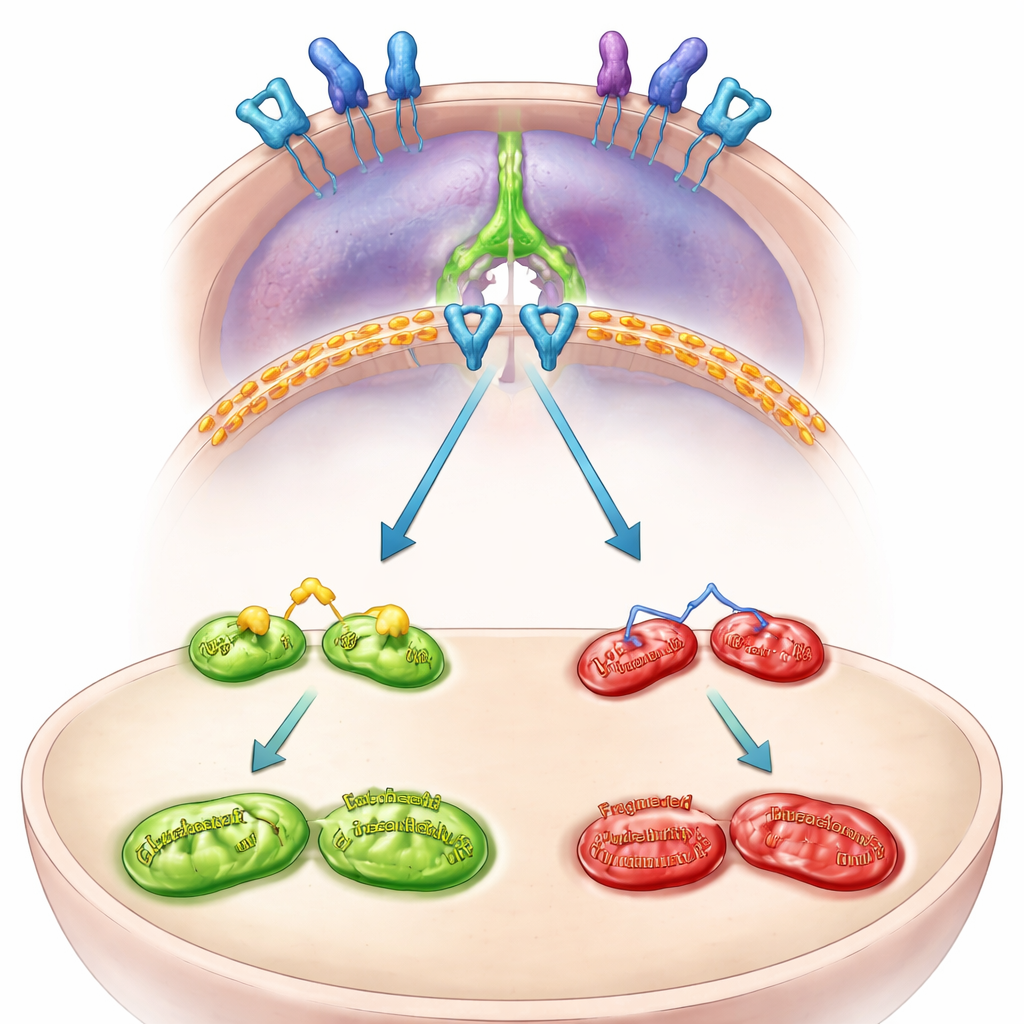
内在线路:从线粒体到免疫逃逸
团队随后绘制了将MFN2与PD-L1相连的内部信号线路。他们发现MFN2通常抑制细胞表面的一条生长信号——EGFR。当MFN2丢失时,EGFR变得更为活跃并激活另一个蛋白STAT3。被激活的STAT3进入细胞核,增强PD-L1的转录指令。阻断MFN2缺失细胞中的EGFR或STAT3可以阻止PD-L1的上升并减少其在细胞表面的表达。在以三维类器官形式培养的患者来源微型肿瘤中,沉默MFN2同样激活了EGFR和STAT3并提高了PD-L1,证实该通路在人体肿瘤中也在起作用,而非仅存在于细胞系中。
让“冷”肿瘤再次变“热”
由于PD-L1帮助肿瘤对免疫攻击变得“冷淡”,科学家们探讨了抑制STAT3是否能在动物体内逆转这一效果。在携带MFN2低表达肿瘤的小鼠中,使用抑制STAT3的药物可延缓肿瘤生长,恢复肿瘤内CD8 T细胞的存在,并增强有助于T细胞聚集和维持活性的免疫信使分子。这些变化表明,即便肿瘤已将MFN2下调,通过针对下游的EGFR–STAT3通路仍可能重新开启免疫攻击之门。
这对未来癌症治疗意味着什么
总体而言,该研究揭示了MFN2——一种以维持线粒体健康著称的蛋白——亦在癌细胞内部充当抑制强大免疫屏蔽通路的刹车。当MFN2丢失时,EGFR和STAT3推动PD-L1上调,帮助肿瘤逃避免疫细胞的识别与清除。检测肿瘤中的MFN2水平可能有助于预测谁将从现有的PD-1/PD-L1药物中受益,而将EGFR或STAT3抑制剂与免疫检查点疗法联合,或能将耐药的“冷”肿瘤转变为免疫系统可再次识别和攻击的目标。
引用: Liu, Y., Wang, N., Li, Z. et al. Mitofusin-2 suppresses tumor immune escape through EGFR/STAT3-mediated PD-L1 transcription. Cell Death Dis 17, 364 (2026). https://doi.org/10.1038/s41419-026-08668-3
关键词: 肿瘤免疫逃避, PD-L1调控, 线粒体动力学, EGFR STAT3信号通路, 癌症免疫治疗耐药