Clear Sky Science · it
Mitofusin-2 sopprime la fuga immunitaria tumorale attraverso la trascrizione di PD-L1 mediata da EGFR/STAT3
Perché a volte le nostre cellule ignorano il cancro
I trattamenti oncologici che sfruttano il sistema immunitario hanno trasformato la cura di molti pazienti, eppure i tumori spesso imparano a nascondersi alla vista. Questo studio esplora una proteina guardiana poco nota all’interno delle cellule tumorali che contribuisce a decidere se le cellule immunitarie possono vedere e attaccare un tumore. Comprendere come funziona questo interruttore interno potrebbe indicare nuove strategie per migliorare l’efficacia delle immunoterapie esistenti e per estenderne i benefici a più persone.
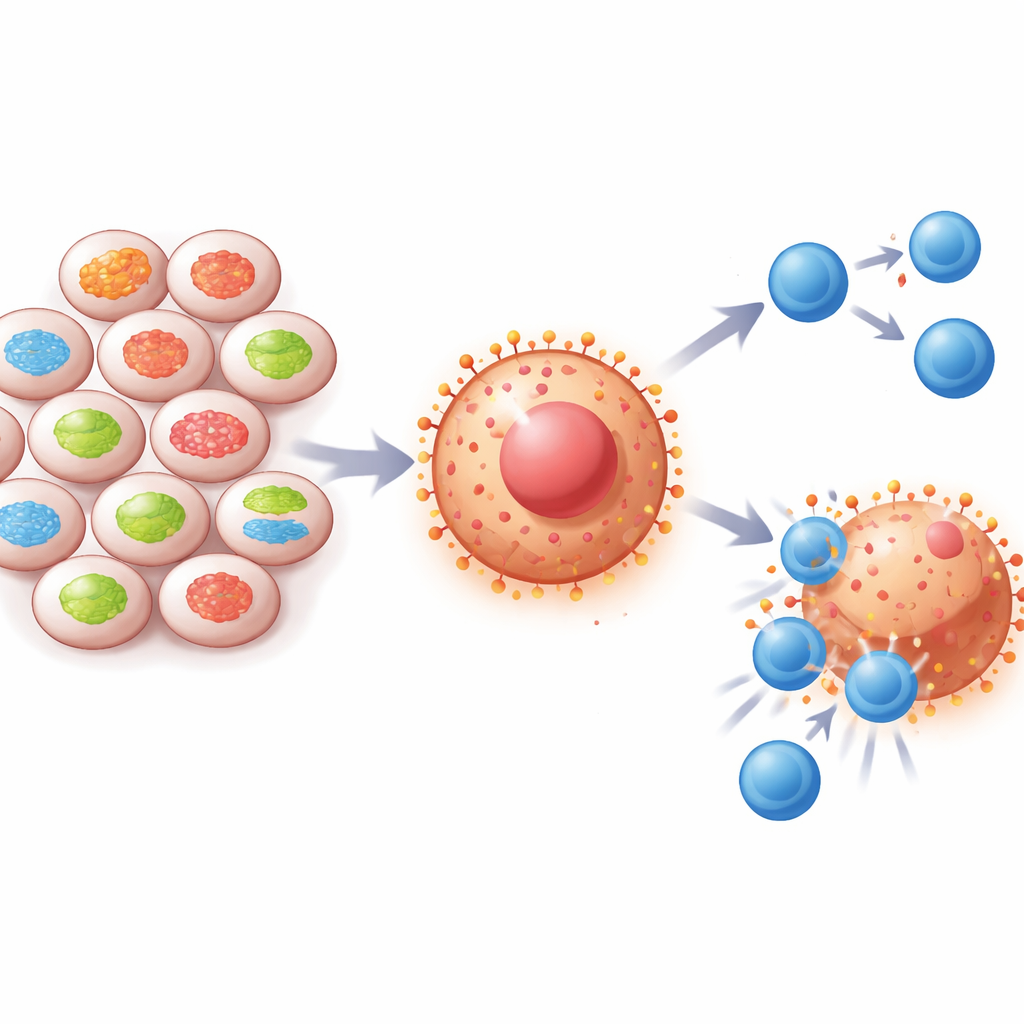
Un legame nascosto tra le centrali cellulari e le difese tumorali
All’interno di ogni cellula, piccole strutture chiamate mitocondri agiscono come centrali energetiche e hub di comunicazione. La proteina Mitofusin-2 (MFN2) aiuta i mitocondri a restare connessi e in salute. I ricercatori hanno osservato che i livelli di MFN2 sono spesso bassi nei tumori polmonari e renali, e i pazienti con meno MFN2 tendono ad avere una sopravvivenza più breve. Allo stesso tempo, questi tumori mostrano elevate quantità di PD-L1, un segnale di “non attaccare” che spegne le cellule immunitarie. Analizzando campioni di pazienti e grandi banche dati sul cancro, il team ha riscontrato che quando MFN2 è bassa, PD-L1 è solitamente alta, suggerendo che questa proteina mitocondriale in qualche modo limita la capacità del tumore di nascondersi al sistema immunitario.
Come i tumori riducono MFN2 per eludere l’attacco immunitario
Per verificare questa ipotesi, gli scienziati hanno alterato i livelli di MFN2 in diversi tipi di cellule tumorali coltivate in laboratorio, incluse cellule di cancro del polmone, del rene e della mammella. Quando hanno ridotto MFN2, le cellule producevano più PD-L1 e ne esponevano di più sulla superficie, anche in condizioni stressanti come basso ossigeno o scarse risorse nutritive che imitano l’interno del tumore. Ripristinando MFN2, PD-L1 tornava a diminuire. In modelli murini, i tumori privi di MFN2 crescevano più rapidamente e presentavano un numero minore di cellule CD8 T anti-tumore al loro interno. I campioni clinici dei pazienti hanno mostrato uno schema simile: i tumori più ricchi di MFN2 contenevano più cellule CD8 T e quei pazienti rispondevano meglio ai farmaci che bloccano PD-1 o PD-L1.
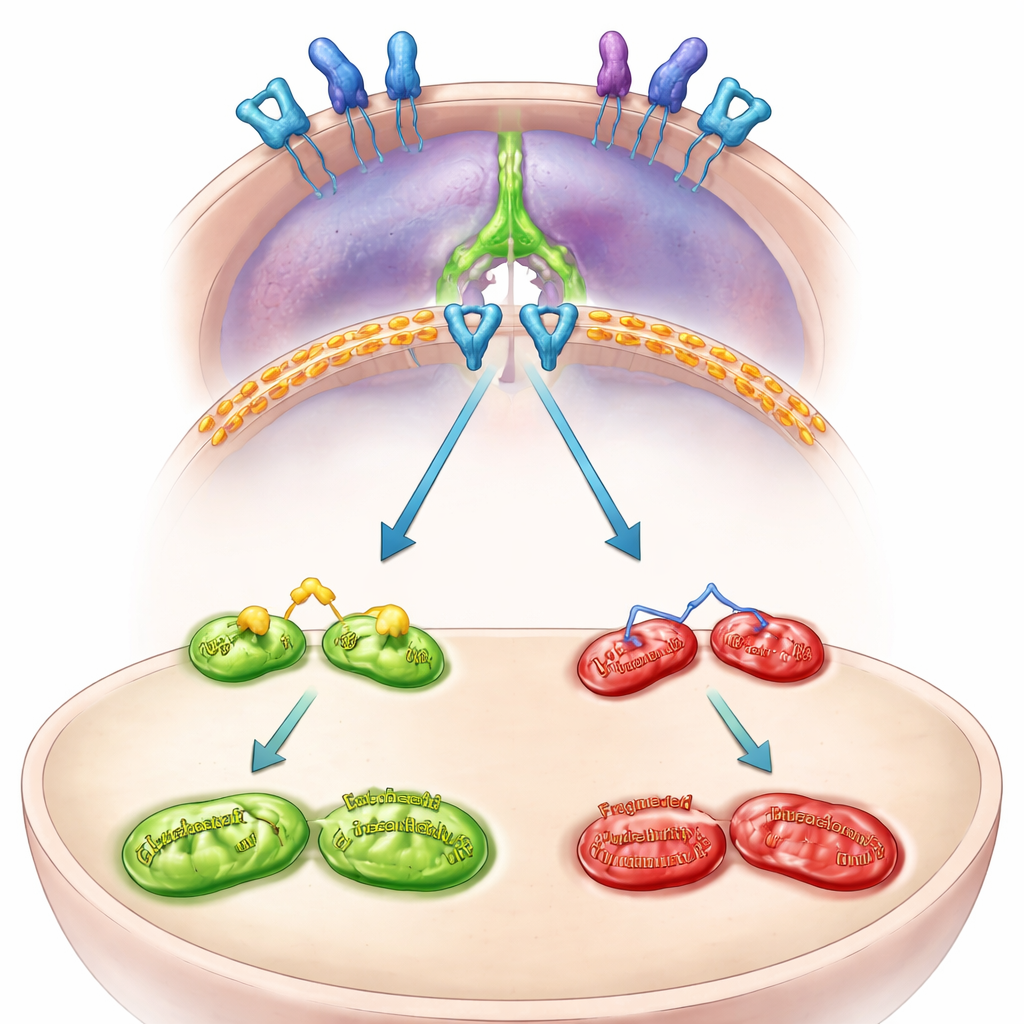
Il cablaggio interno: dai mitocondri alla fuga immunitaria
Il team ha quindi mappato il circuito interno che collega MFN2 a PD-L1. Hanno scoperto che MFN2 normalmente tiene sotto controllo un segnale di crescita sulla superficie cellulare chiamato EGFR. Quando MFN2 viene perso, EGFR diventa più attivo e attiva a sua volta un’altra proteina, STAT3. STAT3 attivata migra nel nucleo della cellula e aumenta le istruzioni per la produzione di PD-L1. Bloccare EGFR o STAT3 in cellule carenti di MFN2 impediva l’aumento di PD-L1 e ne riduceva la presenza sulla superficie cellulare. In mini-tumori derivati dai pazienti e coltivati come organoidi tridimensionali, il silenziamento di MFN2 riattivava EGFR e STAT3 e aumentava PD-L1, confermando che questa via è attiva nei tumori umani, non solo nelle linee cellulari.
Riscaldare di nuovo i tumori “freddi”
Poiché PD-L1 aiuta i tumori a diventare “freddi” all’attacco immunitario, gli scienziati si sono chiesti se bloccare STAT3 potesse invertire questo effetto negli animali. Nei topi con tumori a basso contenuto di MFN2, il trattamento con farmaci inibitori di STAT3 ha rallentato la crescita tumorale, ripristinato la presenza delle cellule CD8 T all’interno dei tumori e aumentato i messaggeri immunitari che favoriscono il reclutamento e l’attività delle cellule T. Questi cambiamenti suggeriscono che anche quando i tumori hanno già ridotto MFN2, potrebbe essere ancora possibile riaprire la porta all’attacco immunitario mirando alla via EGFR–STAT3 a valle.
Cosa significa per i futuri trattamenti del cancro
Nel complesso, lo studio rivela che MFN2, una proteina nota soprattutto per mantenere la salute mitocondriale, agisce anche come freno su una potente via che protegge i tumori dall’immunità. Quando MFN2 viene persa, EGFR e STAT3 aumentano PD-L1, aiutando i tumori a sfuggire al riconoscimento e alla distruzione da parte delle cellule immunitarie. Misurare MFN2 nei tumori potrebbe aiutare a prevedere chi trarrà beneficio dai farmaci anti-PD-1/PD-L1, e combinare inibitori di EGFR o STAT3 con terapie di checkpoint potrebbe trasformare tumori resistenti e “freddi” in tumori che il sistema immunitario può di nuovo riconoscere e attaccare.
Citazione: Liu, Y., Wang, N., Li, Z. et al. Mitofusin-2 suppresses tumor immune escape through EGFR/STAT3-mediated PD-L1 transcription. Cell Death Dis 17, 364 (2026). https://doi.org/10.1038/s41419-026-08668-3
Parole chiave: fuga immunitaria tumorale, regolazione di PD-L1, dinamiche mitocondriali, segnalizzazione EGFR STAT3, resistenza all’immunoterapia contro il cancro