Clear Sky Science · de
Mitofusin-2 unterdrückt die tumorbedingte Immunflucht durch EGFR/STAT3-vermittelte PD-L1-Transkription
Warum unsere Zellen Krebs manchmal ignorieren
Immunbasierte Krebstherapien haben die Behandlung vieler Patientinnen und Patienten grundlegend verändert, doch Tumoren lernen oft, sich offen zu verbergen. Diese Studie untersucht ein wenig bekanntes Wächterprotein innerhalb von Krebszellen, das mitentscheidet, ob Immunzellen einen Tumor sehen und angreifen können. Zu verstehen, wie dieser interne Schalter funktioniert, könnte neue Wege aufzeigen, bestehende Immuntherapien wirksamer und für mehr Menschen zugänglich zu machen.
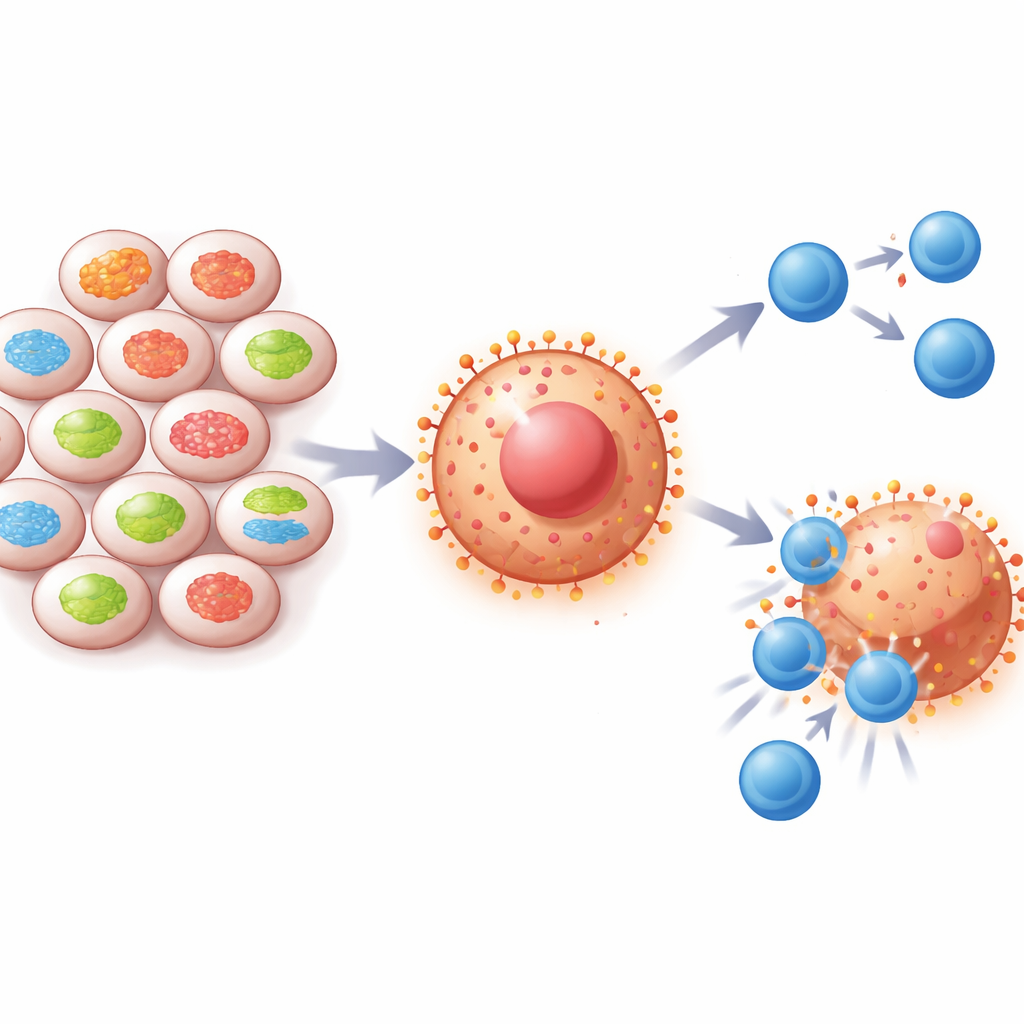
Eine verborgene Verbindung zwischen Zellkraftwerken und Krebsabwehr
In jeder Zelle wirken winzige Strukturen, die Mitochondrien, als Kraftwerke und Kommunikationszentren. Das Protein Mitofusin-2 (MFN2) sorgt dafür, dass Mitochondrien vernetzt und gesund bleiben. Die Forschenden stellten fest, dass MFN2-Spiegel in Lungen- und Nierenkrebs häufig niedrig sind und Patientinnen und Patienten mit weniger MFN2 tendenziell eine kürzere Überlebenszeit haben. Gleichzeitig zeigen diese Tumoren hohe Mengen an PD-L1, einem „Nicht angreifen“-Signal, das Immunzellen ausschaltet. Anhand von Patientenproben und großen Krebsdatenbanken fanden die Forschenden, dass bei niedrigem MFN2 meist hoher PD-L1-Spiegel vorliegt, was nahelegt, dass dieses mitochondriale Protein die Fähigkeit des Tumors, sich vor dem Immunsystem zu verbergen, bremst.
Wie Tumoren MFN2 herunterregulieren, um Immunschutz zu erlangen
Um diese Idee zu prüfen, veränderten die Wissenschaftlerinnen und Wissenschaftler die MFN2-Spiegel in verschiedenen im Labor gezüchteten Krebszelltypen, darunter Lungen-, Nieren- und Brustkrebszellen. Bei reduziertem MFN2 produzierten die Zellen mehr PD-L1 und zeigten mehr davon an ihrer Oberfläche, selbst unter Stressbedingungen wie Sauerstoffmangel oder Nährstoffarmut, die das Tumorinnere nachahmen. Wurde MFN2 wiederhergestellt, sank PD-L1 wieder. In Mausmodellen wuchsen Tumoren ohne MFN2 schneller und enthielten weniger krebsbekämpfende CD8-T-Zellen. Klinische Proben von Patientinnen und Patienten zeigten ein ähnliches Muster: Tumoren mit mehr MFN2 wiesen mehr CD8-T-Zellen auf, und diese Patienten sprachen besser auf Medikamente an, die PD-1 oder PD-L1 blockieren.
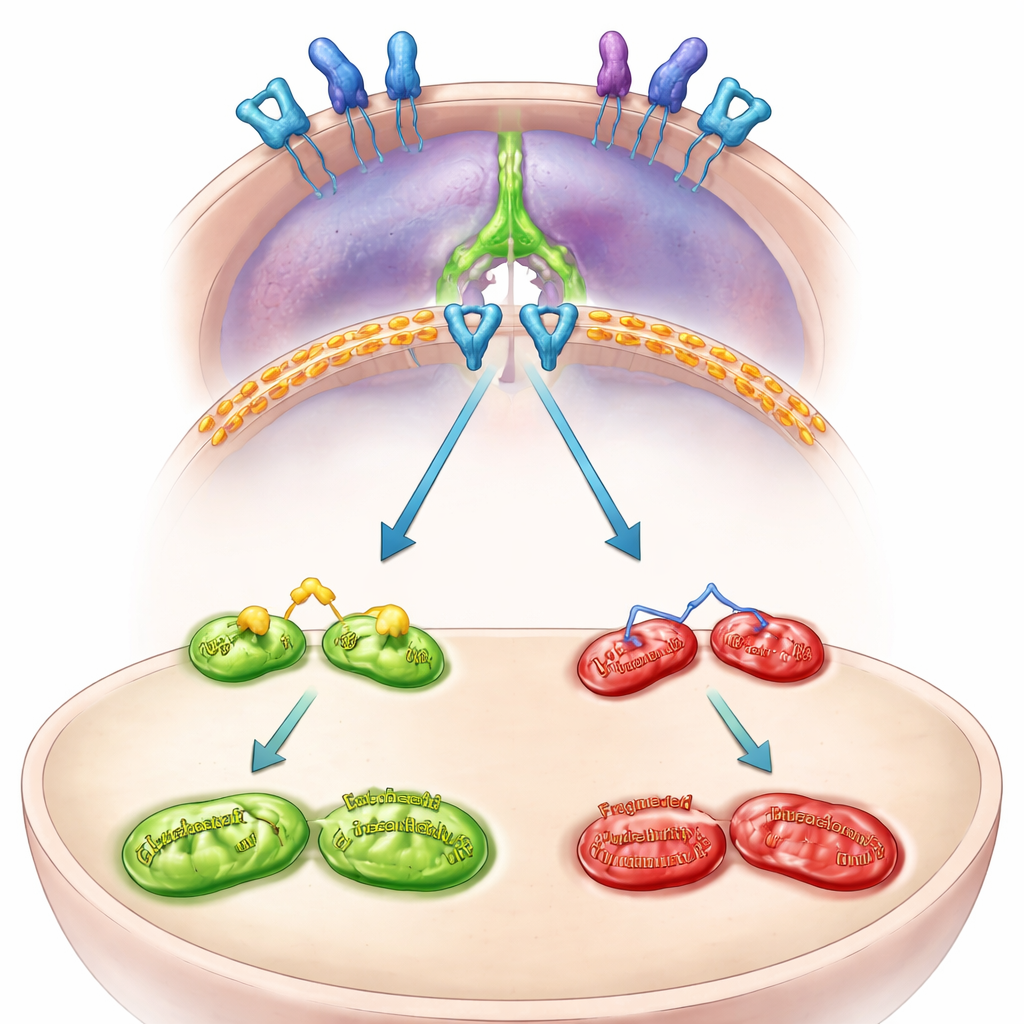
Die interne Verdrahtung: von Mitochondrien zur Immunflucht
Das Team kartierte anschließend die interne Signalverdrahtung, die MFN2 mit PD-L1 verbindet. Sie fanden heraus, dass MFN2 normalerweise ein Wachstumssignal an der Zelloberfläche, das EGFR genannt wird, in Schach hält. Geht MFN2 verloren, wird EGFR aktiver und aktiviert das Protein STAT3. Aktiviertes STAT3 wandert in den Zellkern und verstärkt die Genanweisung zur Produktion von PD-L1. Das Blockieren von EGFR oder STAT3 in MFN2-defizienten Zellen verhinderte den Anstieg von PD-L1 und reduzierte seine Präsenz auf der Zelloberfläche. In aus Patienten gewonnenen Mini-Tumoren, die als dreidimensionale Organoide gezüchtet wurden, schaltete das Abschalten von MFN2 ebenfalls EGFR und STAT3 ein und erhöhte PD-L1, was bestätigte, dass dieser Signalweg in menschlichen Tumoren und nicht nur in Zelllinien aktiv ist.
Kalte Tumoren wieder heiß machen
Da PD-L1 Tumoren gegenüber Immunattacken „kalt“ macht, prüften die Forschenden, ob das Ausschalten von STAT3 diesen Effekt in Tiermodellen umkehren kann. In Mäusen mit MFN2-armen Tumoren verlangsamte die Behandlung mit STAT3-blockierenden Wirkstoffen das Tumorwachstum, stellte die Präsenz von CD8-T-Zellen in den Tumoren wieder her und steigerte Immunbotenstoffe, die T-Zellen anlocken und aktiv halten. Diese Änderungen deuten darauf hin, dass selbst wenn Tumoren MFN2 bereits herunterreguliert haben, es möglich sein könnte, die Tür zur Immunattacke wieder zu öffnen, indem der nachgeschaltete EGFR–STAT3‑Signalweg gezielt wird.
Was das für die zukünftige Krebstherapie bedeutet
Insgesamt zeigt die Studie, dass MFN2, ein Protein, das vor allem für die Aufrechterhaltung mitochondrialer Gesundheit bekannt ist, auch als Bremse eines starken immunabschirmenden Signalwegs in Krebszellen wirkt. Geht MFN2 verloren, treiben EGFR und STAT3 PD-L1 in die Höhe und helfen Tumoren, der Erkennung und Zerstörung durch das Immunsystem zu entgehen. Die Messung von MFN2 in Tumoren könnte dabei helfen vorherzusagen, wer von aktuellen PD-1/PD-L1‑Medikamenten profitiert; die Kombination von EGFR‑ oder STAT3‑Inhibitoren mit Checkpoint‑Therapien könnte resistente, „kalte“ Tumoren in solche verwandeln, die das Immunsystem wieder erkennen und angreifen kann.
Zitation: Liu, Y., Wang, N., Li, Z. et al. Mitofusin-2 suppresses tumor immune escape through EGFR/STAT3-mediated PD-L1 transcription. Cell Death Dis 17, 364 (2026). https://doi.org/10.1038/s41419-026-08668-3
Schlüsselwörter: tumorbedingte Immunflucht, PD-L1-Regulation, mitochondriale Dynamik, EGFR-STAT3-Signalübertragung, Resistenz gegen Krebsimmuntherapie