Clear Sky Science · ar
ميتوفيوزين-2 يثبط هروب الورم من الجهاز المناعي عبر نسخ PD-L1 بوساطة EGFR/STAT3
لماذا تتجاهل خلايانا أحيانًا السرطان
لقد غيّرت العلاجات السرطانية التي تستفيد من الجهاز المناعي معايير الرعاية للعديد من المرضى، إلا أن الأورام كثيرًا ما تتعلّم كيف تختبئ في وضح النهار. تستكشف هذه الدراسة بروتينًا حارسًا قليل المعرفة داخل خلايا السرطان يساعد على تقرير ما إذا كانت الخلايا المناعية تستطيع رؤية الورم ومهاجمته. وفهم كيفية عمل هذا المفتاح الداخلي قد يشير إلى طرق جديدة لجعل العلاجات المناعية الحالية أكثر فعالية ولعدد أكبر من المرضى.
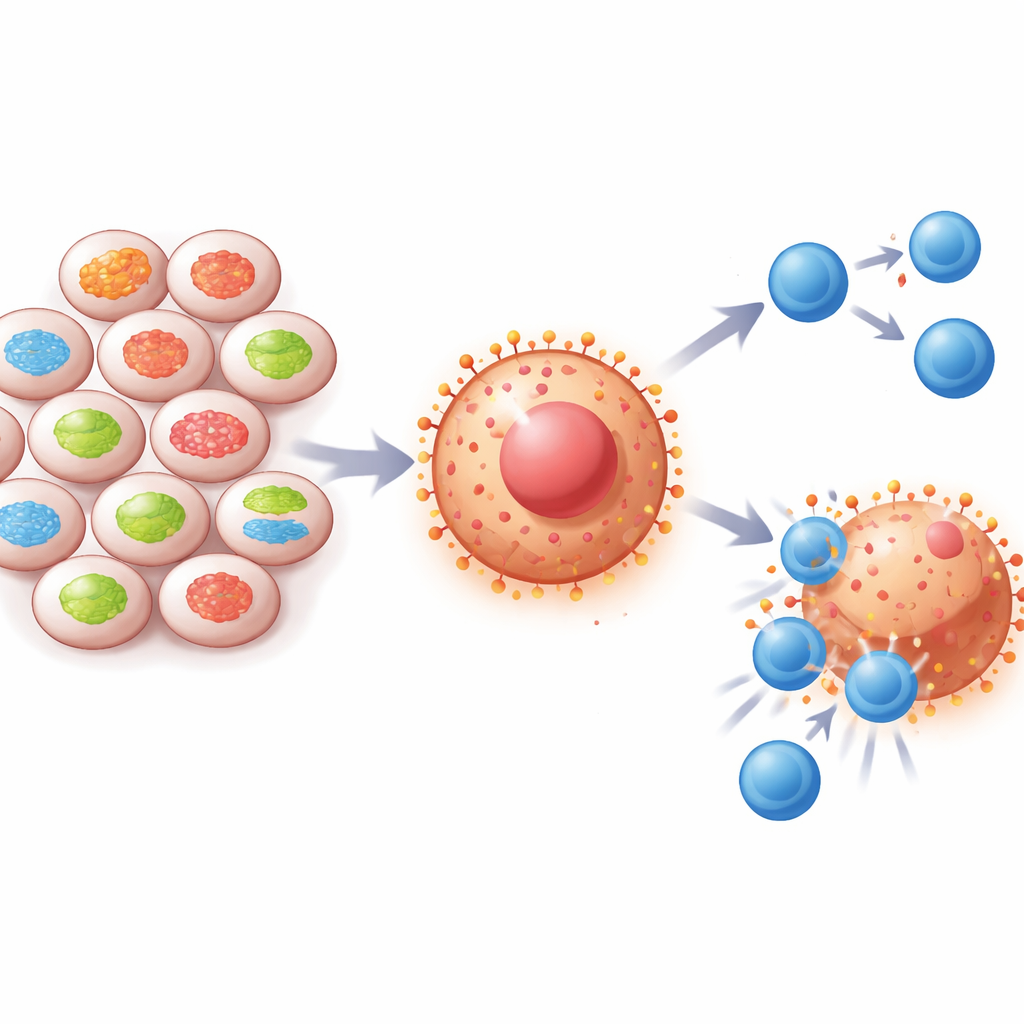
صلة خفية بين محطات طاقة الخلايا ودفاعات السرطان
داخل كل خلية، تعمل هياكل صغيرة تُسمى الميتوكوندريا كمحطات طاقة ومراكز اتصال. يساعد البروتين ميتوفيوزين-2 (MFN2) الميتوكوندريا على البقاء مترابطة وصحية. لاحظ الباحثون أن مستويات MFN2 غالبًا ما تكون منخفضة في سرطانات الرئة والكلى، وأن المرضى الذين لديهم MFN2 أقل يميلون إلى قصر عمر البقاء. في الوقت نفسه، تُظهر هذه الأورام كميات عالية من PD-L1، وهو إشارة «لا تهاجم» التي تُعطِّل الخلايا المناعية. من خلال فحص عينات المرضى وقواعد بيانات سرطانية كبيرة، وجد الفريق أنه عندما يكون MFN2 منخفضًا، غالبًا ما يكون PD-L1 مرتفعًا، ما يوحي بأن هذا البروتين الميتوكوندري يقيّد بطريقة ما قدرة الورم على الاختباء من الجهاز المناعي.
كيف تخفض الأورام MFN2 لتفادي الهجوم المناعي
لاختبار هذه الفكرة، عدّل العلماء مستويات MFN2 في أنواع عديدة من خلايا السرطان المزروعة في المختبر، بما في ذلك سرطانات الرئة والكلى والثدي. عندما قلّلوا MFN2، أنتجت الخلايا المزيد من PD-L1 وعرضته أكثر على سطحها، حتى تحت ظروف ضاغطة مثل نقص الأكسجين أو قلة المغذيات التي تحاكي داخل الورم. عندما أعادوا MFN2، انخفض PD-L1 مرة أخرى. في نماذج الفئران، نمت الأورام التي تفتقر إلى MFN2 بشكل أسرع واحتوت على عدد أقل من خلايا CD8 T المحاربة للسرطان بداخلها. أظهرت عينات سريرية من المرضى نمطًا مماثلًا: الأورام الغنية بـMFN2 احتوت على مزيد من خلايا CD8 T، وأظهر هؤلاء المرضى استجابة أفضل للأدوية التي تحجب PD-1 أو PD-L1.
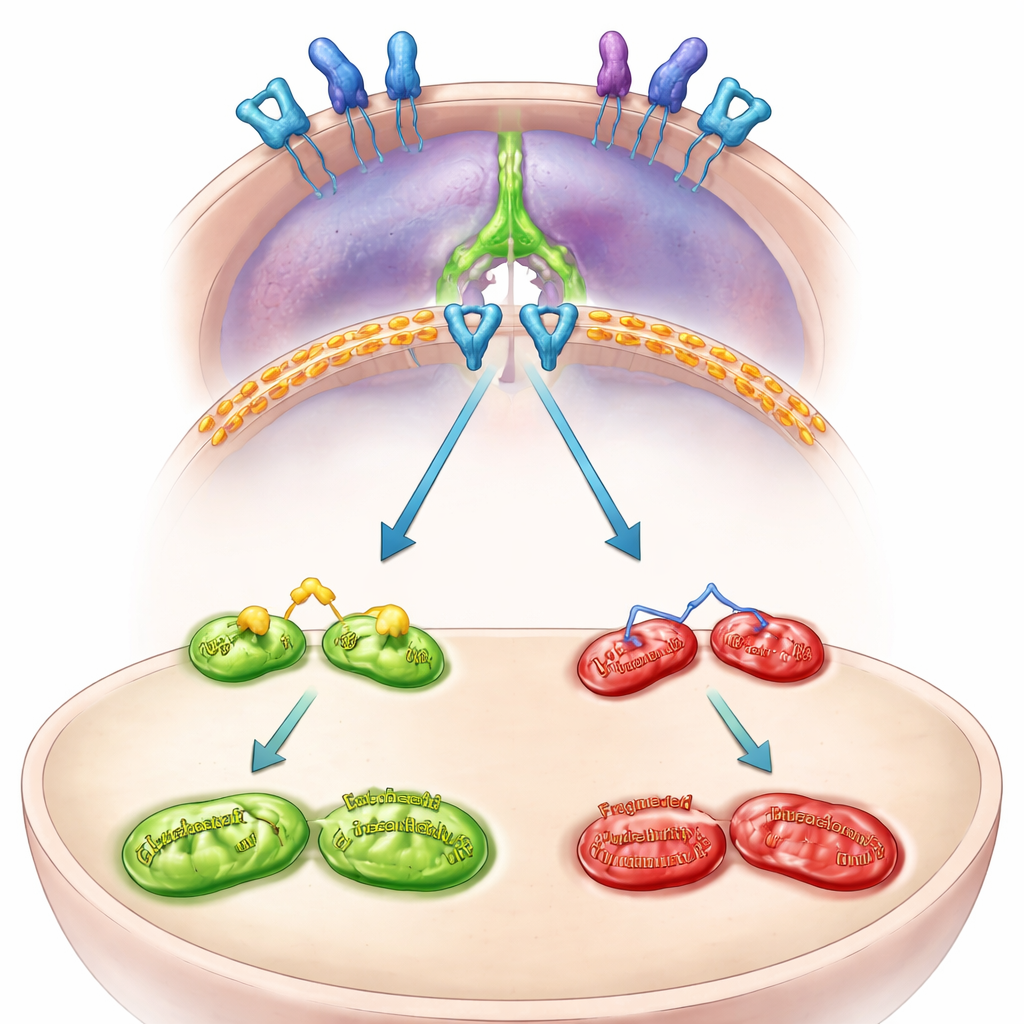
الأسلاك الداخلية: من الميتوكوندريا إلى هروب الجهاز المناعي
ثم رسم الفريق الخارطة الداخلية التي تربط MFN2 بـPD-L1. وجدوا أن MFN2 عادة ما يسيطر على إشارة نمو على سطح الخلية تُسمى EGFR. عندما يفقد MFN2، يصبح EGFR أكثر نشاطًا ويشغّل بروتينًا آخر، STAT3. تنتقل STAT3 المفعلة إلى نواة الخلية وتزيد التعليمات لصنع PD-L1. منع EGFR أو STAT3 في الخلايا الفاقدة لـMFN2 حال دون ارتفاع PD-L1 وقلّل من وجوده على سطح الخلية. في أعضية ثلاثية الأبعاد مشتقة من مرضى مزروعة كميني-أورام، أدت إسكات MFN2 مرة أخرى إلى تفعيل EGFR وSTAT3 ورفع مستوى PD-L1، مؤكدة أن هذا المسار يعمل في الأورام البشرية، وليس فقط في خطوط الخلايا.
تحويل الأورام الباردة إلى حارة مجددًا
نظرًا لأن PD-L1 يساعد الأورام على أن تصبح «باردة» أمام الهجوم المناعي، تساءل العلماء عما إذا كان إيقاف STAT3 يمكن أن يعكس هذا التأثير في الحيوانات. في الفئران التي تحمل أورامًا منخفضة MFN2، أدى العلاج بأدوية تحجب STAT3 إلى إبطاء نمو الأورام، واستعادة وجود خلايا CD8 T داخل الأورام، وزيادة الجزيئات الرسولية المناعية التي تساعد خلايا T على التجمع والبقاء نشطة. تقترح هذه التغيرات أنه حتى عندما تكون الأورام قد خفّضت MFN2 بالفعل، قد يكون من الممكن إعادة فتح الباب للهجوم المناعي عن طريق استهداف المسار الهابط EGFR–STAT3.
ماذا يعني هذا لعلاج السرطان مستقبلاً
بشكل عام، تكشف الدراسة أن MFN2، وهو بروتين معروف بدوره في المحافظة على صحة الميتوكوندريا، يعمل أيضًا كمكبح لمسار قوي يعزل الورم عن الجهاز المناعي داخل الخلايا السرطانية. عندما يفقد MFN2، يدفع EGFR وSTAT3 مستوى PD-L1 إلى الارتفاع، مما يساعد الأورام على الهروب من التعرف عليها وتدميرها بواسطة الخلايا المناعية. قد يساعد قياس MFN2 في الأورام على التنبؤ بمن سيستفيد من أدوية PD-1/PD-L1 الحالية، وقد يحول الجمع بين مثبطات EGFR أو STAT3 والعلاجات المناعية النقاطية الأورام المقاومة «الباردة» إلى أورام يمكن للجهاز المناعي التعرف عليها ومهاجمتها مرة أخرى.
الاستشهاد: Liu, Y., Wang, N., Li, Z. et al. Mitofusin-2 suppresses tumor immune escape through EGFR/STAT3-mediated PD-L1 transcription. Cell Death Dis 17, 364 (2026). https://doi.org/10.1038/s41419-026-08668-3
الكلمات المفتاحية: هروب الورم من الجهاز المناعي, تنظيم PD-L1, ديناميكيات الميتوكوندريا, إشارة EGFR STAT3, مقاومة العلاج المناعي للسرطان