Clear Sky Science · pl
Mitofusyna-2 hamuje ucieczkę nowotworu przed układem odpornościowym poprzez transkrypcję PD-L1 zależną od EGFR/STAT3
Dlaczego nasze komórki czasem ignorują raka
Immunoterapie przeciwnowotworowe zrewolucjonizowały leczenie wielu pacjentów, ale guzy często uczą się ukrywać na widoku. W badaniu tym przyjrzano się mało znanemu białku‑strażnikowi wewnątrz komórek nowotworowych, które pomaga decydować, czy komórki odpornościowe potrafią wykryć i zaatakować guz. Zrozumienie, jak działa ten wewnętrzny przełącznik, może wskazać nowe sposoby zwiększenia skuteczności istniejących immunoterapii i rozszerzenia ich działania na większą liczbę pacjentów.
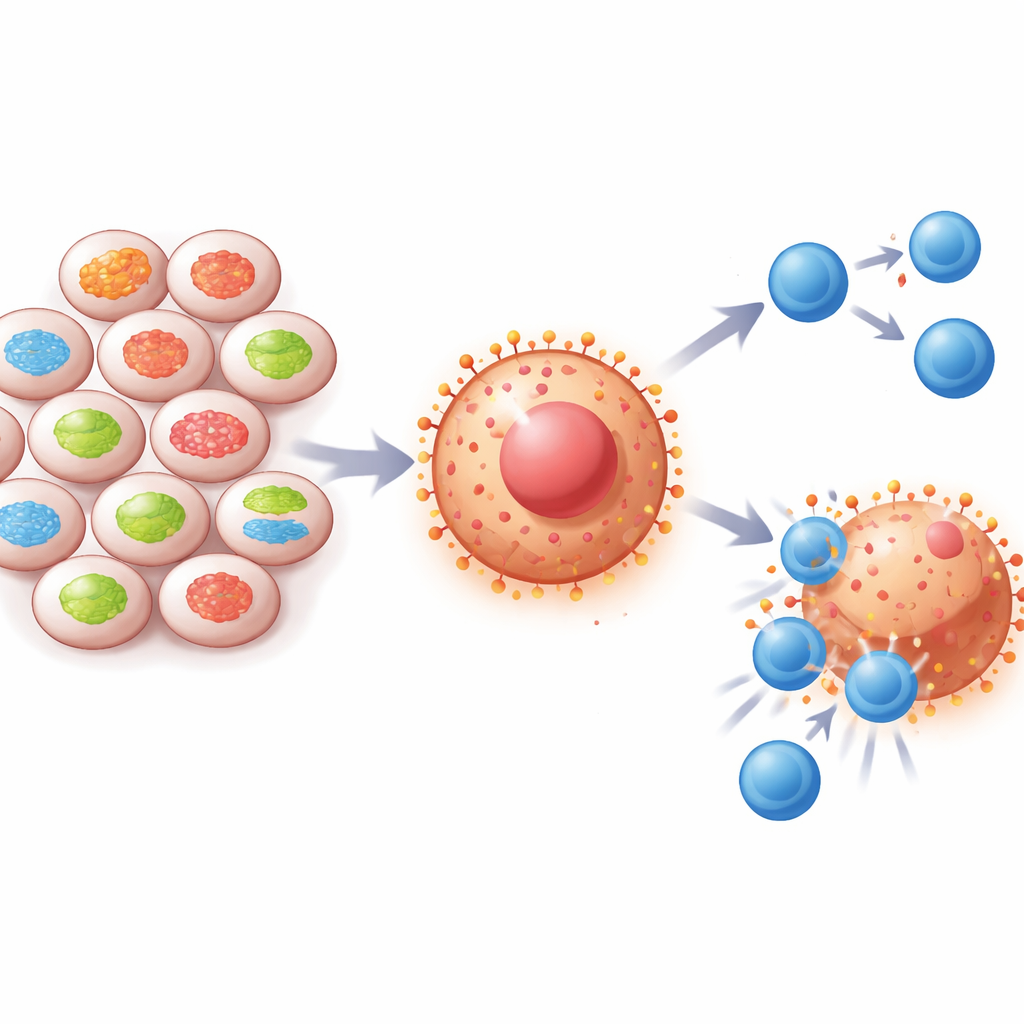
Ukryte powiązanie między centrami energetycznymi komórek a obroną nowotworu
Wewnątrz każdej komórki maleńkie struktury zwane mitochondriami pełnią rolę elektrowni i ośrodków komunikacyjnych. Białko Mitofusyna‑2 (MFN2) pomaga mitochondriom pozostawać połączonym i zdrowym. Badacze zauważyli, że poziomy MFN2 często są niskie w raku płuca i nerek, a pacjenci z mniejszą ilością MFN2 mają tendencję do krótszego przeżycia. Równocześnie te nowotwory wykazują duże ilości PD-L1, sygnału „nie atakować”, który wycisza komórki odpornościowe. Analiza próbek pacjentów i dużych baz danych nowotworowych wykazała, że gdy MFN2 jest niski, PD-L1 zwykle jest wysoki, co sugeruje, że to białko mitochondrialne w jakiś sposób ogranicza zdolność guza do ukrywania się przed układem odpornościowym.
Jak guzy obniżają MFN2, by uniknąć ataku immunologicznego
Aby sprawdzić ten pomysł, naukowcy zmieniali poziomy MFN2 w różnych typach komórek nowotworowych hodowanych w laboratorium, w tym raka płuca, nerek i piersi. Gdy obniżono MFN2, komórki produkowały więcej PD-L1 i wykazywały go więcej na swojej powierzchni, nawet w warunkach stresowych, takich jak niskie stężenie tlenu czy ubogie substancje odżywcze, które naśladują wnętrze guza. Przywrócenie MFN2 powodowało spadek PD-L1. W modelach mysich guzy pozbawione MFN2 rosły szybciej i zawierały mniej komórek CD8 walczących z rakiem. Próbki kliniczne od pacjentów wykazywały podobny wzorzec: nowotwory bogatsze w MFN2 zawierały więcej komórek CD8, a tacy pacjenci lepiej reagowali na leki blokujące PD-1 lub PD-L1.
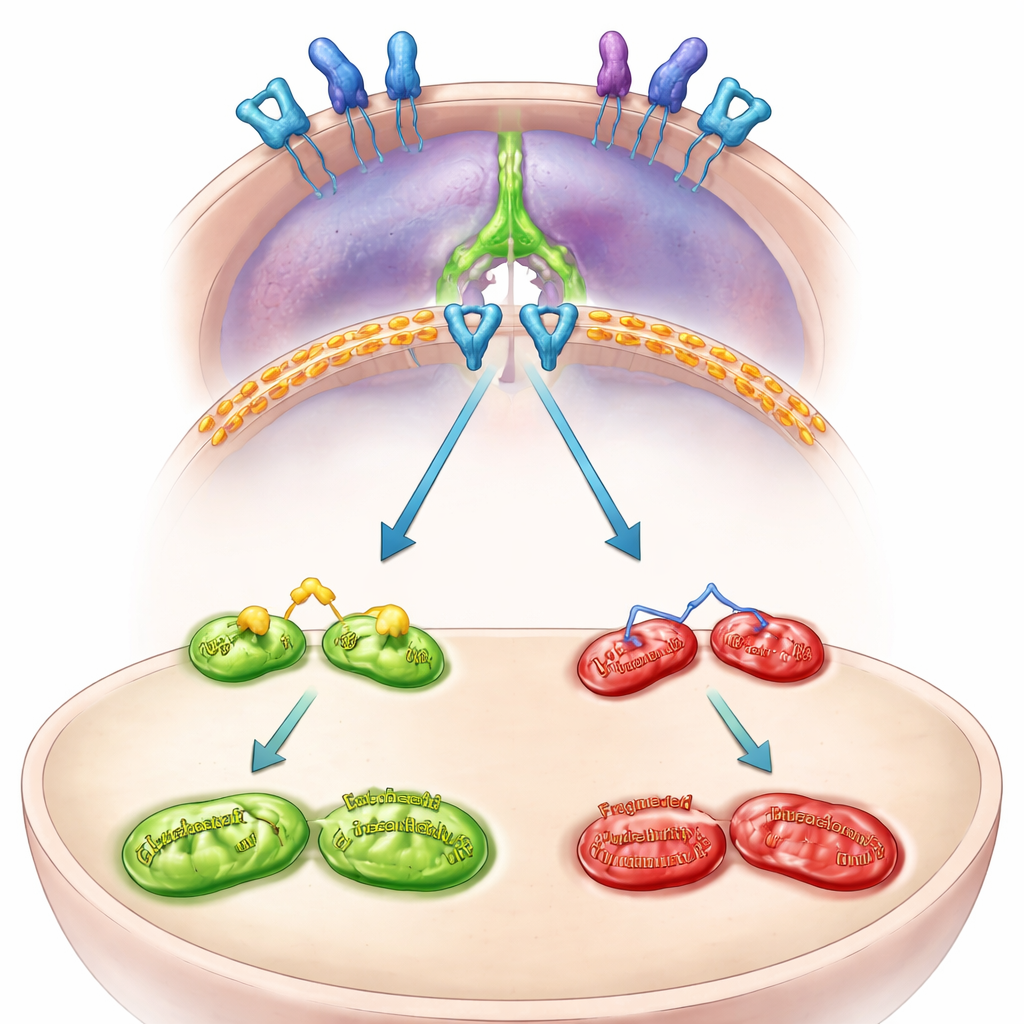
Wewnętrzne okablowanie: od mitochondriów do ucieczki przed układem odpornościowym
Zespół następnie zmapował wewnętrzne powiązania łączące MFN2 z PD-L1. Odkryli, że MFN2 zwykle utrzymuje w ryzach sygnał wzrostowy na powierzchni komórki, zwany EGFR. Kiedy MFN2 zostaje utracona, EGFR staje się bardziej aktywny i uruchamia kolejne białko, STAT3. Aktywowany STAT3 przemieszczając się do jądra komórkowego zwiększa instrukcje do wytwarzania PD-L1. Zablokowanie EGFR lub STAT3 w komórkach pozbawionych MFN2 zapobiegało wzrostowi PD-L1 i zmniejszało jego ekspresję na powierzchni komórki. W mini‑guzach pochodzących od pacjentów hodowanych jako trójwymiarowe organoidy wyciszenie MFN2 ponownie aktywowało EGFR i STAT3 oraz podnosiło poziomy PD-L1, co potwierdza, że ten szlak działa w ludzkich nowotworach, a nie tylko w liniach komórkowych.
Ogrzanie „zimnych” guzów
Ponieważ PD-L1 pomaga guzom stać się „zimnymi” względem ataku immunologicznego, naukowcy sprawdzili, czy wyłączenie STAT3 może odwrócić ten efekt u zwierząt. U myszy z guzami o niskim poziomie MFN2 leczenie lekami blokującymi STAT3 spowolniło wzrost nowotworów, przywróciło obecność komórek CD8 wewnątrz guzów i zwiększyło wydzielanie cząsteczek sygnałowych układu odpornościowego, które pomagają gromadzić się i utrzymywać aktywność limfocytów T. Zmiany te sugerują, że nawet gdy guzy już obniżyły MFN2, wciąż może być możliwe ponowne otwarcie drogi do ataku immunologicznego poprzez celowanie w zstępujący szlak EGFR–STAT3.
Co to oznacza dla przyszłego leczenia raka
Podsumowując, badanie ujawnia, że MFN2, białko najbardziej znane z utrzymania zdrowia mitochondriów, działa także jako hamulec potężnej ścieżki osłaniającej nowotwór przed układem odpornościowym. Gdy MFN2 zanika, EGFR i STAT3 podnoszą poziom PD-L1, co pomaga guzom unikać rozpoznania i zniszczenia przez komórki odpornościowe. Oznaczanie poziomu MFN2 w guzach mogłoby pomóc przewidzieć, kto skorzysta na obecnych lekach przeciw PD-1/PD-L1, a łączenie inhibitorów EGFR lub STAT3 z terapiami blokującymi punkty kontrolne może przemienić oporne, „zimne” guzy w takie, które układ odpornościowy znów będzie potrafił rozpoznać i zaatakować.
Cytowanie: Liu, Y., Wang, N., Li, Z. et al. Mitofusin-2 suppresses tumor immune escape through EGFR/STAT3-mediated PD-L1 transcription. Cell Death Dis 17, 364 (2026). https://doi.org/10.1038/s41419-026-08668-3
Słowa kluczowe: ucieczka nowotworu przed układem odpornościowym, regulacja PD-L1, dynamika mitochondrialna, szlak sygnalizacyjny EGFR STAT3, oporność na immunoterapię przeciwnowotworową