Clear Sky Science · ru
Митофузин‑2 подавляет иммунное уклонение опухоли через транскрипцию PD‑L1, опосредованную EGFR/STAT3
Почему наши клетки иногда не распознают рак
Лечение рака, использующее иммунную систему, изменило подход к терапии многих пациентов, однако опухоли часто находят способы прятаться на виду. В этом исследовании изучается малоизвестный белок‑регулятор внутри раковых клеток, который во многом решает, смогут ли иммунные клетки заметить и атаковать опухоль. Понимание работы этого внутреннего переключателя может указать пути для повышения эффективности существующих иммунотерапий и расширения числа пациентов, которые от них выигрывают.
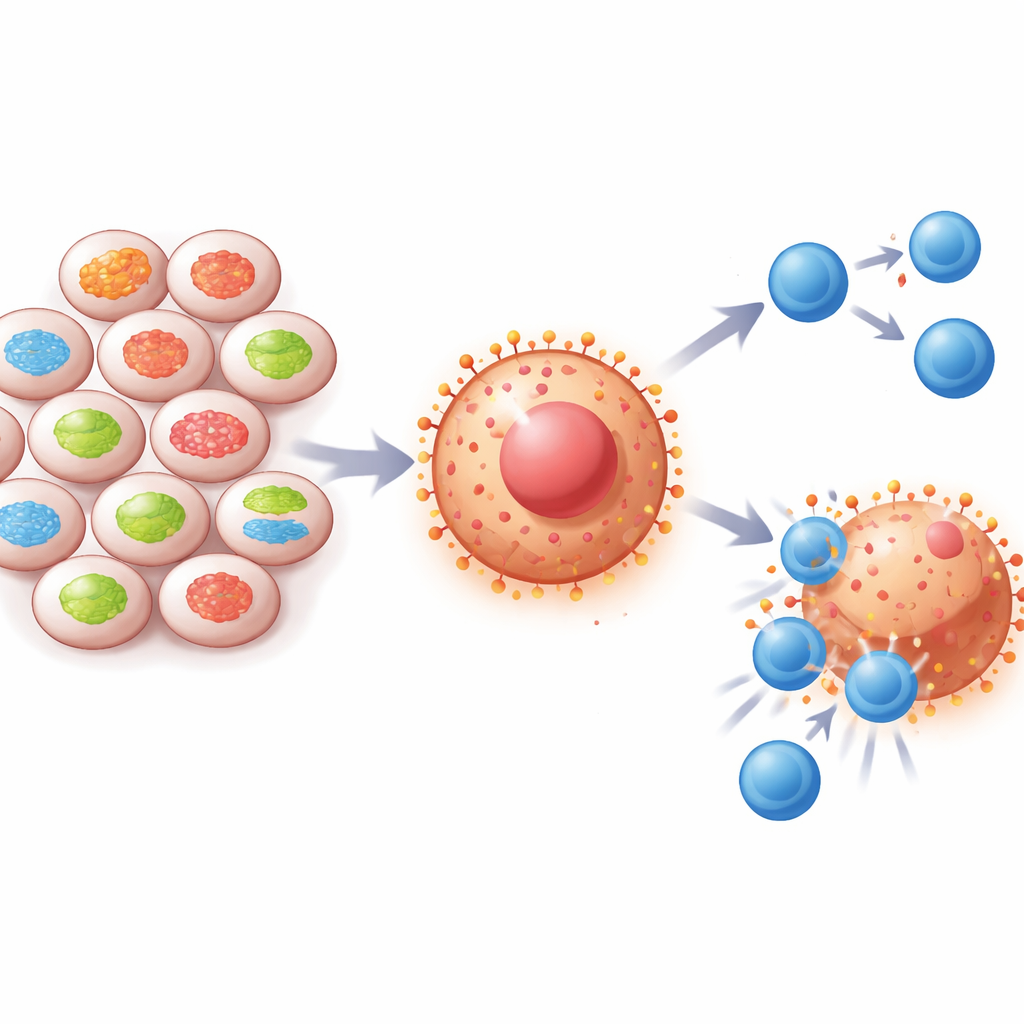
Скрытая связь между «электростанциями» клетки и механизмами защиты опухоли
В каждой клетке крошечные структуры — митохондрии — выступают в роли электростанций и центров коммуникации. Белок митофузин‑2 (MFN2) помогает митохондриям оставаться связанными и функционировать нормально. Исследователи заметили, что уровни MFN2 часто снижены при раке легких и почек, а у пациентов с низким содержанием MFN2 выживаемость, как правило, короче. При этом в этих опухолях обнаруживается много PD‑L1 — сигнала «не атаковать», который подавляет иммунные клетки. Анализ образцов пациентов и больших онкогенных баз данных показал, что при низком MFN2 PD‑L1 обычно высок, что наводит на мысль: этот митохондриальный белок каким‑то образом сдерживает способность опухоли прятаться от иммунитета.
Как опухоли понижают MFN2, чтобы уйти от иммунной атаки
Чтобы проверить эту гипотезу, ученые изменяли уровень MFN2 во многих типах выращиваемых в лаборатории раковых клеток, включая клетки рака легких, почки и молочной железы. При снижении MFN2 клетки стали синтезировать больше PD‑L1 и демонстрировать его в большей степени на поверхности, даже в стрессовых условиях — низкого содержания кислорода или плохого питания, имитирующих внутриопухолевую среду. При восстановлении MFN2 уровень PD‑L1 возвращался к низким значениям. В модельных экспериментах на мышах опухоли с дефицитом MFN2 росли быстрее и содержали меньше CD8+ Т‑клеток. Клинические образцы пациентов показали аналогичный паттерн: опухоли, богатые MFN2, содержали больше CD8+ Т‑клеток, а такие пациенты лучше отвечали на препараты, блокирующие PD‑1 или PD‑L1.
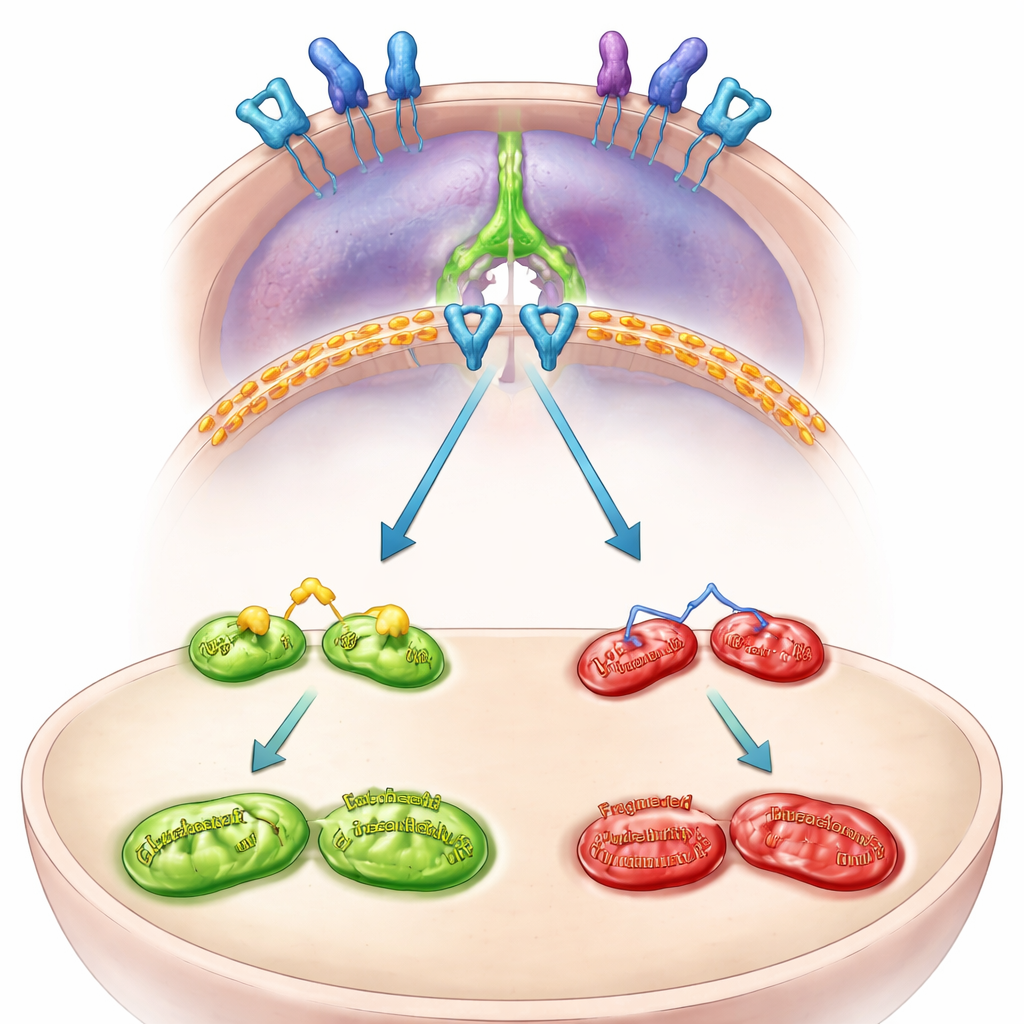
Внутренняя схема: от митохондрий к иммунному уклонению
Далее команда проследила внутрирегуляторную схему, связывающую MFN2 с PD‑L1. Они обнаружили, что MFN2 в норме сдерживает активацию поверхностного сигнала роста EGFR. При потере MFN2 EGFR становится более активным и запускает другую молекулу — STAT3. Активированный STAT3 перемещается в ядро клетки и усиливает транскрипцию PD‑L1. Блокирование EGFR или STAT3 в клетках с дефицитом MFN2 препятствовало нарастанию PD‑L1 и снижало его экспрессию на поверхности клетки. В органоидах — мини‑опухолях, полученных от пациентов и выращенных в трёхмерной культуре — выключение MFN2 также активировало EGFR и STAT3 и повышало PD‑L1, подтверждая, что этот путь работает в человеческих опухолях, а не только в линиях клеток.
Превращение «холодных» опухолей в «горячие»
Поскольку PD‑L1 делает опухоли «холодными» для иммунной атаки, ученые проверили, можно ли отменить этот эффект путем подавления STAT3 в экспериментах на животных. У мышей с опухолями, характеризующимися низким MFN2, лечение препаратами‑ингибиторами STAT3 замедляло рост опухолей, восстанавливало присутствие CD8+ Т‑клеток в опухолях и повышало выработку сигнальных молекул, привлекающих и поддерживающих Т‑клетки. Эти изменения указывают на то, что даже при уже пониженном MFN2 возможно вновь открыть доступ для иммунной атаки, нацелившись на нисходящий путь EGFR–STAT3.
Что это значит для будущего лечения рака
В целом исследование показывает, что MFN2, белок, прежде всего известный поддержанием здоровья митохондрий, также действует как тормоз мощного пути, защищающего опухоль от иммунной системы. При потере MFN2 EGFR и STAT3 повышают экспрессию PD‑L1, помогая опухолям избегать распознавания и уничтожения иммунными клетками. Оценка уровня MFN2 в опухолях может помочь предсказать, кто получит пользу от имеющихся препаратов против PD‑1/PD‑L1, а сочетание ингибиторов EGFR или STAT3 с чекпойнт‑терапией может превратить резистентные «холодные» опухоли в те, которые иммунная система снова сможет распознать и атаковать.
Цитирование: Liu, Y., Wang, N., Li, Z. et al. Mitofusin-2 suppresses tumor immune escape through EGFR/STAT3-mediated PD-L1 transcription. Cell Death Dis 17, 364 (2026). https://doi.org/10.1038/s41419-026-08668-3
Ключевые слова: иммунное уклонение опухоли, регуляция PD‑L1, динамика митохондрий, сигнaling EGFR STAT3, резистентность к иммунотерапии рака