Clear Sky Science · zh
使用人胚胎干细胞心肌细胞和生物工程化3D室性心脏组织条研究PKD2缺陷相关心肌病
为什么肾病与心脏有关
患有常染色体显性多囊肾病(ADPKD)的人通常被视为肾脏患者,但许多人也会出现严重的心脏问题。临床上长期观察到这些患者常有心室壁增厚、收缩功能减弱和心律失常,但导致肾囊肿的基因缺陷如何直接损伤心肌仍不清楚。本研究利用最先进的体外人源心脏组织,提出一个简单而重要的问题:肾相关蛋白多囊蛋白-2(polycystin-2)的缺陷如何削弱心脏,这种弱化能否至少部分被逆转?
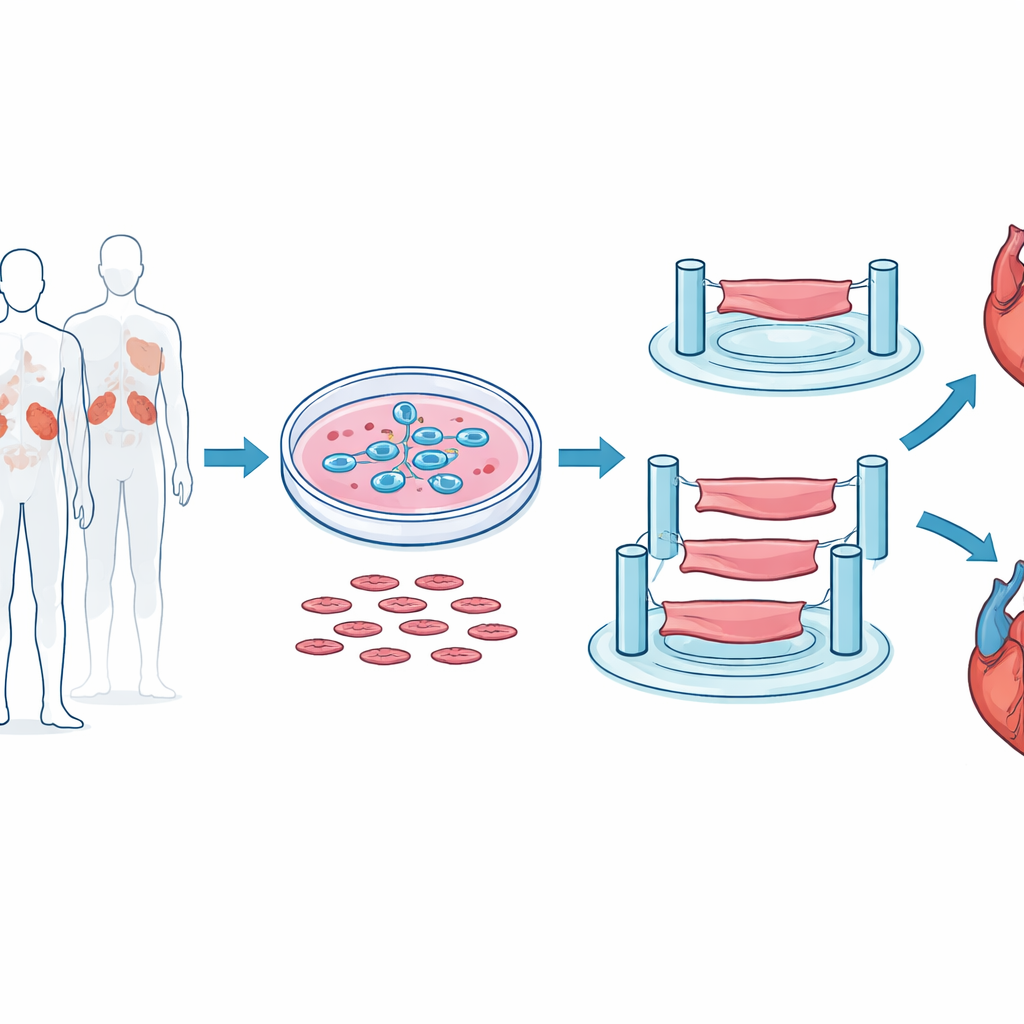
在实验室构建迷你心脏条
为了尽可能接近真实的人类心脏功能,研究者没有依赖小鼠心脏或平面细胞层。相反,他们从人胚胎干细胞入手,精确诱导其分化为跳动的心肌细胞。将这些细胞与支持性细胞和凝胶样支架混合并成型为微小的三维室性组织条,每条仅几毫米长,但能在柔性支柱之间有节律地收缩。该体系使团队能够测量组织条的牵引力、收缩与舒张速度,以及对电刺激的反应,类似对心肌进行微型负荷测试。
缺失多囊蛋白-2时发生了什么
团队随后使用基因沉默工具降低这些心肌细胞中多囊蛋白-2的量,以模拟许多ADPKD患者的缺陷。多囊蛋白-2被敲低后,组织条仍然有节律跳动,但收缩力明显减弱,收缩与舒张变得迟缓。这种功能减弱在两个独立的干细胞系和不同的沉默方法中均出现,进一步支持多囊蛋白-2对人心肌功能的重要性。值得注意的是,组织的整体微结构——其基本排列和内部支架——看起来正常,表明问题更可能出在细胞功能而非明显的结构损伤或紊乱。
钙处理失衡与细胞应激
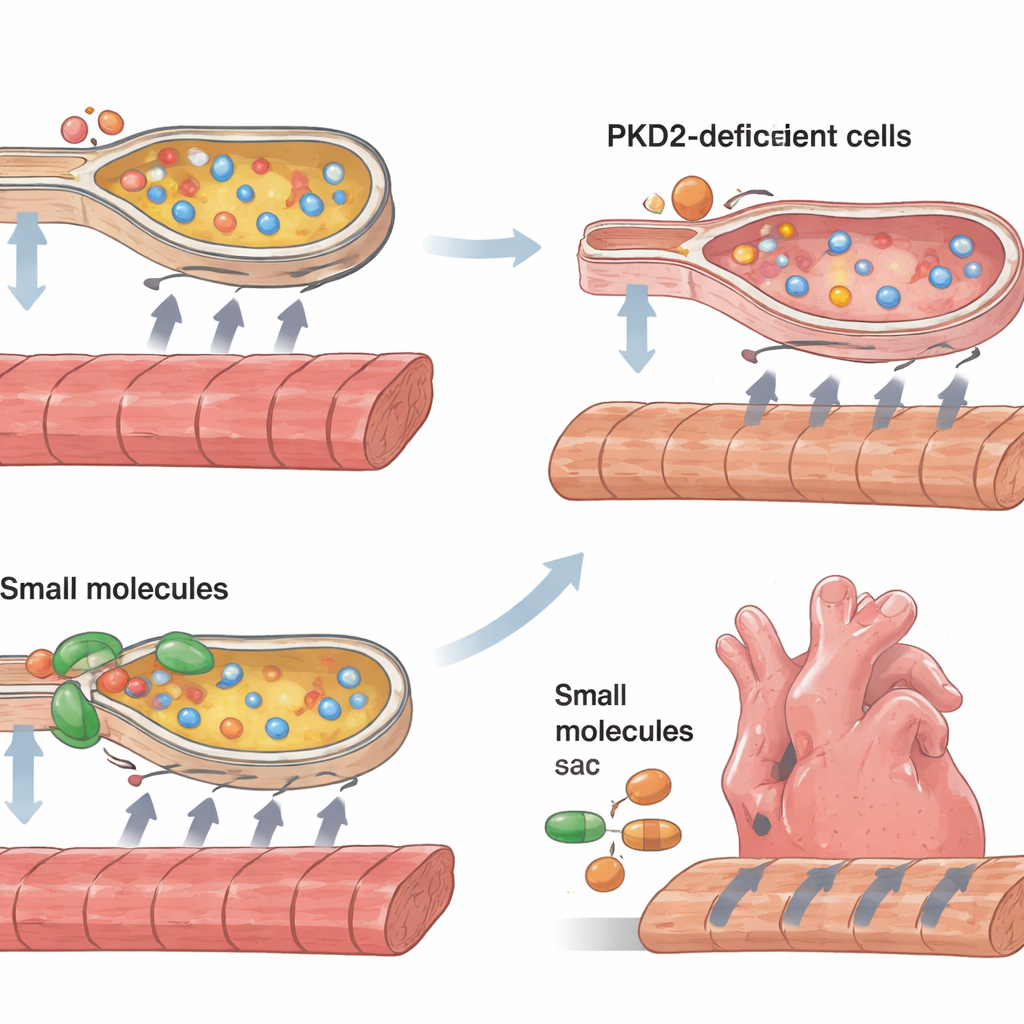
心肌细胞依赖精确的钙处理:钙离子涌入细胞触发收缩,随后被泵回细胞内储存结构以实现舒张并为下一次收缩做准备。在缺乏足够多囊蛋白-2的细胞中,每次收缩时钙信号的峰值变小且清除更慢。与内质网重叠的内部储存囊室似乎储钙量减少且补充速度变慢。与此同时,内质网应激的分子标志明显上升,更多细胞出现程序性死亡标记和与心肌病相关的细胞肥大特征。一个关键的钙泵SERCA2及其调节蛋白磷脂酸苷蛋白(phospholamban)活性均降低,为缺失蛋白与受损钙循环之间提供了具体的机械性联系。
尝试拯救功能衰退的迷你心脏
基于这一机制图景,研究者尝试修复功能减弱的组织条。他们使用两种小分子——4-苯基丁酸和牛磺熊去氧胆酸(tauroursodeoxycholic acid),这两者作为化学分子伴侣可改善蛋白折叠并已知可缓解内质网应激。他们还应用了一种名为CDN1163的化合物以增强SERCA泵活性。所有三种处理都改善了组织条的收缩强度并加速了收缩与舒张,在缺乏多囊蛋白-2的组织条中改善尤为明显。修复是部分的——这些干预并未使组织完全恢复正常——但显示出缓解细胞应激和恢复钙泵功能可以显著改善该模型中病变人心肌的表现。
这对患者意味着什么
这项工作表明,多囊蛋白-2的缺陷可以直接通过扰乱钙处理并使细胞内部质量控制系统超负荷,从而削弱人心肌的功能——即便在没有肾功能衰竭或高血压的背景下也是如此。通过构建并测试生物工程化的人源心脏组织条,研究将一个遗传缺陷与一系列具体事件连接起来:多囊蛋白-2减少、钙泵功能减弱、细胞内应激上升,最终导致收缩迟缓与力弱。同样重要的是,该平台还表明已知能降低细胞应激或增强钙泵的药物可以部分恢复功能。尽管在将这些策略应用于患者之前仍需大量工作,但这些发现为多囊肾病隐匿性心脏并发症指明了切实可行、可验证的治疗方向。
引用: Li, J., Peng, W., Kwok, M. et al. Investigating PKD2 deficiency-associated cardiomyopathies using hESC-cardiomyocytes and bioengineered 3D ventricular cardiac tissue strips. Cell Death Dis 17, 368 (2026). https://doi.org/10.1038/s41419-026-08639-8
关键词: 多囊肾病, 心肌病, 钙信号传导, 干细胞心脏模型, 内质网应激