Clear Sky Science · ar
التحقيق في اعتلالات القلب المرتبطة بنقص PKD2 باستخدام خلايا قلبية بشرية مشتقة من الخلايا الجذعية البشرية ونُسُج بطينية قلبية ثلاثية الأبعاد مُهندَسة حيويًّا
لماذا تهم أمراض الكلى القلب
غالبًا ما يُنظر إلى الأشخاص المصابين بمرض الكلى المتعدد الكيسات السائد وراثيًا (ADPKD) على أنهم مرضى كلى، لكن العديد منهم يطوّر مشاكل قلبية خطيرة أيضًا. لوحظ منذ زمن زيادة سماكة جدران القلب وضعف الضخ واضطرابات النظم لدى هؤلاء المرضى، ومع ذلك ظل الرابط المباشر بين الطفرات الجينية المسببة لأكياس الكلى وتضرّر عضلة القلب غير واضح. تستخدم هذه الدراسة أنسجة قلب بشرية مزروعة في المختبر متقدمة لطرح سؤال بسيط لكنه مهم: كيف يضعف عيب في بروتين مرتبط بالكلى يُسمى بوليسيستن-2 القلب، وهل يمكن عكس ذلك جزئيًا؟
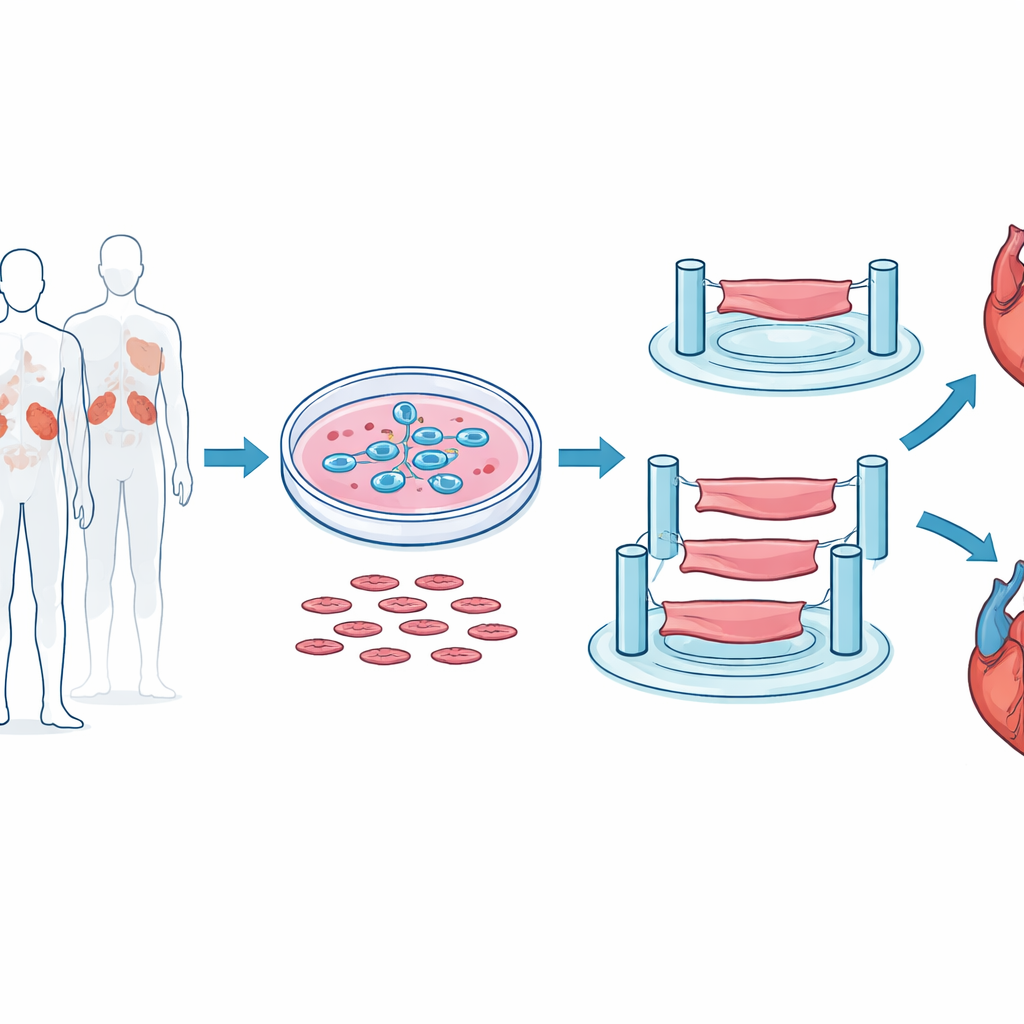
بناء شرائط قلبية صغيرة في المختبر
للاقتراب قدر الإمكان من سلوك القلب البشري الحقيقي، لم يعتمد الباحثون على قلوب الفئران أو طبقات خلوية مسطحة. بدلاً من ذلك بدأوا بالخلايا الجذعية الجنينية البشرية ووجهوها بعناية لتتحول إلى خلايا عضلية قلبية نابضة. ثم خلطت هذه الخلايا بخلايا داعمة ومواد هلامية شبه هيكلية وصُبّت لتشكيل شرائط ثلاثية الأبعاد صغيرة من النسيج البطيني، طول كل منها بضعة مليمترات فقط لكنها قادرة على الانقباض إيقاعيًا بين أعمدة مرنة. أتاح هذا الإعداد للفريق قياس قوة الشد التي تولّدها الشرائط، وسرعة انقباضها واسترخائها، واستجابتها للتحفيز الكهربائي، تمامًا مثل اختبار تدريب مصغر لعضلة القلب.
ماذا يحدث عند فقدان بوليسيستن-2
قلّص الفريق بعد ذلك كمية بوليسيستن-2 في هذه الخلايا القلبية باستخدام أدوات جينية تُكتم جين PKD2، مقلّدين بذلك العيب الموجود في العديد من مرضى ADPKD. عندما تم خفض بوليسيستن-2، استمرت الشرائط النسيجية في النبض، لكنها كانت تضغط بقوة أقل بكثير وأصبحت تقلّصاتها واسترخاءاتها أبطأ. ظهر هذا الضعف في سطرين مستقلين من الخلايا الجذعية وبطرق كتم مختلفة، مما يعزّز فرضية أهمية بوليسيستن-2 لأداء عضلة القلب البشرية. والأهم أن البنية الدقيقة العامة للنسيج—تنظيمه الأساسي والهياكل الداخلية—بدت طبيعية، مما يشير إلى مشكلة في وظيفة الخلايا بدلاً من تلف أو اضطراب مرئي كبير.
سوء إدارة الكالسيوم وإجهاد الخلية
تعتمد الخلايا القلبية على معالجة دقيقة للكالسيوم، الذي يغمر الخلية لتحفيز الانقباض ثم يتم ضخه مرة أخرى إلى مخازن داخلية لكي تسترخي الخلية وتستعد للنبضة التالية. في الخلايا التي تفتقر إلى كمية كافية من بوليسيستن-2، كانت دفعات الكالسيوم خلال كل نبضة أصغر واستغرق التخلص منها وقتًا أطول. بدت الأكياس الداخلية المخزنة، التي تتداخل مع بنية تسمى الشبكة الإندوبلازمية، أنها تحتوي على كمية أقل من الكالسيوم وتتعافى ببطء. وفي الوقت نفسه ارتفعت علامات جزيئية لإجهاد الشبكة الإندوبلازمية بشكل حاد، وأظهرت مزيد من الخلايا علامات الموت المبرمج وميزات التضخّم المرتبطة باعتلال عضلة القلب. كان مضخٌّ كالسيوم رئيسي، SERCA2، وشريكه المنظم فوسفولامبان أقل نشاطًا، مما يوفّر رابطًا ميكانيكيًا ملموسًا بين البروتين المفقود واضطراب دورة الكالسيوم.
اختبار طرق لمساعدة القلوب المصغّرة الفاشلة
مسلّحين بهذه الصورة الآلية، جرّب الباحثون إنقاذ الشرائط النسيجية الضعيفة. استخدموا جزيئين صغيرين، 4-فينيلبيوتيرات وحمض الطاورورسوديوكسيكوليك، اللذين يعملان كمساعدين كيميائيين لطي البروتين ومعروفين بتخفيف إجهاد الشبكة الإندوبلازمية. كما طبّقوا مركبًا يُدعى CDN1163 يعزّز نشاط مضخّة SERCA. حسّنت العلاجات الثلاثة قوة الانقباض وسرّعت كلًا من الانقباض والارتخاء في الشرائط، مع مكاسب واضحة بشكل خاص في الشرائط التي تفتقر إلى بوليسيستن-2. كان الاسترداد جزئيًا فقط—فلم تُعد الأنْسجة طبيعية بالكامل—لكنها أظهرت أن تخفيف إجهاد الخلية واستعادة ضخ الكالسيوم يمكن أن يحسّن أداء عضلة القلب البشرية المريضة في هذا النموذج بشكل ملموس.
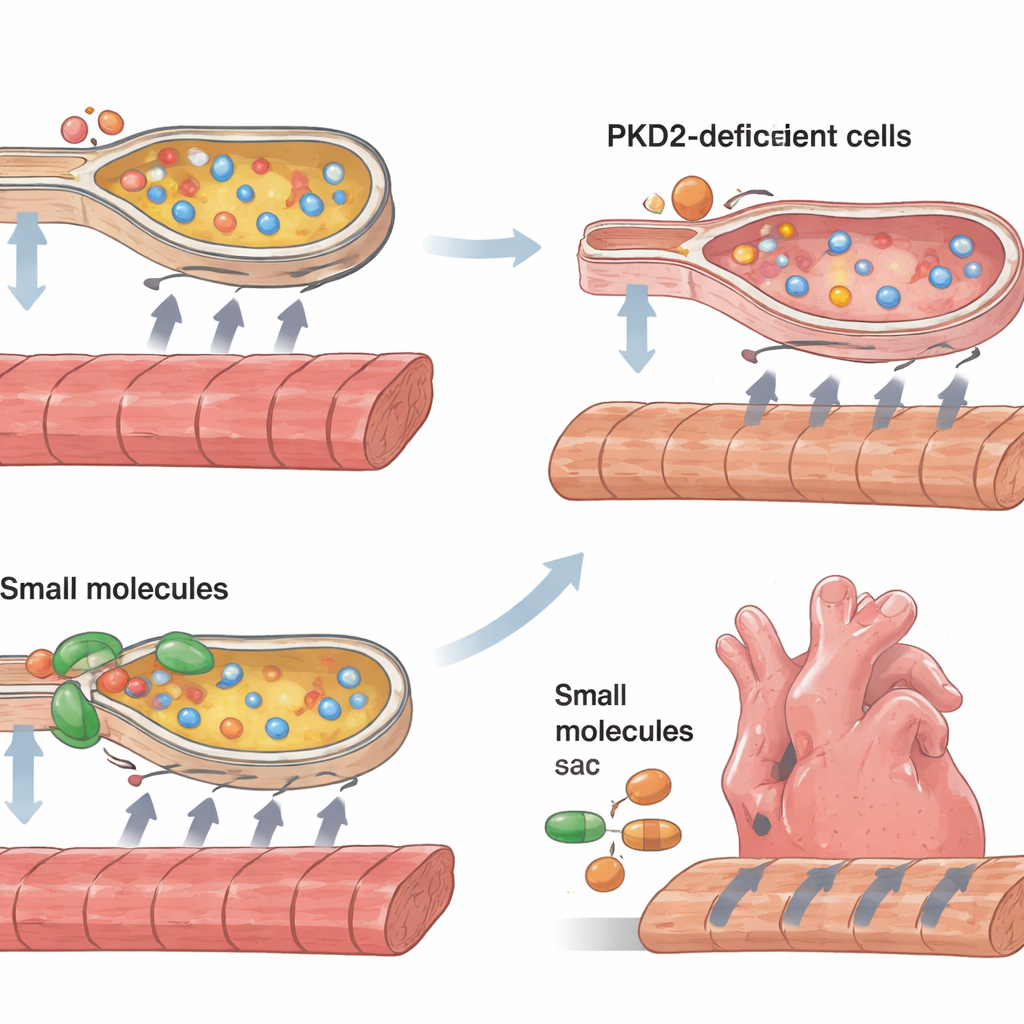
ماذا يعني هذا للمرضى
تُبيّن هذه الدراسة أن العيوب في بوليسيستن-2 يمكن أن تُضعِف عضلة القلب البشرية مباشرة عن طريق اضطراب معالجة الكالسيوم وإرهاق نظام الرقابة الداخلية على جودة البروتين، حتى خارج سياق فشل الكلى أو ارتفاع ضغط الدم. من خلال بناء واختبار شرائط قلبية بشرية مُهندَسة حيويًّا، تربط الدراسة العيب الوراثي بسلسلة محددة من الأحداث: انخفاض بوليسيستن-2، ضعف مضخّات الكالسيوم، ازدياد الإجهاد الداخلي، وفي النهاية تقلّصات أبطأ وأضعف. وبقدر أهميته، يبيّن نفس الأسلوب أن أدوية معروفة تقلّل إجهاد الخلايا أو تعزّز ضخ الكالسيوم يمكن أن تستعيد الوظيفة جزئيًا. وبينما لا يزال الكثير من العمل مطلوبًا قبل تجربة هذه الاستراتيجيات على البشر، تشير النتائج إلى علاجات واقعية قابلة للاختبار لمضاعفات القلب الخفيّة المرتبطة بمرض الكلى المتعدد الكيسات.
الاستشهاد: Li, J., Peng, W., Kwok, M. et al. Investigating PKD2 deficiency-associated cardiomyopathies using hESC-cardiomyocytes and bioengineered 3D ventricular cardiac tissue strips. Cell Death Dis 17, 368 (2026). https://doi.org/10.1038/s41419-026-08639-8
الكلمات المفتاحية: مرض الكلى المتعدد الكيسات, اعتلال عضلة القلب, إشارات الكالسيوم, نماذج القلب من الخلايا الجذعية, إجهاد الشبكة الإندوبلازمية