Clear Sky Science · it
Investigazione delle cardiomiopatie associate alla carenza di PKD2 usando cardiomiociti da hESC e strisce di tessuto cardiaco ventricolare 3D bioingegnerizzate
Perché la malattia renale conta per il cuore
Le persone con malattia policistica renale autosomica dominante (ADPKD) sono di solito considerate pazienti renali, ma molte sviluppano anche gravi problemi cardiaci. I medici hanno a lungo osservato ispessimento delle pareti cardiache, funzione contrattile ridotta e aritmie in questi pazienti, tuttavia il legame diretto tra i geni difettosi che causano le cisti renali e il danno al muscolo cardiaco è rimasto poco chiaro. Questo studio utilizza tessuti cardiaci umani coltivati in laboratorio all’avanguardia per porre una domanda semplice ma importante: come un difetto in una proteina legata al rene, chiamata policistina-2, indebolisce il cuore, e tale debolezza può essere almeno in parte invertita?
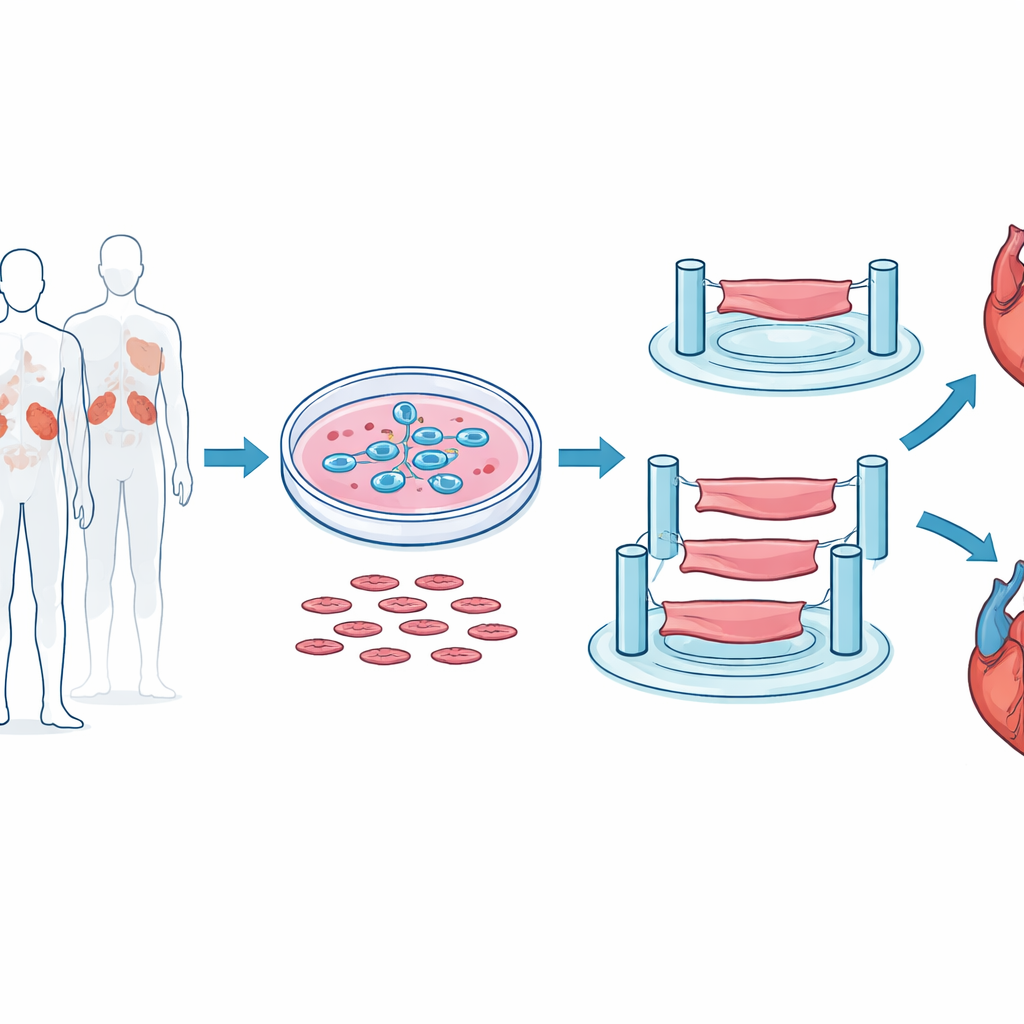
Costruire strisce di mini-cuore in laboratorio
Per avvicinarsi il più possibile al comportamento del cuore umano reale, i ricercatori non si sono affidati a cuori di topo o a monostrati cellulari. Invece hanno iniziato da cellule staminali embrionali umane e le hanno guidate con cura a diventare cellule muscolari cardiache battenti. Queste cellule sono state poi miscelate con cellule di supporto e impalcature gellose e modellate in piccole strisce tridimensionali di tessuto ventricolare, lunghe solo pochi millimetri ma capaci di contrarsi ritmicamente tra perni flessibili. Questo allestimento ha permesso al team di misurare quanto intensamente le strisce si contraevano, quanto rapidamente si contraevano e si rilassavano e come rispondevano alla stimolazione elettrica, molto simile a un test d’allenamento in miniatura per il muscolo cardiaco.
Cosa succede quando la policistina-2 viene persa
Il gruppo ha quindi ridotto la quantità di policistina-2 in queste cellule cardiache usando strumenti genetici che silenziano il gene PKD2, imitando il difetto osservato in molti pazienti con ADPKD. Quando la policistina-2 è stata abbattuta, le strisce di tessuto continuavano a battere, ma si contraevano con molta meno forza e le loro contrazioni e rilassamenti sono diventati lenti. Questa debolezza è apparsa in due linee indipendenti di cellule staminali e con diversi metodi di silenziamento, rafforzando l’ipotesi che la policistina-2 sia veramente importante per le prestazioni del muscolo cardiaco umano. È importante notare che la microstruttura complessiva del tessuto — la sua organizzazione di base e l’impalcatura interna — appariva normale, indicando un problema di funzione cellulare piuttosto che un danno grossolano o disorganizzazione.
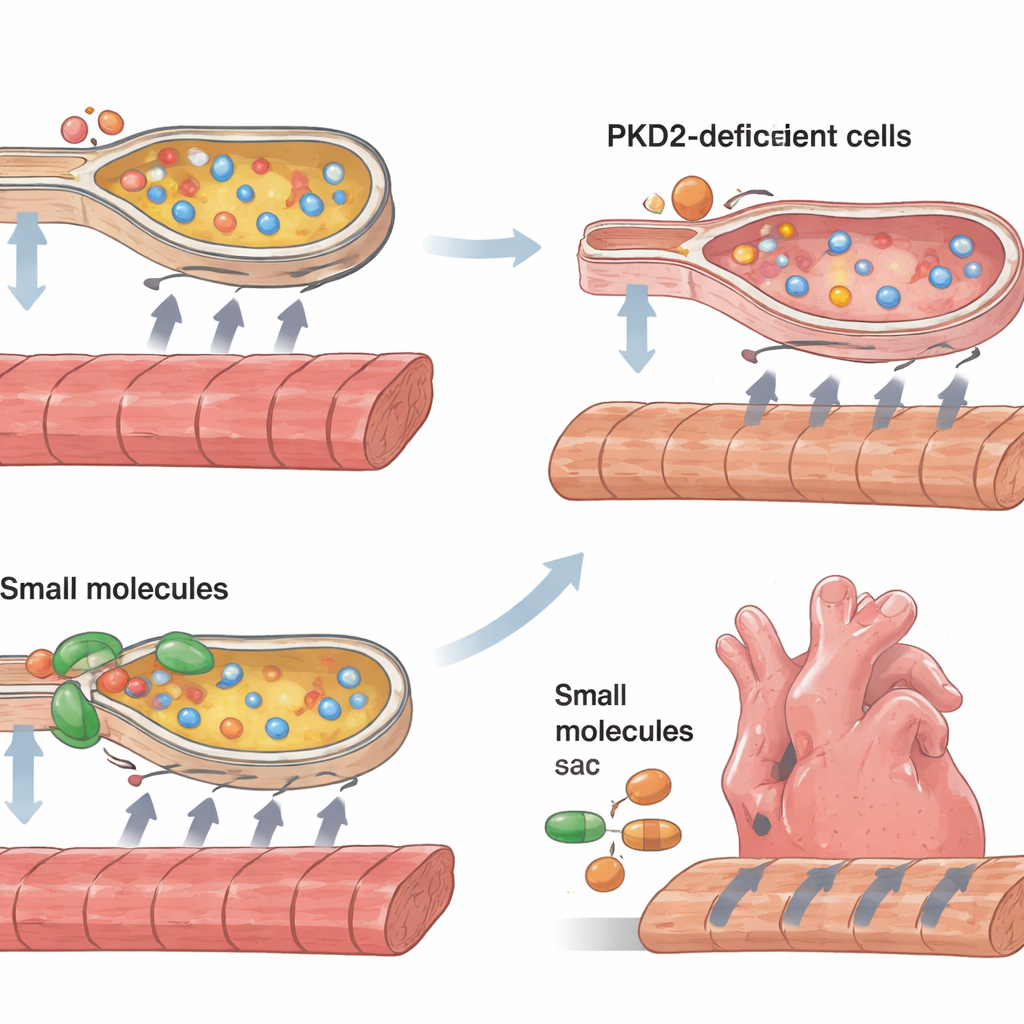
Cattiva gestione del calcio e stress cellulare
Le cellule cardiache dipendono da una gestione precisa del calcio, che entra nella cellula per innescare la contrazione e poi viene pompato nuovamente nei compartimenti di immagazzinamento interni affinché la cellula si rilassi e si prepari al battito successivo. Nelle cellule prive di sufficiente policistina-2, le ondate di calcio durante ogni battito erano più piccole e impiegavano più tempo a svuotarsi. Le sacche interne di stoccaggio, che si sovrappongono a una struttura chiamata reticolo endoplasmatico, sembravano contenere meno calcio e ricaricarsi più lentamente. Allo stesso tempo, i segnali molecolari di stress del reticolo endoplasmatico aumentavano nettamente, e più cellule presentavano marcatori di morte cellulare programmata e caratteristiche di ingrandimento associate alla cardiomiopatia. Una pompa chiave del calcio, SERCA2, e il suo partner regolatorio fosfolambano risultavano entrambi meno attivi, offrendo un collegamento meccanico concreto tra la proteina mancante e l’alterato ciclo del calcio.
Testare modi per aiutare i mini-cuori in difficoltà
Con questa immagine meccanicistica, i ricercatori hanno provato a recuperare le deboli strisce di tessuto. Hanno usato due piccole molecole, 4-fenilbutirrato e acido tauroursodesossicolico, che agiscono come assistenti chimici per il ripiegamento delle proteine e sono note per mitigare lo stress del reticolo endoplasmatico. Hanno inoltre applicato un composto chiamato CDN1163 che stimola l’attività della pompa SERCA. Tutti e tre i trattamenti hanno migliorato la forza di contrazione e accelerato sia la contrazione sia il rilassamento nelle strisce di tessuto, con guadagni particolarmente marcati nelle strisce carenti di policistina-2. Il recupero è stato solo parziale — queste interventi non hanno reso i tessuti completamente normali — ma hanno mostrato che alleviare lo stress cellulare e ripristinare il pompaggio del calcio può migliorare significativamente le prestazioni del muscolo cardiaco umano malato in questo modello.
Cosa significa per i pazienti
Questo lavoro dimostra che i difetti nella policistina-2 possono indebolire direttamente il muscolo cardiaco umano disturbando la gestione del calcio e sovraccaricando il sistema di controllo qualità interno della cellula, anche al di fuori del contesto di insufficienza renale o ipertensione. Costruendo e testando strisce cardiache umane bioingegnerizzate, lo studio collega un difetto genetico a una specifica catena di eventi: riduzione della policistina-2, pompe del calcio indebolite, aumento dello stress interno e, in ultima analisi, contrazioni più lente e più deboli. Non meno importante, la stessa piattaforma rivela che farmaci già noti per ridurre lo stress cellulare o potenziare il pompaggio del calcio possono ripristinare parzialmente la funzione. Sebbene resti molto lavoro prima che queste strategie possano essere testate sulle persone, i risultati indicano terapie realistiche e verificabili per le complicanze cardiache nascoste della malattia policistica renale.
Citazione: Li, J., Peng, W., Kwok, M. et al. Investigating PKD2 deficiency-associated cardiomyopathies using hESC-cardiomyocytes and bioengineered 3D ventricular cardiac tissue strips. Cell Death Dis 17, 368 (2026). https://doi.org/10.1038/s41419-026-08639-8
Parole chiave: malattia policistica renale, cardiomiopatia, segnalazione del calcio, modelli cardiaci da cellule staminali, stress del reticolo endoplasmatico