Clear Sky Science · ja
hESC心筋細胞とバイオエンジニアリングした3D心室組織ストリップを用いたPKD2欠損関連心筋症の解析
なぜ腎疾患が心臓に関係するのか
常染色体優性多発性嚢胞性腎疾患(ADPKD)は通常は腎臓の病気として扱われますが、多くの患者が重篤な心臓合併症も発症します。臨床では心室壁の肥厚、収縮力低下、不整脈が長く観察されてきましたが、腎嚢胞を引き起こす遺伝子異常と心筋障害を直接結びつける機構は明確ではありませんでした。本研究は、最先端の培養ヒト心組織を用いて単純だが重要な問いを投げかけます:腎関連タンパク質であるポリシスチン-2の欠損はどのようにして心臓を弱らせるのか、そしてその弱化は少なくとも部分的に回復できるのか?
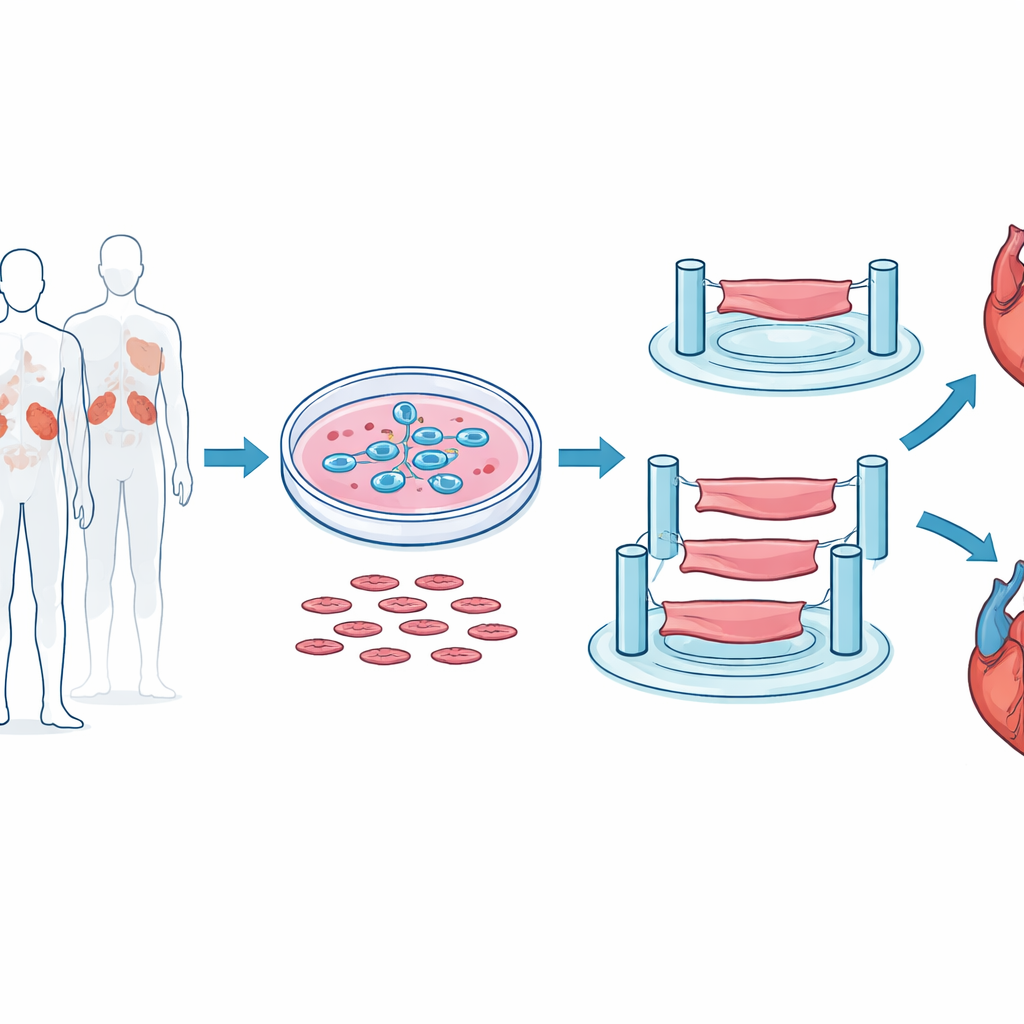
ラボでミニ心筋ストリップを作る
実際のヒト心臓に近づくために、研究者たちはマウス心や単層培養に頼りませんでした。代わりにヒト胚性幹細胞(hESC)を出発点とし、これを拍動する心筋細胞へと慎重に分化させました。それらの細胞を支持細胞やゲル状の足場と混合し、柔軟なポストの間でリズミカルに収縮する数ミリ長の微小な三次元心室組織ストリップに成形しました。この系により、ストリップが引く力、収縮・弛緩の速度、電気刺激への応答などを測定でき、心筋のミニチュアな運動試験のように機能を評価できます。
ポリシスチン-2が失われると何が起きるか
次に研究チームは遺伝学的手法でPKD2遺伝子をサイレンシングし、これらの心筋細胞でポリシスチン-2の量を減少させ、ADPKD患者で見られる欠損を模倣しました。ポリシスチン-2が抑制されると、組織ストリップは拍動を続けたものの、収縮力は著しく低下し、収縮および弛緩が遅延しました。この弱化は二つの独立した幹細胞系統と異なるサイレンシング法で再現され、ポリシスチン-2がヒト心筋の機能に実際に重要であることを支持します。重要なのは、組織の全体的な微細構造—基本的な配置や内部の足場構造—は正常に見え、粗大な損傷や解剖学的な乱れではなく細胞機能の障害が原因であることを示唆している点です。
カルシウムの不均衡と細胞内ストレス
心筋細胞は収縮を誘発するためにカルシウムを正確に扱うことに依存しており、収縮後は休止に備えてそのカルシウムを内部貯蔵へと再取り込みします。ポリシスチン-2が不足する細胞では、拍動ごとのカルシウムの流入が小さく、クリアされるのに時間がかかりました。小胞体と重なる内部貯蔵構造は保持するカルシウム量が減り、再充填も遅く見えました。同時に小胞体ストレスの分子マーカーが急増し、プログラム細胞死の指標や心筋症に伴う細胞肥大の特徴を示す細胞が増加しました。主要なカルシウムポンプであるSERCA2とその調節因子ホスホランバンはともに活性が低下しており、欠損タンパク質とカルシウム循環障害とを結ぶ具体的な機械的つながりを提供します。
弱ったミニ心筋を助ける方法の試験
このメカニズム像をもとに、研究者たちは弱った組織ストリップの機能回復を試みました。タンパク質の折りたたみを助け、小胞体ストレスを緩和することが知られる小分子化合物、4-フェニル酪酸とタウロウルソデオキシコール酸を用いました。さらにSERCAポンプ活性を高める化合物CDN1163も適用しました。これら三つの処置はいずれも収縮力を改善し、収縮および弛緩を速め、特にポリシスチン-2欠損のストリップで顕著な改善を示しました。回復は部分的であり、組織を完全に正常には戻しませんでしたが、細胞内ストレスを和らげカルシウムポンプを回復させることで病的ヒト心筋の性能を有意に向上させうることを示しました。
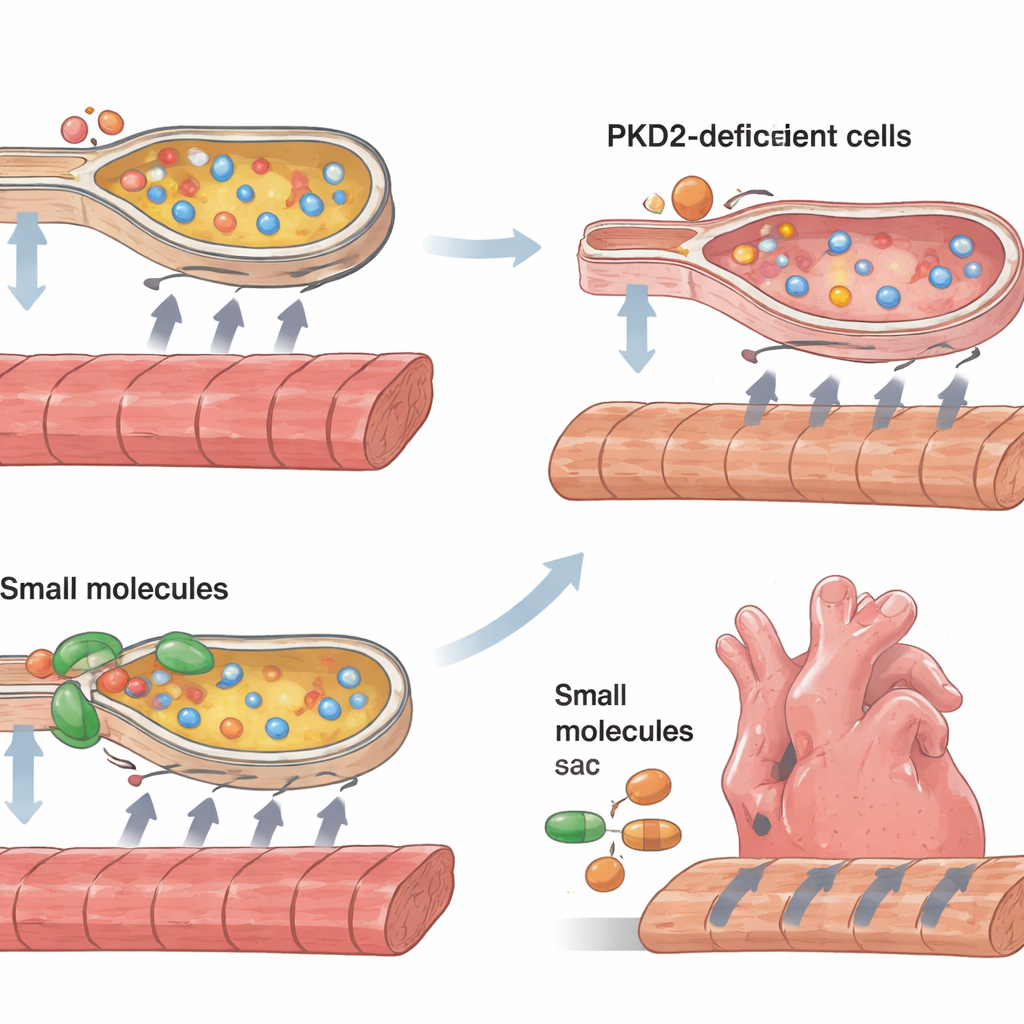
患者にとっての意義
本研究は、ポリシスチン-2の欠損がカルシウム制御の攪乱と細胞内品質管理系の過負荷を通じて、腎不全や高血圧の有無にかかわらずヒト心筋を直接弱らせうることを示しています。バイオエンジニアリングしたヒト心筋ストリップを構築・評価することで、遺伝的欠陥と一連の具体的な事象—ポリシスチン-2減少、カルシウムポンプ低下、内部ストレス上昇、結果としての収縮低下—を結びつけました。同時に、細胞ストレスを低減する薬剤やカルシウムポンプを強化する薬剤が機能を部分的に回復し得ることを示した点も重要です。これらの戦略を患者に適用するにはなお多くの検討が必要ですが、ADPKDの隠れた心合併症に対する現実的で検証可能な治療方針を指し示す結果です。
引用: Li, J., Peng, W., Kwok, M. et al. Investigating PKD2 deficiency-associated cardiomyopathies using hESC-cardiomyocytes and bioengineered 3D ventricular cardiac tissue strips. Cell Death Dis 17, 368 (2026). https://doi.org/10.1038/s41419-026-08639-8
キーワード: 多発性嚢胞性腎疾患, 心筋症, カルシウムシグナル伝達, 幹細胞心モデル, 小胞体ストレス