Clear Sky Science · de
Untersuchung von mit PKD2-Mangel verbundenen Kardiomyopathien mithilfe von hESC-Kardiomyozyten und bioingenieurtechnisch hergestellten 3D-Ventrikel-Herzstreifen
Warum Nierenerkrankungen fürs Herz wichtig sind
Menschen mit autosomal-dominanter polyzystischer Nierenerkrankung (ADPKD) gelten meist als Nierenpatienten, entwickeln aber häufig auch ernsthafte Herzprobleme. Ärztinnen und Ärzte beobachten seit Langem verdickte Herzwände, abgeschwächte Pumpfunktion und Rhythmusstörungen bei diesen Patientinnen und Patienten; der direkte Zusammenhang zwischen den fehlerhaften Genen, die Nierenzysten verursachen, und der Schädigung des Herzmuskels blieb jedoch unklar. Diese Studie nutzt hochmoderne, im Labor gezüchtete menschliche Herzgewebe, um eine einfache, aber wichtige Frage zu stellen: Wie schwächt ein Defekt in einem nierenspezifischen Protein, der Polycystin‑2, das Herz, und lässt sich diese Schwäche zumindest teilweise rückgängig machen?
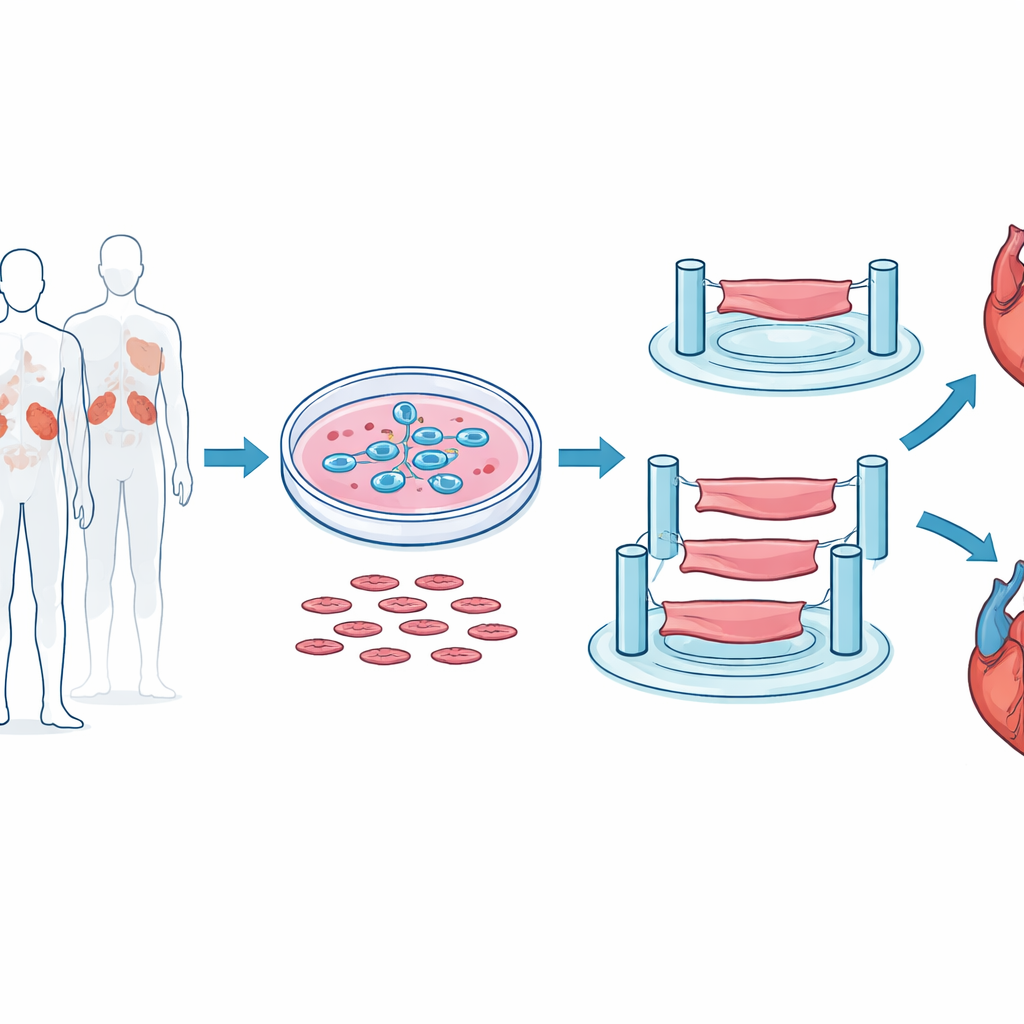
Mini-Herzstreifen im Labor herstellen
Um dem Verhalten des menschlichen Herzens möglichst nahe zu kommen, verzichteten die Forschenden auf Mausherzen oder flache Zellschichten. Stattdessen begannen sie mit humanen embryonalen Stammzellen und leiteten diese gezielt zu schlagenden Herzmuskelzellen (Kardiomyozyten) her. Diese Zellen wurden dann mit Stützzellen und gelartigen Gerüsten vermischt und zu winzigen dreidimensionalen Ventrikelstreifen geformt, jeweils nur wenige Millimeter lang, aber in der Lage, rhythmisch zwischen flexiblen Pfosten zu kontrahieren. Dieses System erlaubte dem Team zu messen, wie stark die Streifen zogen, wie schnell sie sich zusammenzogen und entspannten und wie sie auf elektrische Stimulation reagierten — ähnlich einem Mini-Workout-Test für Herzmuskel.
Was passiert, wenn Polycystin‑2 fehlt
Als Nächstes reduzierten die Forschenden die Menge an Polycystin‑2 in diesen Herzmuskelzellen mithilfe genetischer Werkzeuge, die das PKD2-Gen stilllegen, um den Defekt zu simulieren, der bei vielen ADPKD-Patienten vorkommt. Nach Knockdown von Polycystin‑2 schlugen die Gewebestreifen zwar weiter, aber sie erzeugten deutlich weniger Kraft und ihre Kontraktionen sowie Relaxationen wurden träge. Diese Schwäche zeigte sich in zwei unabhängigen Stammzelllinien und mit unterschiedlichen Stilllegungsmethoden, was die Bedeutung von Polycystin‑2 für die Leistungsfähigkeit des menschlichen Herzmuskels untermauert. Wichtig ist, dass die Gesamtmikrostruktur des Gewebes — seine grundlegende Organisation und interne Gerüststruktur — normal aussah, was auf eine Funktionsstörung der Zellen statt auf grobe Schäden oder Desorganisation hinweist.
Calciumfehlsteuerung und zellulärer Stress
Herzmuskelzellen sind auf präzise Calcium-Regelung angewiesen: Calcium strömt in die Zelle, um die Kontraktion auszulösen, und wird dann wieder in interne Speicherkammern gepumpt, damit die Zelle relaxieren und sich auf den nächsten Schlag vorbereiten kann. In Zellen mit zu wenig Polycystin‑2 waren die Calcium‑Spitzen bei jedem Schlag kleiner und benötigten länger zum Abklingen. Die internen Speicherblasen, die mit dem endoplasmatischen Retikulum überlappen, schienen weniger Calcium zu halten und langsamer wieder aufgefüllt zu werden. Gleichzeitig stiegen molekulare Marker für ER‑Stress deutlich an, und mehr Zellen zeigten Zeichen programmierter Zellsterblichkeit sowie Vergrößerungsmerkmale, die mit Kardiomyopathie assoziiert sind. Eine wichtige Calcium‑Pumpe, SERCA2, und ihr Regulationspartner Phospholamban waren beide weniger aktiv, was eine konkrete mechanische Verbindung zwischen dem fehlenden Protein und der gestörten Calcium‑Zyklik liefert.
Ansätze zur Unterstützung der geschwächten Mini‑Herzen testen
Ausgestattet mit diesem mechanistischen Bild versuchten die Forschenden, die schwachen Gewebestreifen zu retten. Sie verwendeten zwei kleine Moleküle, 4‑Phenylbutyrat und Tauroursodeoxycholsäure, die als chemische Hilfen beim Proteinfalten wirken und dafür bekannt sind, ER‑Stress zu lindern. Außerdem setzten sie eine Verbindung namens CDN1163 ein, die die SERCA‑Pumpenaktivität steigert. Alle drei Behandlungen verbesserten die Kontraktionskraft und beschleunigten sowohl Kontraktion als auch Relaxation der Gewebestreifen, mit besonders starken Verbesserungen in Streifen ohne Polycystin‑2. Die Rettung war nur teilweise — die Interventionen stellten die Gewebe nicht vollständig normal wieder her — zeigte aber, dass die Verringerung zellulären Stresses und die Wiederherstellung der Calcium‑Pumpleistung die Funktion erkrankter menschlicher Herzmuskeln in diesem Modell merklich verbessern können.
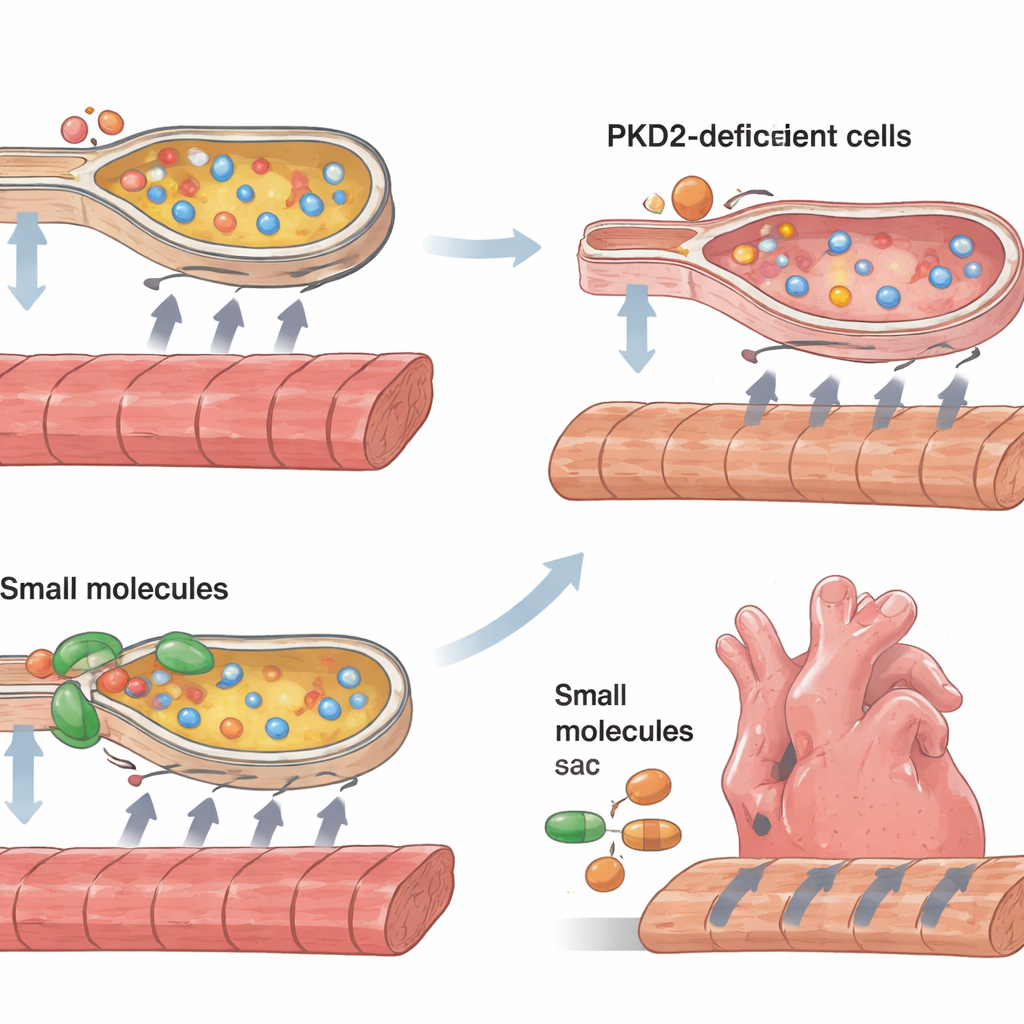
Was das für Patientinnen und Patienten bedeutet
Diese Arbeit zeigt, dass Defekte in Polycystin‑2 den menschlichen Herzmuskel direkt schwächen können, indem sie die Calcium‑Handhabung stören und das interne Qualitätskontrollsystem der Zelle überlasten — selbst außerhalb des Kontexts versagender Nieren oder Bluthochdrucks. Durch den Aufbau und die Prüfung bioengineerter menschlicher Herzstreifen verbindet die Studie eine genetische Störung mit einer klaren Ereigniskette: verringerte Polycystin‑2, geschwächte Calcium‑Pumpen, zunehmender interner Stress und schließlich träge, schwächere Kontraktionen. Ebenso wichtig ist, dass dieselbe Plattform zeigt, dass bereits bekannte Wirkstoffe, die zellulären Stress reduzieren oder die Calcium‑Pumpe fördern, die Funktion teilweise wiederherstellen können. Zwar ist noch viel Arbeit nötig, bevor diese Strategien am Menschen erprobt werden können, doch die Ergebnisse deuten auf realistische, überprüfbare Therapien für die oft verborgenen Herzkomplikationen der polyzystischen Nierenerkrankung hin.
Zitation: Li, J., Peng, W., Kwok, M. et al. Investigating PKD2 deficiency-associated cardiomyopathies using hESC-cardiomyocytes and bioengineered 3D ventricular cardiac tissue strips. Cell Death Dis 17, 368 (2026). https://doi.org/10.1038/s41419-026-08639-8
Schlüsselwörter: polyzystische Nierenerkrankung, Kardiomyopathie, Calcium-Signalgebung, Stammzell-Herzmodelle, Endoplasmatischer-Retikulum-Stress