Clear Sky Science · fr
Étudier les cardiomyopathies associées à une déficience en PKD2 à l’aide de cardiomyocytes dérivés d’hESC et de bandes ventriculaires cardiaques 3D bio-ingénierées
Pourquoi la maladie rénale importe pour le cœur
Les personnes atteintes de maladie rénale polykystique autosomique dominante (MRPAD) sont généralement considérées comme des patients rénaux, mais beaucoup développent aussi des problèmes cardiaques sérieux. Les cliniciens ont depuis longtemps observé un épaississement des parois cardiaques, une faiblesse de la contraction et des rythmes anormaux chez ces patients, pourtant le lien direct entre les gènes défectueux qui provoquent des kystes rénaux et les lésions du muscle cardiaque est resté flou. Cette étude utilise des tissus cardiaques humains cultivés en laboratoire à la pointe de la technologie pour poser une question simple mais importante : comment un défaut d’une protéine liée aux reins, appelée polycystine‑2, affaiblit‑il le cœur, et cette faiblesse peut‑elle être au moins partiellement renversée ?
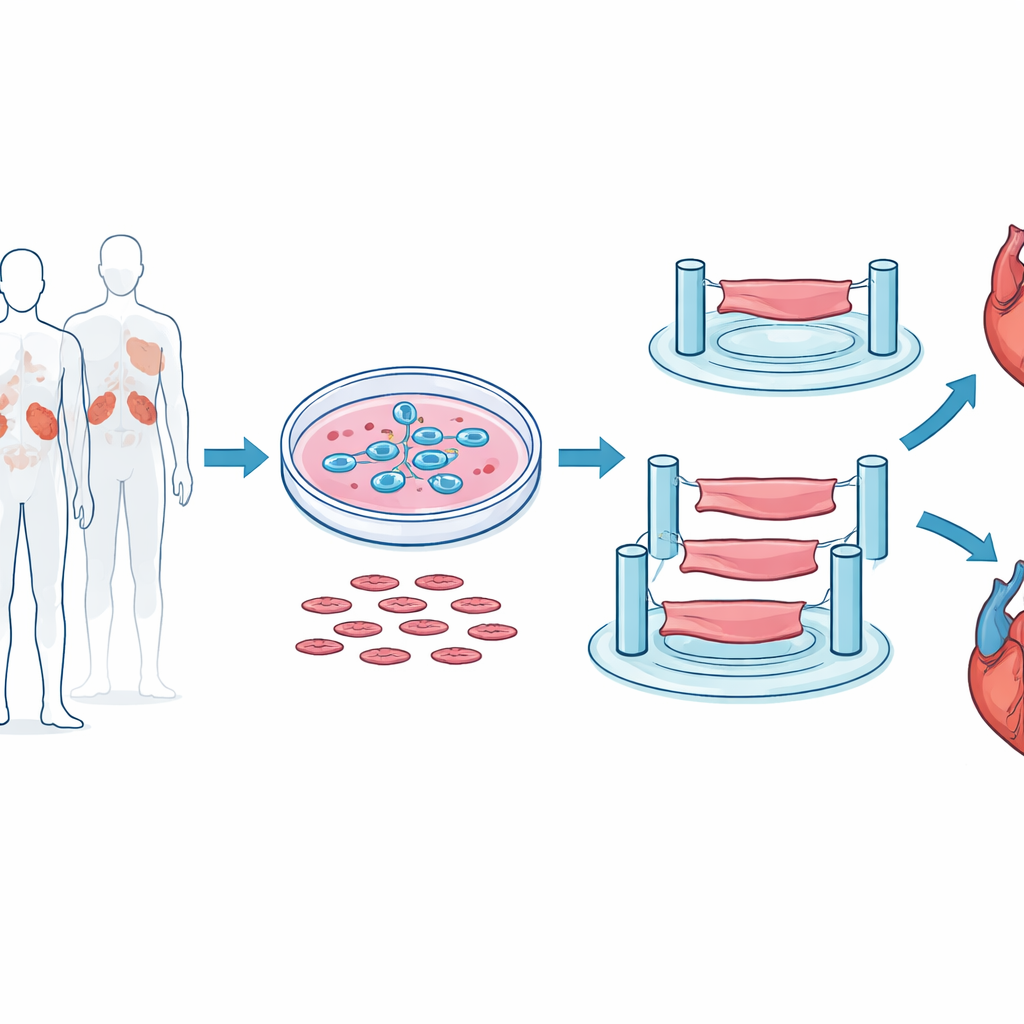
Construire des bandes miniatures de cœur en laboratoire
Pour se rapprocher le plus possible du comportement du cœur humain, les chercheurs ne se sont pas appuyés sur des cœurs de souris ni sur des couches cellulaires plates. Ils ont commencé par des cellules souches embryonnaires humaines et les ont guidées avec soin pour qu’elles deviennent des cellules musculaires cardiaques battantes. Ces cellules ont ensuite été mélangées à des cellules de soutien et à des échafaudages gélifiés, puis moulées en petites bandes tridimensionnelles de tissu ventriculaire, chacune ne mesurant que quelques millimètres de long mais capable de se contracter rythmiquement entre des colonnes flexibles. Ce dispositif a permis à l’équipe de mesurer la force de contraction des bandes, la vitesse de contraction et de relaxation, et leur réponse à un pacing électrique, un peu comme un test d’effort miniature pour le muscle cardiaque.
Que se passe‑t‑il quand la polycystine‑2 disparaît
L’équipe a ensuite réduit la quantité de polycystine‑2 dans ces cellules cardiaques en utilisant des outils génétiques qui silencient le gène PKD2, reproduisant le défaut observé chez de nombreux patients atteints de MRPAD. Lorsque la polycystine‑2 était diminuée, les bandes tissulaires continuaient de battre, mais elles se contractaient avec beaucoup moins de force et leurs contractions et relaxations devenaient lentes. Cette faiblesse est apparue dans deux lignées indépendantes de cellules souches et avec différentes méthodes de silencement, ce qui renforce l’hypothèse que la polycystine‑2 est réellement importante pour la performance du muscle cardiaque humain. Fait important, la microstructure globale du tissu — son organisation de base et son échafaudage interne — semblait normale, indiquant un problème de fonction cellulaire plutôt qu’un dommage ou une désorganisation manifeste.
Mauvaise gestion du calcium et stress cellulaire
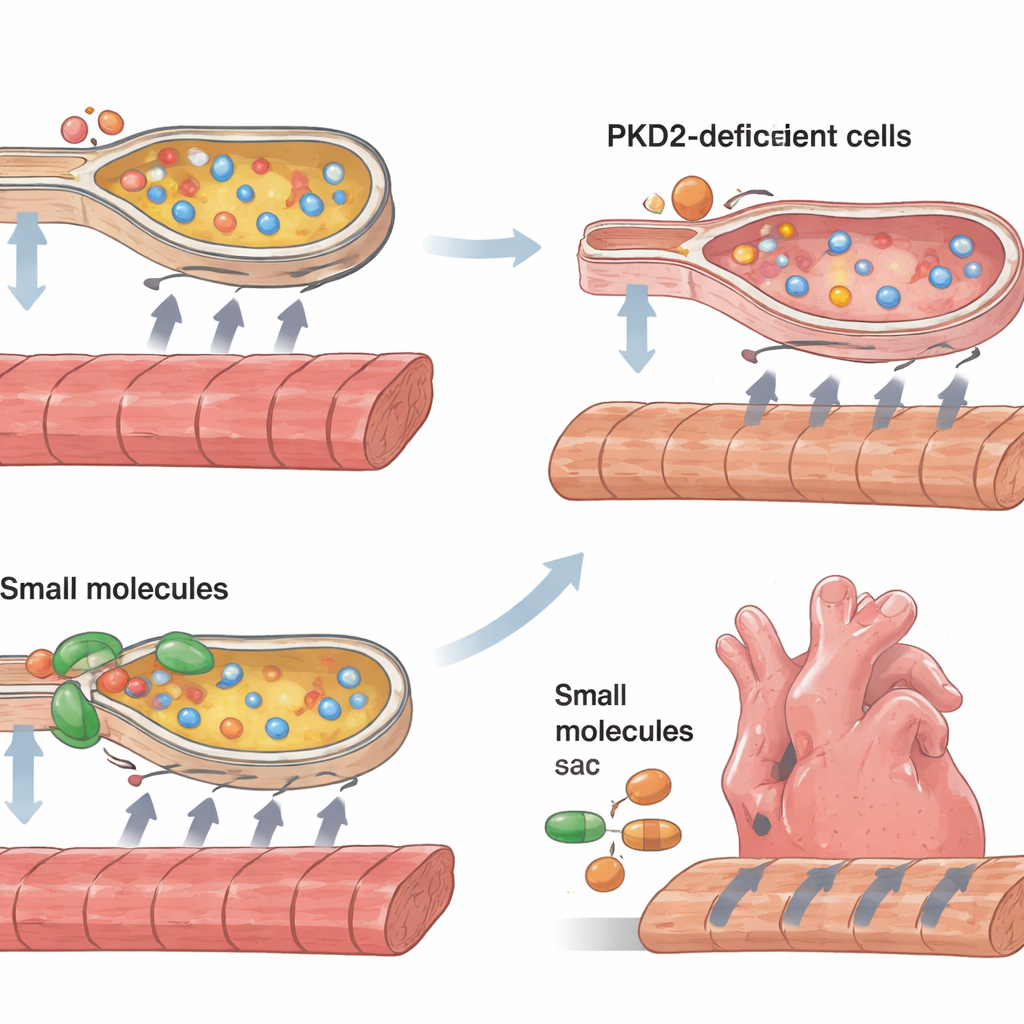
Les cellules cardiaques dépendent d’une gestion précise du calcium, qui inonde la cellule pour déclencher la contraction puis est pompé dans des compartiments de stockage internes pour permettre la relaxation et préparer le battement suivant. Dans les cellules manquant de polycystine‑2, les pics calciques lors de chaque battement étaient plus faibles et mettaient plus de temps à se résorber. Les sacs de stockage internes, qui chevauchent une structure appelée réticulum endoplasmique, semblaient contenir moins de calcium et se remplir plus lentement. Parallèlement, les signes moléculaires de stress du réticulum endoplasmique augmentaient fortement, et davantage de cellules montraient des marqueurs d’apoptose programmée et des caractéristiques d’hypertrophie associées à la cardiomyopathie. Une pompe calcique clé, SERCA2, et son partenaire régulateur phospholamban étaient tous deux moins actifs, offrant un lien mécanique concret entre la protéine manquante et l’altération du cycle calcique.
Tester des moyens d’aider les mini‑cœurs défaillants
Fort de ce tableau mécanistique, les chercheurs ont tenté de rescaper les bandes tissulaires faibles. Ils ont utilisé deux petites molécules, le 4‑phénylbutyrate et l’acide tauroursodésoxycholique, qui agissent comme aides chimiques au repliement des protéines et sont connus pour atténuer le stress du réticulum endoplasmique. Ils ont aussi appliqué un composé appelé CDN1163 qui stimule l’activité de la pompe SERCA. Les trois traitements ont amélioré la force de contraction et accéléré à la fois la contraction et la relaxation des bandes tissulaires, avec des gains particulièrement marqués dans les bandes dépourvues de polycystine‑2. Le sauvetage n’était que partiel — ces interventions n’ont pas rendu les tissus complètement normaux — mais elles ont montré que réduire le stress cellulaire et restaurer le pompage du calcium peut améliorer de manière significative la performance du muscle cardiaque humain malade dans ce modèle.
Que signifie cela pour les patients
Ce travail montre que les défauts en polycystine‑2 peuvent affaiblir directement le muscle cardiaque humain en perturbant la gestion du calcium et en surchargeant le système de contrôle de la qualité interne de la cellule, même en dehors du contexte d’un rein défaillant ou d’une hypertension. En construisant et en testant des bandes cardiaques humaines bio‑ingénierées, l’étude relie un défaut génétique à une chaîne d’événements spécifiques : diminution de la polycystine‑2, affaiblissement des pompes calciques, montée du stress interne et, finalement, contractions plus lentes et plus faibles. Tout aussi important, cette même plateforme révèle que des médicaments déjà connus pour réduire le stress cellulaire ou améliorer le pompage calcique peuvent restaurer partiellement la fonction. Bien qu’il reste beaucoup à faire avant que ces stratégies puissent être testées chez l’homme, les résultats suggèrent des thérapies réalistes et testables pour les complications cardiaques discrètes de la maladie rénale polykystique.
Citation: Li, J., Peng, W., Kwok, M. et al. Investigating PKD2 deficiency-associated cardiomyopathies using hESC-cardiomyocytes and bioengineered 3D ventricular cardiac tissue strips. Cell Death Dis 17, 368 (2026). https://doi.org/10.1038/s41419-026-08639-8
Mots-clés: maladie rénale polykystique, cardiomyopathie, signalisation calcique, modèles cardiaques à partir de cellules souches, stress du réticulum endoplasmique