Clear Sky Science · es
Investigación de las miocardiopatías asociadas a la deficiencia de PKD2 mediante cardiomiocitos derivados de hESC y tiras ventriculares cardíacas 3D bioingenierizadas
Por qué la enfermedad renal importa para el corazón
Las personas con enfermedad renal poliquística autosómica dominante (ERPAD) suelen considerarse pacientes renales, pero muchas también desarrollan problemas cardíacos graves. Los médicos han observado durante mucho tiempo engrosamiento de las paredes cardíacas, una capacidad de contracción reducida y ritmos anormales en estos pacientes, sin que hasta ahora quedara claro el vínculo directo entre los genes defectuosos que causan los quistes renales y el daño al músculo cardíaco. Este estudio utiliza tejidos cardíacos humanos cultivados con técnicas avanzadas para plantear una pregunta simple pero importante: ¿cómo debilita el corazón un defecto en una proteína relacionada con el riñón, llamada policistina‑2, y puede esa debilidad revertirse al menos en parte?
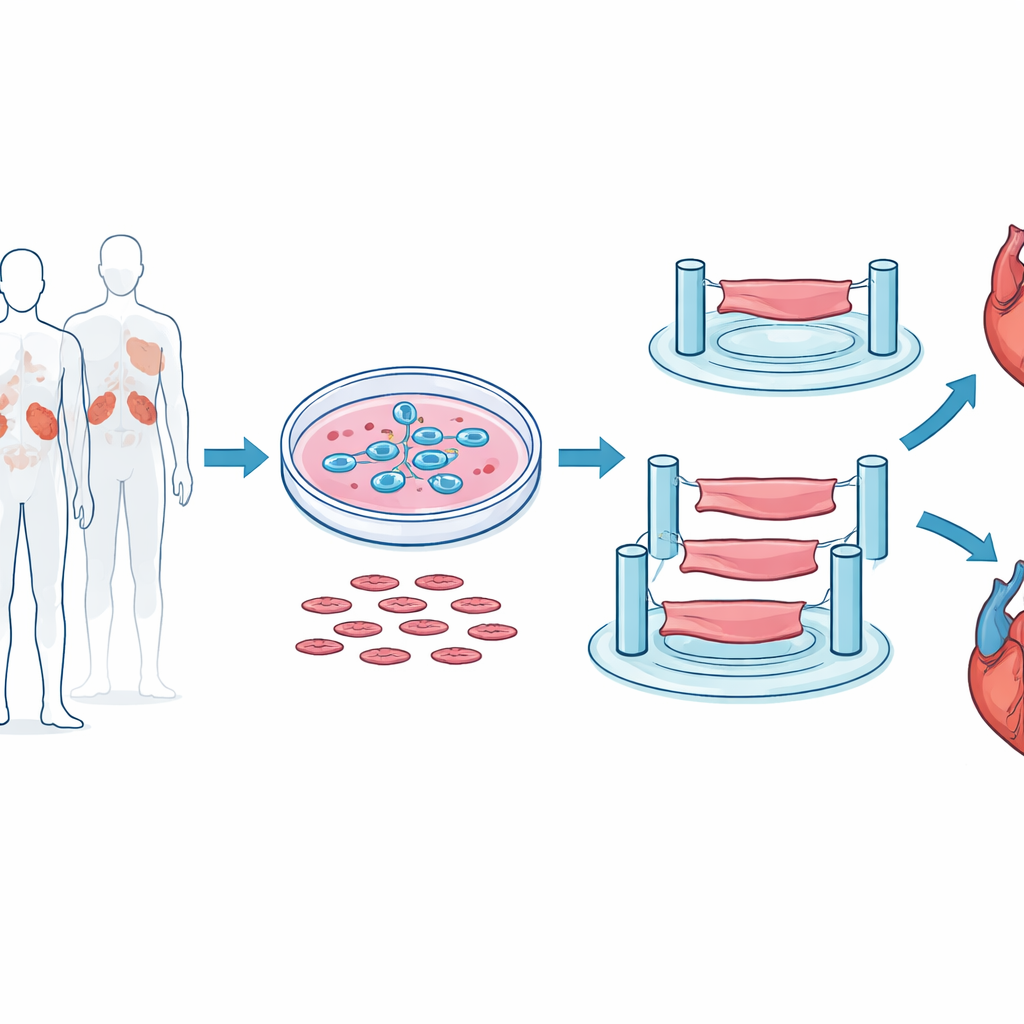
Construyendo tiras de mini corazón en el laboratorio
Para acercarse lo más posible al comportamiento real del corazón humano, los investigadores no se basaron en corazones de ratón ni en monocapas celulares. En su lugar, empezaron con células madre embrionarias humanas y las guiaron cuidadosamente para que se convirtieran en cardiomiocitos que laten. Estas células se mezclaron con células de soporte y andamios gelatinosos y se moldearon en pequeñas tiras tridimensionales de tejido ventricular, de apenas unos pocos milímetros de longitud, capaces de contraerse rítmicamente entre postes flexibles. Esta disposición permitió al equipo medir cuánto fuerza generaban las tiras, la rapidez de sus contracciones y relajaciones y su respuesta al estímulo eléctrico, algo así como una prueba de esfuerzo en miniatura para el músculo cardíaco.
Qué sucede cuando se pierde la policistina‑2
El equipo redujo a continuación la cantidad de policistina‑2 en estas células cardíacas usando herramientas genéticas que silencian el gen PKD2, imitando el defecto observado en muchos pacientes con ERPAD. Cuando la policistina‑2 se redujo, las tiras de tejido seguían latiendo, pero generaban mucha menos fuerza y sus contracciones y relajaciones se volvieron más lentas. Esta debilidad apareció en dos líneas independientes de células madre y con distintos métodos de silenciamiento, lo que refuerza la idea de que la policistina‑2 es verdaderamente importante para el rendimiento del músculo cardíaco humano. Es importante destacar que la microestructura general del tejido —su organización básica y andamiaje interno— parecía normal, lo que sugiere un problema en la función celular más que un daño o desorganización macroscópicos.
Mala gestión del calcio y estrés celular
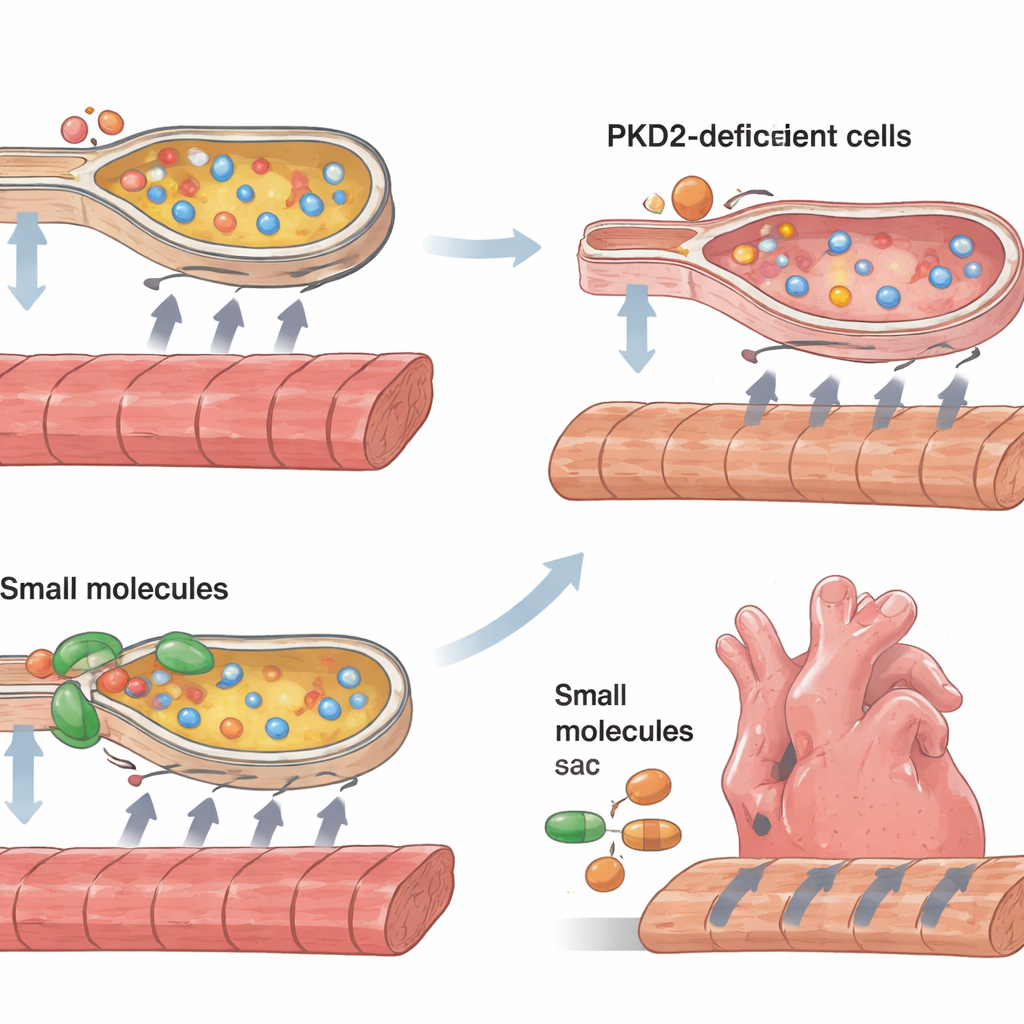
Las células cardíacas dependen de un manejo preciso del calcio: éste entra rápidamente en la célula para activar la contracción y luego se bombea de nuevo a los compartimentos internos de almacenamiento para que la célula pueda relajarse y prepararse para el siguiente latido. En las células con insuficiente policistina‑2, los picos de calcio en cada latido eran menores y tardaban más en eliminarse. Los sacos de almacenamiento internos, que se solapan con una estructura llamada retículo endoplásmico, parecían contener menos calcio y rellenarse más despacio. Al mismo tiempo, los marcadores moleculares de estrés del retículo endoplásmico aumentaron considerablemente, y más células mostraron señales de muerte celular programada y rasgos de hipertrofia asociados a la miocardiopatía. Una bomba clave de calcio, SERCA2, y su regulador fosfolamban mostraron menor actividad, lo que ofrece un vínculo mecánico concreto entre la proteína faltante y el ciclo de calcio deteriorado.
Probando maneras de ayudar a los mini corazones fallidos
Con este panorama mecanístico, los investigadores intentaron rescatar las tiras de tejido debilitadas. Usaron dos pequeñas moléculas, 4‑fenilbutirato y ácido tauroursodesoxicólico, que actúan como ayudantes químicos en el plegamiento de proteínas y se sabe que alivian el estrés del retículo endoplásmico. También aplicaron un compuesto llamado CDN1163 que estimula la actividad de la bomba SERCA. Los tres tratamientos mejoraron la fuerza de contracción y aceleraron tanto la contracción como la relajación en las tiras de tejido, con ganancias particularmente notables en las tiras con déficit de policistina‑2. La recuperación fue solo parcial —estas intervenciones no normalizaron completamente los tejidos— pero demostraron que aliviar el estrés celular y restaurar el bombeo de calcio puede mejorar de forma significativa el rendimiento del músculo cardíaco humano enfermo en este modelo.
Qué significa esto para los pacientes
Este trabajo muestra que los defectos en la policistina‑2 pueden debilitar directamente el músculo cardíaco humano al alterar el manejo del calcio y sobrecargar el sistema interno de control de calidad de la célula, incluso fuera del contexto de insuficiencia renal o hipertensión. Al construir y probar tiras cardíacas humanas bioingenierizadas, el estudio conecta un fallo genético con una cadena específica de eventos: menos policistina‑2, bombas de calcio más débiles, aumento del estrés interno y, en última instancia, contracciones más lentas y menos potentes. Igualmente importante, la misma plataforma revela que fármacos ya conocidos por reducir el estrés celular o mejorar el bombeo de calcio pueden restaurar parcialmente la función. Aunque queda mucho por hacer antes de que estas estrategias puedan probarse en personas, los hallazgos señalan terapias realistas y susceptibles de ensayo para las complicaciones cardíacas ocultas de la enfermedad renal poliquística.
Cita: Li, J., Peng, W., Kwok, M. et al. Investigating PKD2 deficiency-associated cardiomyopathies using hESC-cardiomyocytes and bioengineered 3D ventricular cardiac tissue strips. Cell Death Dis 17, 368 (2026). https://doi.org/10.1038/s41419-026-08639-8
Palabras clave: enfermedad renal poliquística, miocardiopatía, señalización del calcio, modelos cardíacos con células madre, estrés del retículo endoplásmico