Clear Sky Science · zh
一种新的候选抑瘤因子 tRF-Ser 通过调控 CNBP/HSPA8 轴抑制胃癌进展
这对胃癌为何重要
胃(胃部)癌仍然是全球最致命的癌症之一,部分原因在于肿瘤常常对化疗产生耐药且易于广泛转移。本研究揭示了胃细胞内一种先前未知的天然防御机制:一种名为 tRF-Ser 的微小 RNA 片段,有助于抑制肿瘤。通过阐明该分子如何减缓癌症生长、促进一种铁依赖性细胞死亡形式并增强化疗效果,研究指出了针对难以控制的肿瘤患者的潜在新治疗策略。
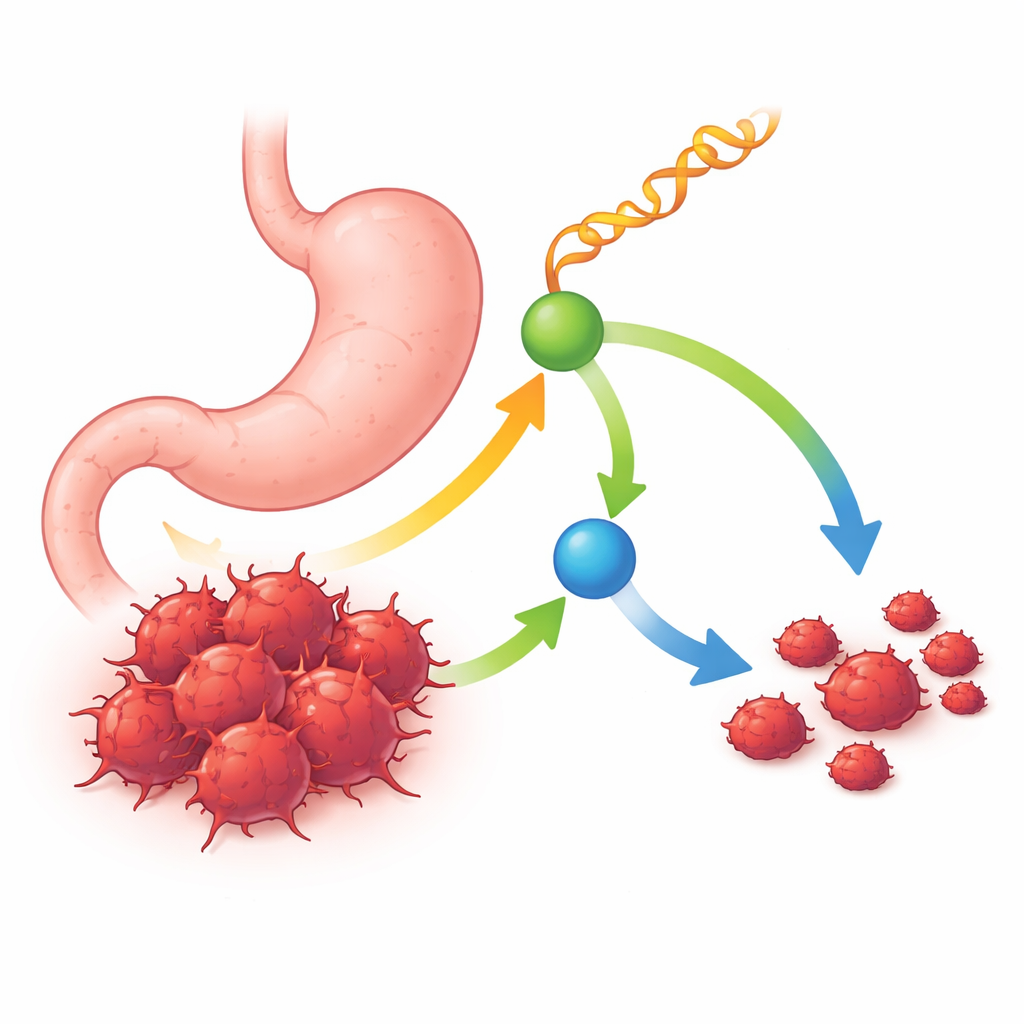
一种具有重要保护作用的小 RNA
研究人员首先比较了人类胃肿瘤与附近健康组织中的小 RNA 分子,重点关注一类称为 tRNA 衍生片段的特殊分子——从细胞的蛋白合成适配子 RNA 中切割出的短片段。在众多候选者中,一种片段脱颖而出:tRF-Ser,其在肿瘤样本和胃癌细胞系中的表达持续低于正常组织。肿瘤中 tRF-Ser 含量较高的患者往往存活时间更长,肿瘤体积更小、分期更低并且淋巴结转移更少。这些模式提示 tRF-Ser 作为一种随着疾病进展而丧失的天然抑瘤因子。
tRF-Ser 如何减缓肿瘤生长与扩散
为检验 tRF-Ser 的实际功能,团队在体外培养的胃癌细胞中上调或抑制其水平。当 tRF-Ser 增加时,癌细胞分裂速度减慢,克隆形成减少,更多细胞在细胞周期早期被阻止进入 DNA 复制阶段。细胞迁移与穿膜侵袭能力也下降,驱动肿瘤扩散的上皮-间质转化(EMT)关键标志物表达降低。相反,当 tRF-Ser 下调时,细胞生长更快、侵袭性更强且呈现更明显的 EMT 特征。在小鼠体内,工程化表达额外 tRF-Ser 的肿瘤细胞形成的皮下肿瘤更小且肺部转移更少,证实这种小 RNA 能在生物体内抑制癌症。
重塑癌细胞的应激与死亡通路
除了单纯减缓增殖外,tRF-Ser 促使癌细胞倾向于一种铁依赖且由脂质氧化驱动的细胞死亡形式——铁死亡。在接受诱导铁死亡药物处理时,富含 tRF-Ser 的细胞表现出更多的氧化损伤、线粒体破坏以及关键保护酶 GPX4 水平下降;当 tRF-Ser 缺乏时则呈现相反模式。研究还考察了经典化疗药物 5-氟尿嘧啶(5‑FU)的反应。含量较高的 tRF-Ser 使细胞更容易被该药物杀死,而 tRF-Ser 较低的细胞更具耐药性。在小鼠模型中,将 tRF-Ser 过表达与 5‑FU 及铁死亡诱导剂联合使用,产生了最强的肿瘤缩小效果,并在肿瘤内观察到明显的氧化损伤生化信号增强。
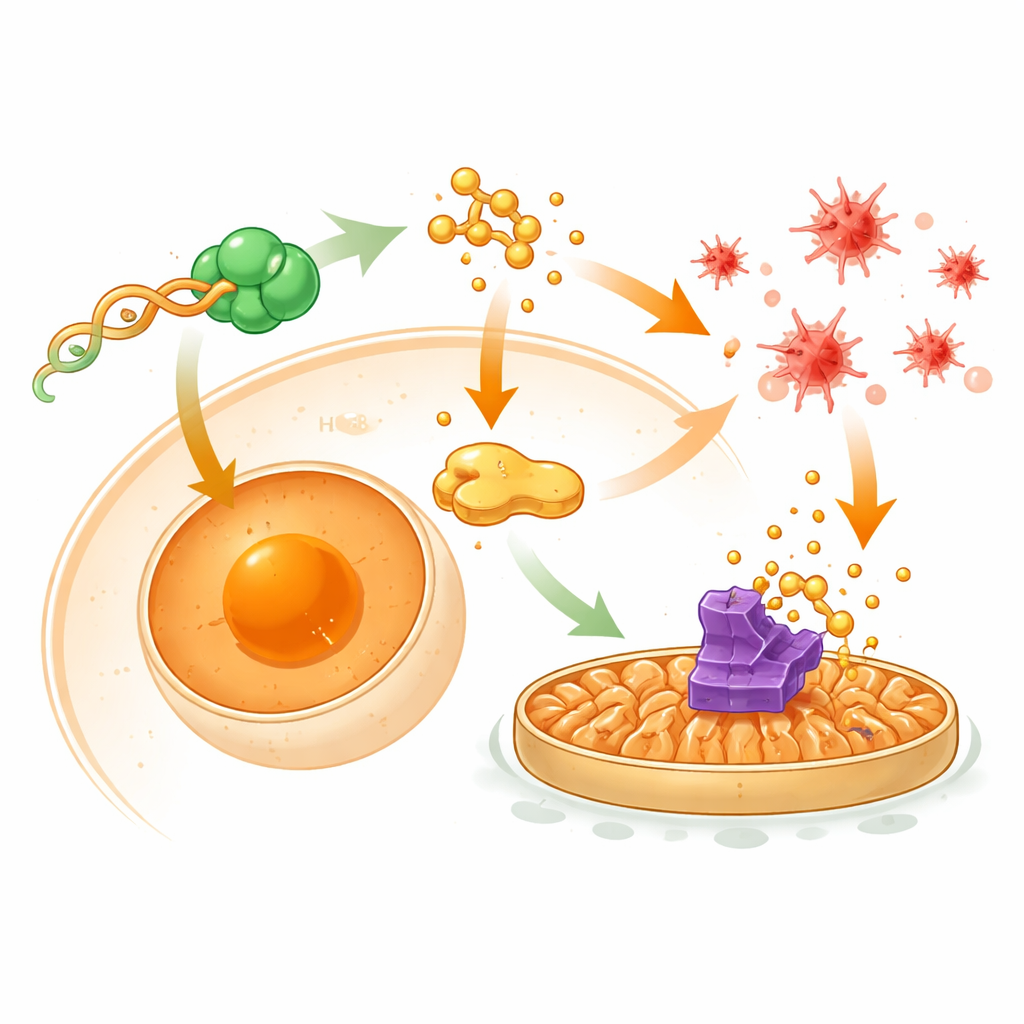
肿瘤细胞内隐藏的控制回路
为了解这些效应背后的连接方式,研究人员绘制了 tRF-Ser 与蛋白及下游基因的互作图谱。他们发现 tRF-Ser 可以物理结合一种称为 CNBP 的 DNA 结合蛋白,并使更多 CNBP 停留在细胞质中而非进入细胞核。正常情况下,进入核内的 CNBP 会激活一种分子伴侣基因 HSPA8,后者有助于维持 GPX4 并支持涉及 β-连环蛋白的 EMT 驱动信号。通过将 CNBP 阻留在细胞质,tRF-Ser 降低了 HSPA8 水平,削弱了 β-连环蛋白进入细胞核的能力,并使另一蛋白 STUB1 能够标记 GPX4 以便降解。该级联反应同时抑制与侵袭相关的 EMT 并解除对铁死亡的抑制,从而使癌细胞更易受到氧化损伤和化疗的影响。
这对未来治疗意味着什么
综上所述,该研究揭示了一个紧凑的调控轴——tRF-Ser、CNBP 与 HSPA8——将肿瘤生长、转移行为、细胞死亡和药物反应联系在一起。通俗地说,tRF-Ser 类似一名分子交通警察,将一个促生长因子(CNBP)从细胞的控制中心引偏,使其无法打开一套生存程序(经由 HSPA8 和 GPX4)。恢复或模拟 tRF-Ser,或靶向其下游伙伴,因而有望增强现有药物(如 5‑氟尿嘧啶)的疗效并帮助克服治疗耐药。尽管在临床应用前仍需进一步研究,本研究突显了微小 RNA 片段在将癌细胞从生存推向自毁方面可能发挥的关键作用。
引用: Jiao, J., Wang, G., Liu, J. et al. A new candidate tumor suppressor tRF-Ser inhibits gastric cancer progression by regulating the CNBP/HSPA8 axis. Cell Death Dis 17, 379 (2026). https://doi.org/10.1038/s41419-026-08608-1
关键词: 胃癌, 抑瘤 RNA, 铁死亡, 化疗耐药, HSPA8 CNBP 轴