Clear Sky Science · ru
Новый кандидат на роль супрессора опухоли tRF-Ser тормозит прогрессирование рака желудка, регулируя ось CNBP/HSPA8
Почему это важно для рака желудка
Рак желудка остается одним из самых смертельных видов рака в мире, отчасти потому что опухоли часто устойчивы к химиотерапии и агрессивно метастазируют. В этом исследовании выявлена ранее неописанная естественная защита в клетках желудка: крошечный фрагмент РНК под названием tRF-Ser, который помогает сдерживать опухолевый рост. Показав, как эта молекула замедляет развитие рака, способствует форме клеточной гибели, зависящей от железа, и повышает эффективность химиотерапии, исследование указывает на новые стратегии лечения пациентов с трудно контролируемыми опухолями.
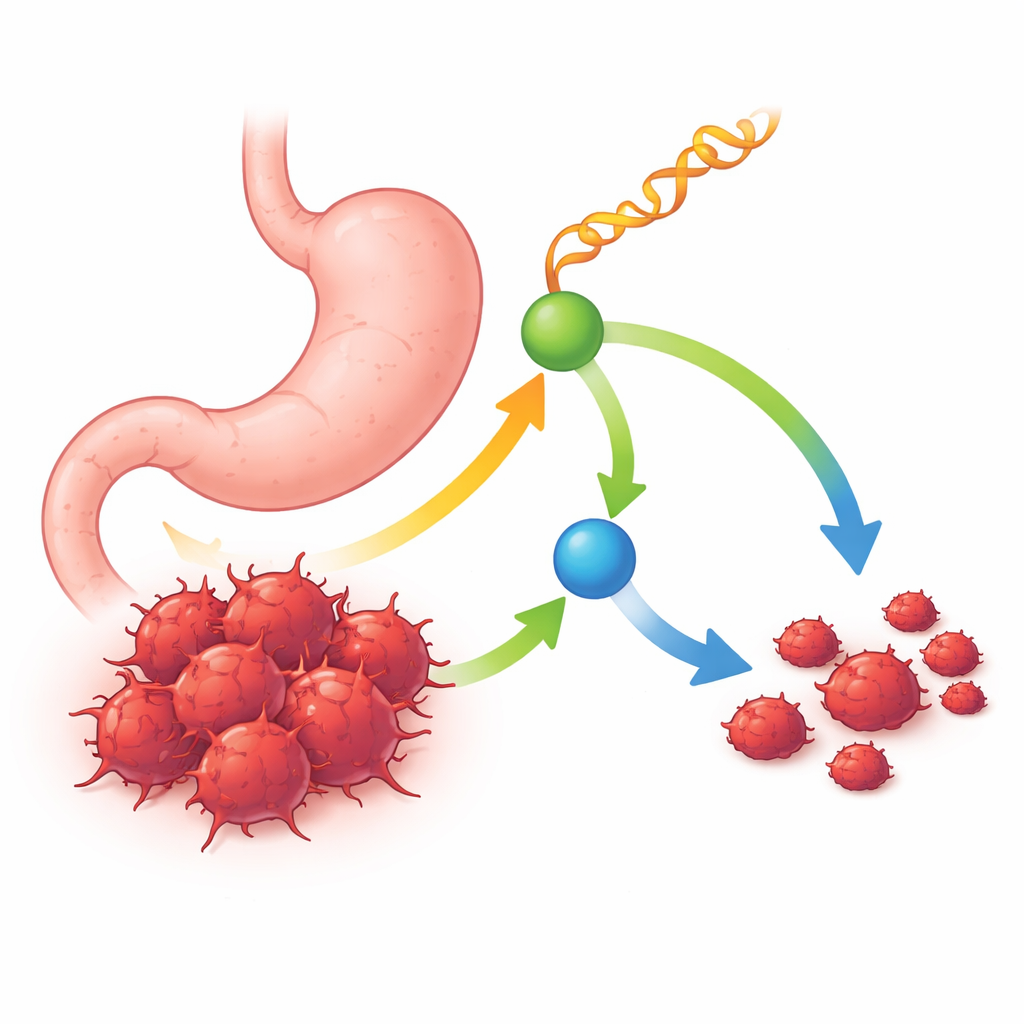
Маленькая РНК с большой защитной ролью
Исследователи начали с сравнения малых молекул РНК в образцах рака желудка и прилежащих здоровых тканях. Они сосредоточились на особом классе — фрагментах, происходящих от тРНК (tRNA‑derived fragments) — коротких отрезках, отрезаемых от адаптерных РНК, участвующих в синтезе белка. Среди множества кандидатов выделился один фрагмент: tRF-Ser, уровень которого в опухолевых образцах и клеточных линиях рака желудка был постоянно ниже, чем в нормальных тканях. У пациентов с опухолями, содержащими больше tRF-Ser, наблюдалась более длительная выживаемость, меньшие и менее прогрессирующие опухоли и меньше метастазов в лимфатических узлах. Эти закономерности указывали на то, что tRF-Ser действует как естественный супрессор опухоли, утрачиваемый по мере прогрессирования болезни.
Как tRF-Ser замедляет рост и распространение опухоли
Чтобы выяснить функции tRF-Ser, команда повысила или подавила его уровни в клетках рака желудка, выращенных в лаборатории. При повышении tRF-Ser клетки делились медленнее, образовывали меньше колоний и чаще останавливались на ранней стадии клеточного цикла, до репликации ДНК. Их способность мигрировать и проникать через барьеры также снижалась, а ключевые маркеры эпителиально-мезенхимального перехода (EMT), способствующего расселению опухоли, уменьшались. При понижении tRF-Ser наблюдалось обратное: клетки росли быстрее, становились более инвазивными и проявляли выраженные признаки EMT. У мышей клетки, модифицированные для избыточной продукции tRF-Ser, образовывали меньшие подкожные опухоли и давали меньше метастазов в легких, что подтверждает способность этой маленькой РНК сдерживать рак в живом организме.
Перенастройка стрессовых и путей смерти опухоли
Помимо замедления роста, tRF-Ser направляет раковые клетки к форме клеточной смерти, зависящей от железа и связанной с перекисным окислением липидов — ферроптозу. При обработке индуктором ферроптоза клетки с высоким содержанием tRF-Ser демонстрировали больше оксидативного повреждения, более разрушенные митохондрии и пониженные уровни ключевого защитного фермента GPX4, тогда как при дефиците tRF-Ser наблюдалась противоположная картина. Исследование также изучало реакцию на 5‑фторурацил, стандартный препарат для химиотерапии рака желудка. Клетки с повышенным tRF-Ser легче убивались препаратом, тогда как клетки с низким tRF-Ser были более резистентны. Комбинирование сверхэкспрессии tRF-Ser с 5‑фторурацилом и индуктором ферроптоза давало наибольший противоопухолевый эффект у мышей, сопровождавшийся явными биохимическими признаками усиленного оксидативного повреждения внутри опухолей.
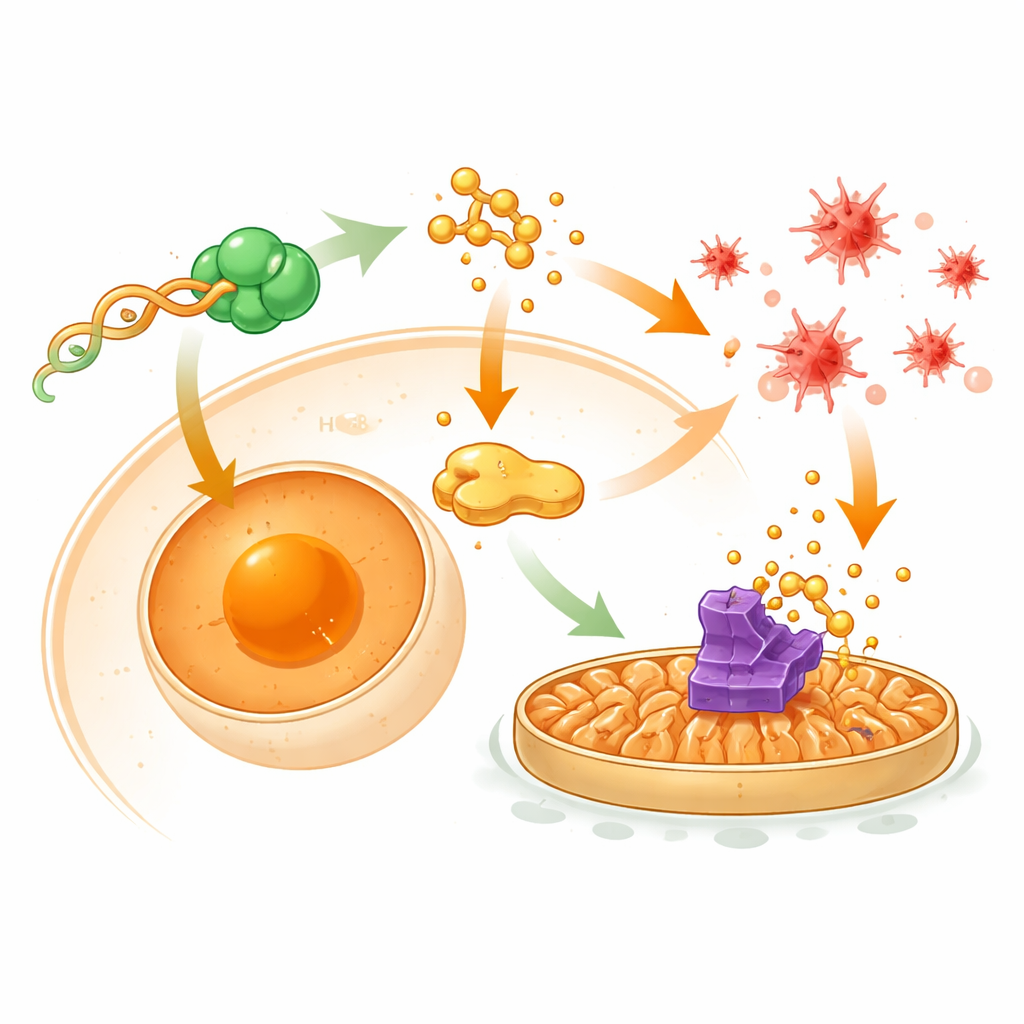
Скрытая управляющая схема внутри опухолевых клеток
Чтобы понять механизмы таких эффектов, исследователи картировали взаимодействия tRF-Ser с белками и последующими генными ответами. Они обнаружили, что tRF-Ser физически связывается с белком, связывающим ДНК, под названием CNBP, и удерживает больше этого белка в цитоплазме, а не в ядре клетки. Когда CNBP попадает в ядро, он обычно активирует ген шаперона HSPA8, который, в свою очередь, помогает поддерживать GPX4 и способствует сигнальным путям EMT через белок β-катенин. Удерживая CNBP вне ядра, tRF-Ser понижает уровни HSPA8, ослабляет транслокацию β-катенина в ядро и позволяет другому белку, STUB1, метить GPX4 для разрушения. Эта каскада одновременно подавляет EMT, связанный с инвазией, и снимает тормоз с ферроптоза, делая раковые клетки более уязвимыми к оксидативному повреждению и химиотерапии.
Что это значит для будущих подходов к лечению
В совокупности работа выявляет компактную регуляторную ось — tRF-Ser, CNBP и HSPA8 — которая связывает рост опухоли, метастатическое поведение, клеточную смерть и чувствительность к лекарствам при раке желудка. Проще говоря, tRF-Ser действует как молекулярный регулировщик движения, отводя фактор, стимулирующий рост (CNBP), от центра управления клетки, чтобы тот не мог включить программу выживания (через HSPA8 и GPX4). Восстановление или имитация действия tRF-Ser либо воздействие на его нисходящие мишени могут повысить эффективность существующих препаратов, таких как 5‑фторурацил, и помочь преодолеть лекарственную устойчивость. Хотя для клинического применения потребуются дополнительные исследования, это исследование подчеркивает, что крошечные фрагменты РНК могут стать ключом к тому, чтобы перевести раковые клетки с выживания на путь самоуничтожения.
Цитирование: Jiao, J., Wang, G., Liu, J. et al. A new candidate tumor suppressor tRF-Ser inhibits gastric cancer progression by regulating the CNBP/HSPA8 axis. Cell Death Dis 17, 379 (2026). https://doi.org/10.1038/s41419-026-08608-1
Ключевые слова: рак желудка, РНК-супрессор опухоли, ферроптоз, химиорезистентность, ось HSPA8 CNBP