Clear Sky Science · fr
Un nouveau candidat suppresseur de tumeur tRF-Ser inhibe la progression du cancer gastrique en régulant l’axe CNBP/HSPA8
Pourquoi c’est important pour le cancer de l’estomac
Le cancer de l’estomac (gastrique) reste l’un des cancers les plus meurtriers dans le monde, en partie parce que les tumeurs résistent souvent à la chimiothérapie et se propagent de manière agressive. Cette étude révèle une défense naturelle jusque‑là inconnue à l’intérieur des cellules gastriques : un tout petit fragment d’ARN appelé tRF‑Ser qui contribue à contenir les tumeurs. En montrant comment cette molécule ralentit la croissance tumorale, favorise une forme de mort cellulaire dépendante du fer et améliore l’efficacité de la chimiothérapie, les chercheurs ouvrent de nouvelles pistes pour traiter des patients dont les tumeurs sont difficiles à contrôler.
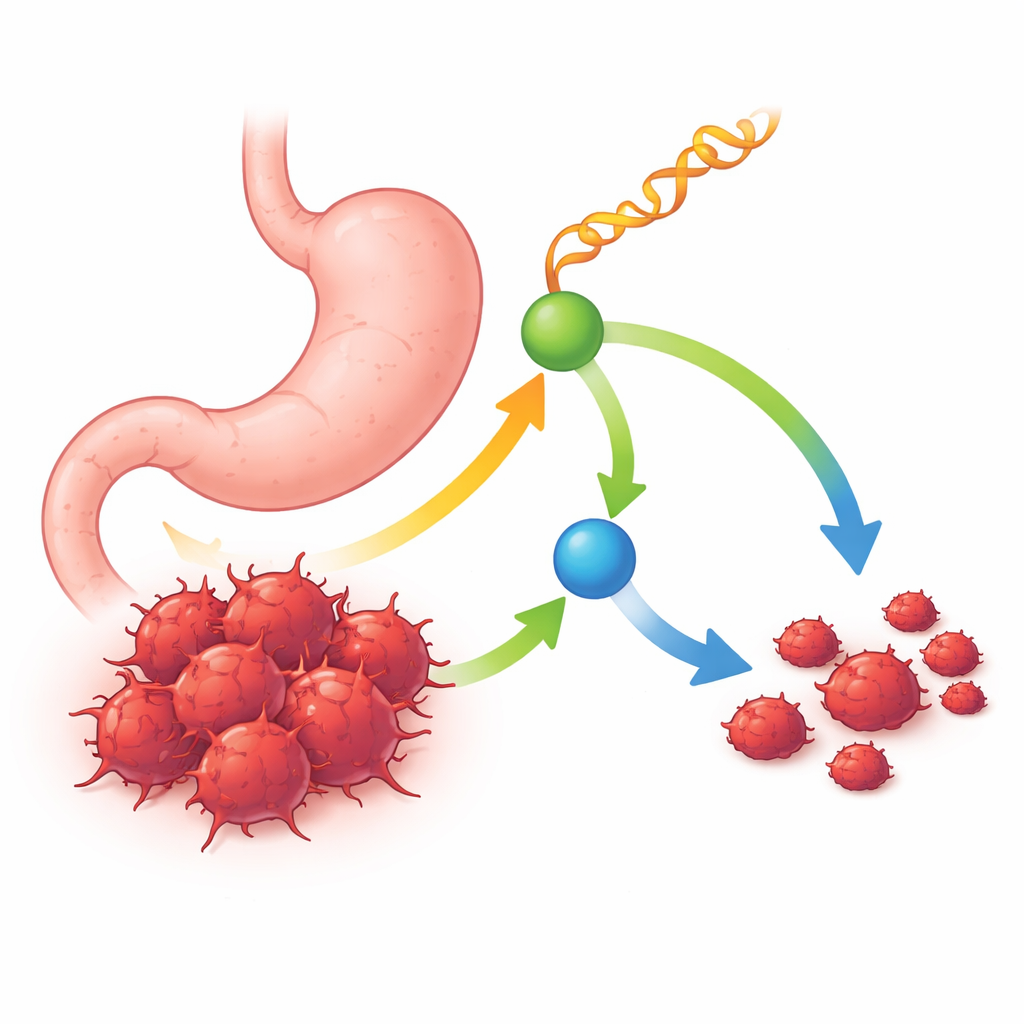
Un petit ARN au grand rôle protecteur
Les chercheurs ont commencé par comparer les petits ARN présents dans des tumeurs gastriques humaines et dans les tissus sains adjacents. Ils se sont intéressés à une classe particulière appelée fragments dérivés de l’ARNt — de courts morceaux coupés à partir des ARN adaptateurs de la synthèse protéique. Parmi de nombreux candidats, un fragment s’est démarqué : tRF‑Ser, systématiquement moins abondant dans les échantillons tumoraux et les lignées de cancer gastrique que dans les tissus normaux. Les patients dont les tumeurs contenaient plus de tRF‑Ser avaient tendance à vivre plus longtemps et présentaient des cancers plus petits, moins avancés et avec moins de métastases ganglionnaires. Ces corrélations suggèrent que tRF‑Ser agit comme un suppresseur tumoral naturel qui est perdu à mesure que la maladie progresse.
Comment le tRF-Ser freine la croissance et la dissémination tumorales
Pour tester la fonction de tRF‑Ser, l’équipe a augmenté ou bloqué son niveau dans des cellules de cancer gastrique cultivées en laboratoire. Lorsqu’on augmentait tRF‑Ser, les cellules cancéreuses se divisaient plus lentement, formaient moins de colonies et étaient plus souvent arrêtées tôt dans le cycle cellulaire, avant la réplication de l’ADN. Leur capacité de migration et d’invasion à travers des membranes diminuait aussi, et les marqueurs clés d’un programme de transition épithélio‑mésenchymateuse (EMT) — qui favorise la dissémination tumorale — baissaient. En réduisant tRF‑Ser, on observait l’effet inverse : les cellules proliféraient plus vite, devenaient plus invasives et présentaient des caractéristiques EMT renforcées. Chez la souris, des cellules tumorales modifiées pour produire davantage de tRF‑Ser formaient des tumeurs sous‑cutanées plus petites et donnaient moins de métastases pulmonaires, confirmant que ce petit ARN peut freiner le cancer in vivo.
Reconfiguration des voies de stress et de mort cellulaire du cancer
Au‑delà d’un simple ralentissement de la croissance, tRF‑Ser pousse les cellules cancéreuses vers une forme de mort cellulaire dépendante du fer et liée aux lipides, appelée ferroptose. Sous traitement par un médicament inducteur de ferroptose, les cellules riches en tRF‑Ser présentaient davantage de dommages oxydatifs, des mitochondries plus perturbées et des niveaux plus faibles d’une enzyme protectrice clé, GPX4, alors qu’un profil opposé apparaissait lorsque tRF‑Ser était faible. L’étude a également examiné la réponse au 5‑fluorouracile, une chimiothérapie standard pour le cancer gastrique. Les cellules contenant plus de tRF‑Ser étaient plus sensibles au médicament, tandis que celles en contenant moins étaient plus résistantes. La combinaison de la surexpression de tRF‑Ser avec le 5‑fluorouracile et un inducteur de ferroptose a produit les effets anti‑tumoraux les plus puissants chez la souris, accompagnés de signes biochimiques nets d’un stress oxydatif accru au sein des tumeurs.
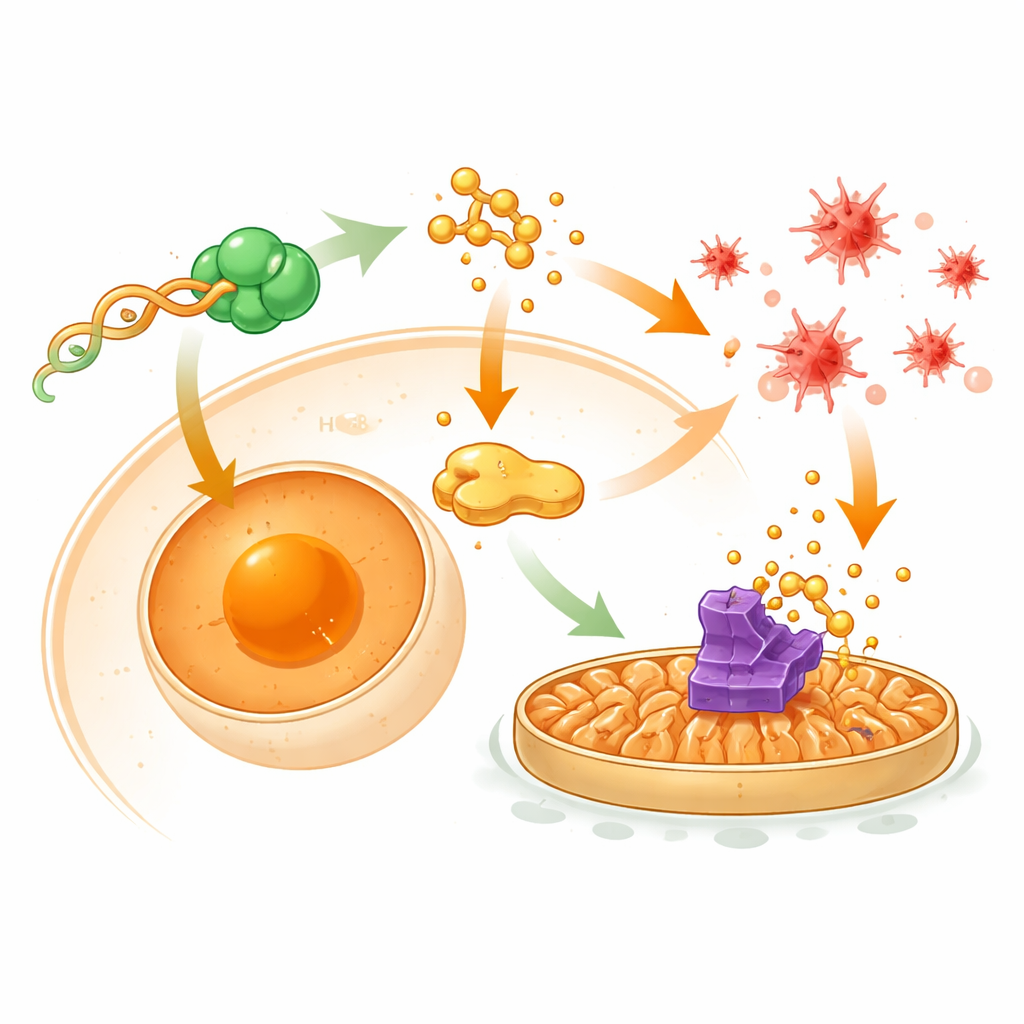
Le circuit de contrôle caché à l’intérieur des cellules tumorales
Pour comprendre le câblage sous‑jacent à ces effets, les chercheurs ont cartographié les interactions de tRF‑Ser avec des protéines et des gènes en aval. Ils ont découvert que tRF‑Ser se lie physiquement à une protéine de liaison à l’ADN appelée CNBP et la retient davantage dans le cytoplasme plutôt que dans le noyau. Quand CNBP atteint le noyau, il active normalement un gène chaperon nommé HSPA8, qui à son tour contribue au maintien de GPX4 et soutient des signaux promoteurs d’EMT impliquant la protéine β‑caténine. En empêchant CNBP d’entrer dans le noyau, tRF‑Ser abaisse les niveaux de HSPA8, affaiblit la translocation nucléaire de la β‑caténine et permet à une autre protéine, STUB1, d’étiqueter GPX4 pour sa destruction. Cette cascade réduit simultanément l’EMT liée à l’invasion et retire un frein à la ferroptose, rendant les cellules cancéreuses plus vulnérables aux dommages oxydatifs et à la chimiothérapie.
Implications pour les traitements futurs
Dans l’ensemble, ce travail révèle un axe régulateur compact — tRF‑Ser, CNBP et HSPA8 — qui relie la croissance tumorale, le comportement métastatique, la mort cellulaire et la réponse aux médicaments dans le cancer gastrique. Concrètement, tRF‑Ser agit comme un agent de circulation moléculaire, détournant un facteur pro‑croissance (CNBP) loin du centre de contrôle de la cellule pour l’empêcher d’activer un programme de survie (via HSPA8 et GPX4). Restaurer ou imiter tRF‑Ser, ou cibler ses partenaires en aval, pourrait ainsi rendre des médicaments existants comme le 5‑fluorouracile plus efficaces et contribuer à surmonter la résistance aux traitements. Bien que des travaux supplémentaires soient nécessaires avant une utilisation clinique, cette étude met en lumière comment de minuscules fragments d’ARN peuvent contenir les clés pour faire basculer les cellules cancéreuses de la survie vers l’autodestruction.
Citation: Jiao, J., Wang, G., Liu, J. et al. A new candidate tumor suppressor tRF-Ser inhibits gastric cancer progression by regulating the CNBP/HSPA8 axis. Cell Death Dis 17, 379 (2026). https://doi.org/10.1038/s41419-026-08608-1
Mots-clés: cancer de l’estomac, ARN suppresseur de tumeur, ferroptose, résistance aux chimiothérapies, axe HSPA8 CNBP