Clear Sky Science · sv
En ny kandidat till tumörsuppressor tRF-Ser hämmar magscancerprogression genom att reglera CNBP/HSPA8‑axeln
Varför detta är viktigt för magsäckscancer
Magsäckscancer (gastric cancer) är fortfarande en av de dödligaste cancerformerna globalt, delvis eftersom tumörer ofta blir resistenta mot kemoterapi och sprider sig aggressivt. Denna studie avslöjar ett tidigare okänt naturligt försvar i magsäcksceller: en liten RNA‑fragment kallad tRF-Ser som hjälper till att hålla tumörer i schack. Genom att visa hur denna molekyl bromsar cancerutveckling, främjar en järn‑driven form av celldöd och gör kemoterapi mer effektiv, pekar forskningen mot nya strategier för att behandla patienter vars tumörer är svåra att kontrollera.
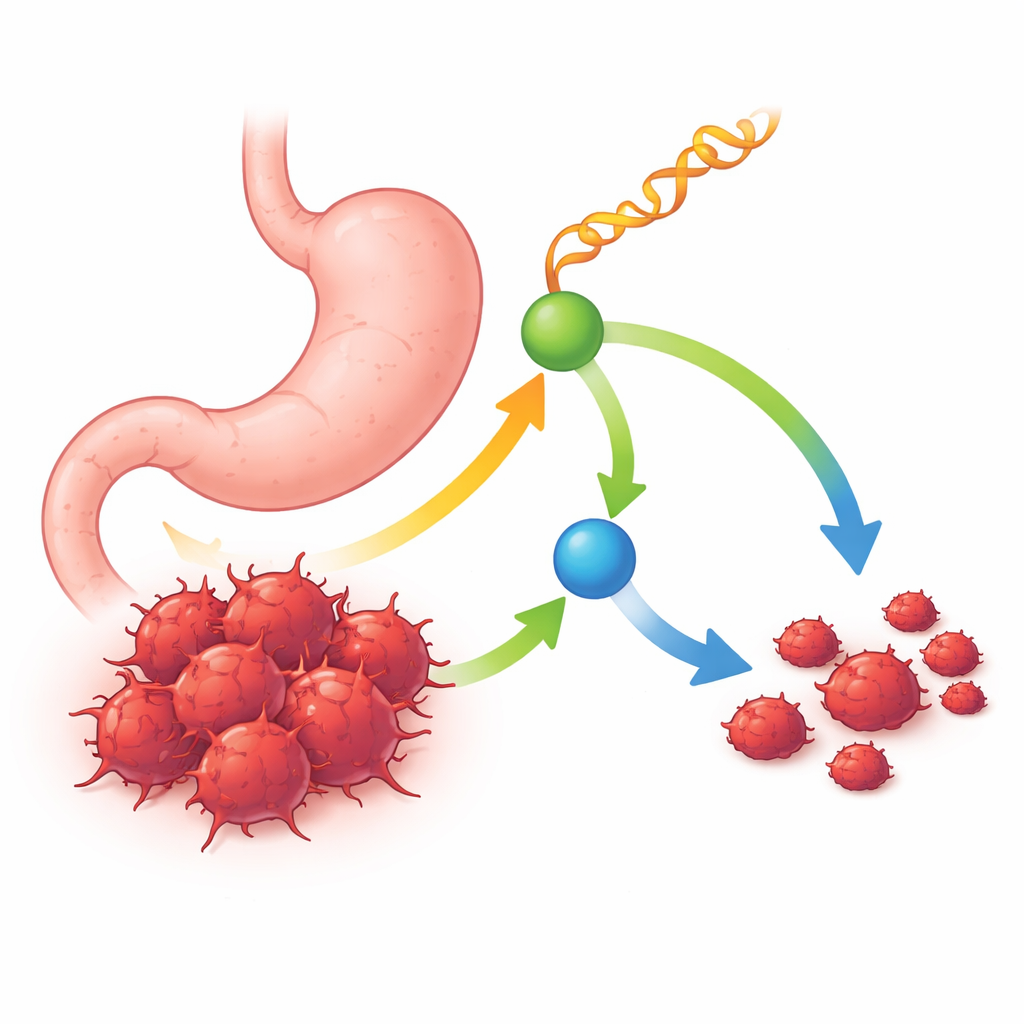
En liten RNA med en stor skyddande roll
Forskarna började med att jämföra små RNA‑molekyler i mänskliga magtumörer och intilliggande frisk vävnad. De fokuserade på en särskild klass kallad tRNA‑ härledda fragment — korta bitar klippta från cellens adapter‑RNA för proteinsyntes. Bland många kandidater framstod ett fragment tydligt: tRF-Ser, som konsekvent var lägre i tumörprover och i cellinjer från magsäckscancer än i normal vävnad. Patienter vars tumörer hade mer tRF-Ser tenderade att leva längre och hade mindre, mindre avancerade tumörer med färre lymfkörtelmetastaser. Dessa mönster föreslog att tRF-Ser fungerar som en naturlig tumörsuppressor som förloras när sjukdomen förvärras.
Hur tRF-Ser bromsar tumörtillväxt och spridning
För att testa vad tRF-Ser faktiskt gör ökade eller blockerade teamet dess nivåer i magsäckscellinjer odlad i laboratoriet. När tRF-Ser ökade delade cancercellerna sig långsammare, bildade färre kolonier och stoppades oftare tidigt i cellcykeln innan DNA‑kopiering. Deras förmåga att migrera och invadera genom membran minskade också, och viktiga markörer för ett formändrande program kallat epitel‑mesenkymal transition (EMT) — som hjälper tumörer att sprida sig — sjönk. När tRF-Ser minskades skedde motsatsen: cellerna växte snabbare, blev mer invasiva och visade tydligare EMT‑drag. I möss bildade tumörceller konstruerade för att producera extra tRF-Ser mindre subkutana tumörer och färre lungmetastaser, vilket bekräftade att detta lilla RNA kan begränsa cancer i levande organismer.
Omskrivning av cancerns stress‑ och döds‑vägar
Bortom att bara bromsa tillväxt driver tRF-Ser cancerceller mot en form av järnberoende, lipiddriven celldöd känd som ferroptos. Vid behandling med ett ferroptosframkallande läkemedel visade celler med mycket tRF-Ser mer oxidativ skada, mer störda mitokondrier och lägre nivåer av ett nyckelprotektivt enzym kallat GPX4, medan motsatt mönster uppträdde när tRF-Ser var knapp. Studien undersökte också svar på 5‑fluorouracil, en standardkemoterapi för magsäckscancer. Celler med mer tRF-Ser dödades lättare av läkemedlet, medan celler med mindre tRF-Ser var mer resistenta. Kombinationen av tRF-Ser‑överuttryck med både 5‑fluorouracil och en ferroptosinducer gav de starkaste tumör‑förminskande effekterna i möss, tillsammans med tydliga biokemiska tecken på förhöjd oxidativ skada inne i tumörerna.
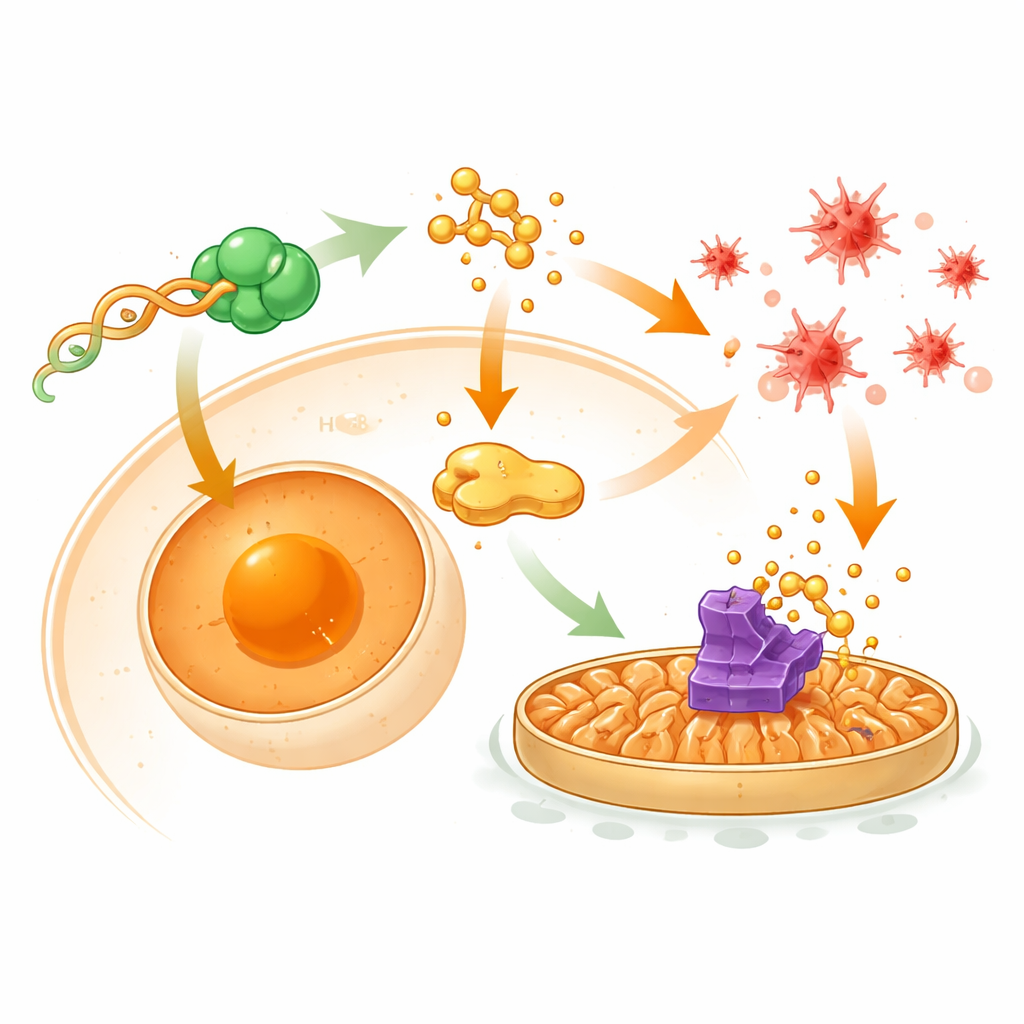
Den dolda styrkretsen inne i tumörceller
För att förstå kopplingarna bakom dessa effekter kartlade forskarna hur tRF-Ser interagerar med proteiner och nedströmsgener. De fann att tRF-Ser fysiskt binder ett DNA‑bindande protein kallat CNBP och håller mer av det fast i cytoplasman istället för i kärnan. När CNBP når kärnan aktiverar det normalt ett chaperon‑gen som heter HSPA8, vilket i sin tur hjälper till att bibehålla GPX4 och stöder EMT‑drivande signaler som involverar proteinet β‑catenin. Genom att hålla CNBP utanför kärnan sänker tRF-Ser HSPA8‑nivåerna, försvagar β‑catenins förflyttning in i kärnan och tillåter ett annat protein, STUB1, att märka GPX4 för nedbrytning. Denna kaskad dämpar samtidigt invasion‑kopplad EMT och tar bort en broms på ferroptos, vilket gör cancerceller mer sårbara för oxidativ skada och kemoterapi.
Vad detta betyder för framtida behandlingar
Tillsammans avslöjar arbetet en kompakt regleringsaxel — tRF-Ser, CNBP och HSPA8 — som binder samman tumörtillväxt, metastatisk beteende, celldöd och läkemedelssvar i magsäckscancer. I vardagliga termer agerar tRF-Ser som en molekylär trafikpolis som avleder en tillväxtfrämjande faktor (CNBP) från cellens kontrollcenter så att den inte kan slå på ett överlevnadsprogram (via HSPA8 och GPX4). Återställande eller efterbildning av tRF-Ser, eller inriktning på dess nedströmsparter, skulle därför kunna göra befintliga läkemedel som 5‑fluorouracil mer effektiva och hjälpa till att övervinna behandlingresistens. Även om vidare arbete krävs innan klinisk användning, understryker denna studie hur små RNA‑bitar kan innehålla nycklarna för att få cancerceller att gå från överlevnad till självförstörelse.
Citering: Jiao, J., Wang, G., Liu, J. et al. A new candidate tumor suppressor tRF-Ser inhibits gastric cancer progression by regulating the CNBP/HSPA8 axis. Cell Death Dis 17, 379 (2026). https://doi.org/10.1038/s41419-026-08608-1
Nyckelord: magsäckscancer, tumörsuppressor-RNA, ferroptos, kemoresistens, HSPA8 CNBP-axel