Clear Sky Science · es
Un nuevo candidato a supresor tumoral tRF-Ser inhibe la progresión del cáncer gástrico regulando el eje CNBP/HSPA8
Por qué esto importa para el cáncer de estómago
El cáncer de estómago (gástrico) sigue siendo uno de los cánceres más letales del mundo, en parte porque los tumores a menudo resisten la quimioterapia y se diseminan de forma agresiva. Este estudio descubre una defensa natural hasta ahora desconocida dentro de las células gástricas: un fragmento de ARN diminuto llamado tRF-Ser que ayuda a mantener los tumores bajo control. Al mostrar cómo esta molécula ralentiza el crecimiento tumoral, fomenta una forma de muerte celular dependiente del hierro y mejora la eficacia de la quimioterapia, la investigación apunta a nuevas estrategias para tratar a pacientes cuyos tumores son difíciles de controlar.
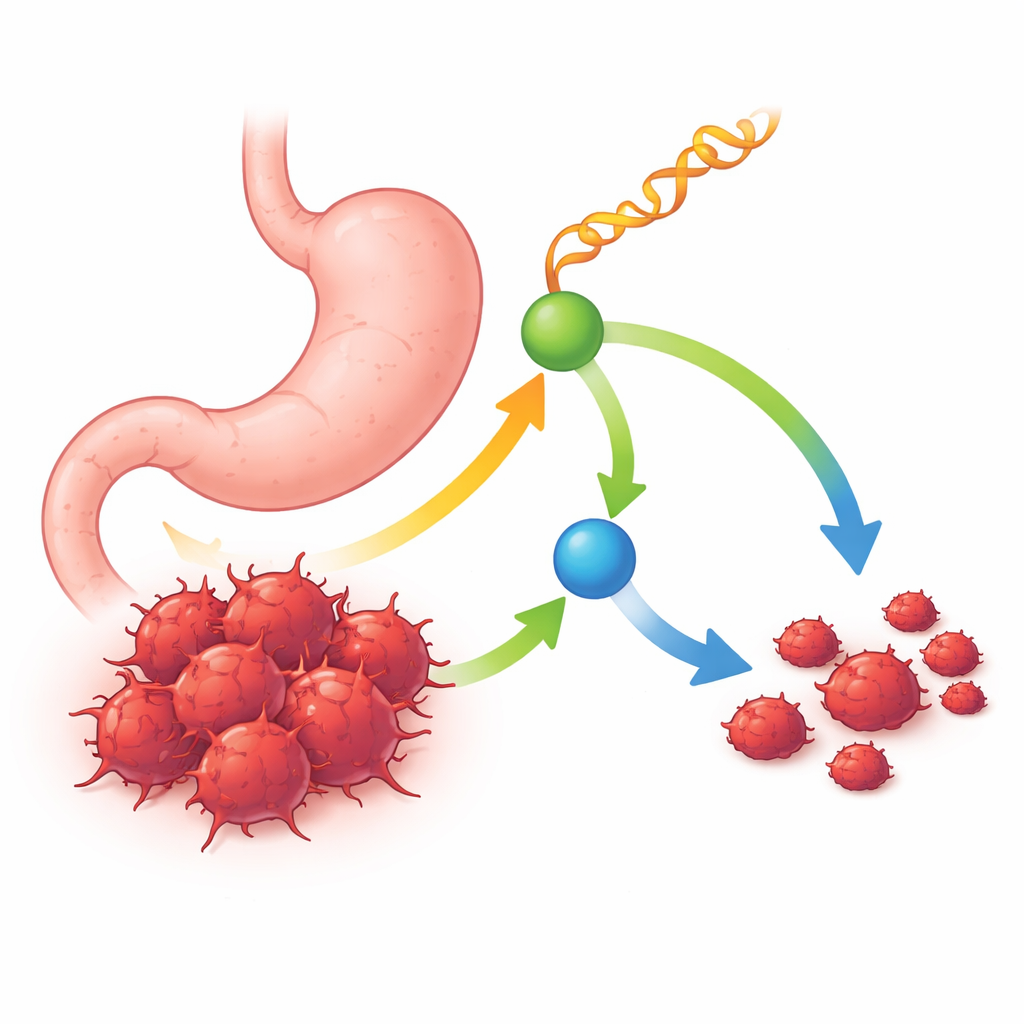
Un ARN pequeño con un gran papel protector
Los investigadores empezaron comparando las pequeñas moléculas de ARN en tumores gástricos humanos y en tejido sano vecino. Se centraron en una clase especial llamada fragmentos derivados de ARNt: piezas cortas cortadas de los ARNt, los adaptadores de la célula para la síntesis de proteínas. Entre muchos candidatos, destacó un fragmento: tRF-Ser, que resultó consistentemente más bajo en muestras tumorales y en líneas celulares de cáncer gástrico que en tejido normal. Los pacientes cuyos tumores contenían más tRF-Ser tendían a vivir más tiempo y presentaban tumores más pequeños, menos avanzados y con menos metástasis en ganglios linfáticos. Estos patrones sugirieron que tRF-Ser actúa como un supresor tumoral natural que se pierde a medida que la enfermedad empeora.
Cómo tRF-Ser frena el crecimiento y la diseminación tumoral
Para comprobar qué hace realmente tRF-Ser, el equipo aumentó o bloqueó sus niveles en células de cáncer gástrico cultivadas en el laboratorio. Cuando se incrementó tRF-Ser, las células cancerosas se dividían más lentamente, formaban menos colonias y tendían a detenerse antes en el ciclo celular, antes de copiar su ADN. También se redujo su capacidad de migrar e invadir a través de membranas, y disminuyeron marcadores clave de un programa de cambio de forma llamado transición epitelio‑mesénquima (EMT), que ayuda a la diseminación tumoral. Cuando tRF-Ser se redujo, ocurrió lo contrario: las células crecieron más rápido, se volvieron más invasivas y mostraron rasgos de EMT más marcados. En ratones, las células tumorales modificadas para producir tRF-Ser adicional formaron tumores subcutáneos más pequeños y menos metástasis pulmonares, confirmando que este pequeño ARN puede frenar el cáncer en organismos vivos.
Reconectando las vías de estrés y muerte celular del cáncer
Más allá de simplemente ralentizar el crecimiento, tRF-Ser empuja a las células cancerosas hacia una forma de muerte celular dependiente del hierro y mediada por lípidos conocida como ferroptosis. Bajo tratamiento con un fármaco que induce ferroptosis, las células ricas en tRF-Ser mostraron más daño oxidativo, mitocondrias más alteradas y niveles más bajos de una enzima protectora clave llamada GPX4, mientras que cuando tRF-Ser era escaso apareció el patrón contrario. El estudio también analizó la respuesta al 5‑fluorouracilo, una quimioterapia estándar para el cáncer gástrico. Las células con más tRF-Ser eran más fácilmente eliminadas por el fármaco, mientras que las células con menos tRF-Ser eran más resistentes. La combinación de sobreexpresión de tRF-Ser con 5‑fluorouracilo y un inductor de ferroptosis produjo los efectos reductores de tumor más fuertes en ratones, junto con claras señales bioquímicas de mayor daño oxidativo dentro de los tumores.
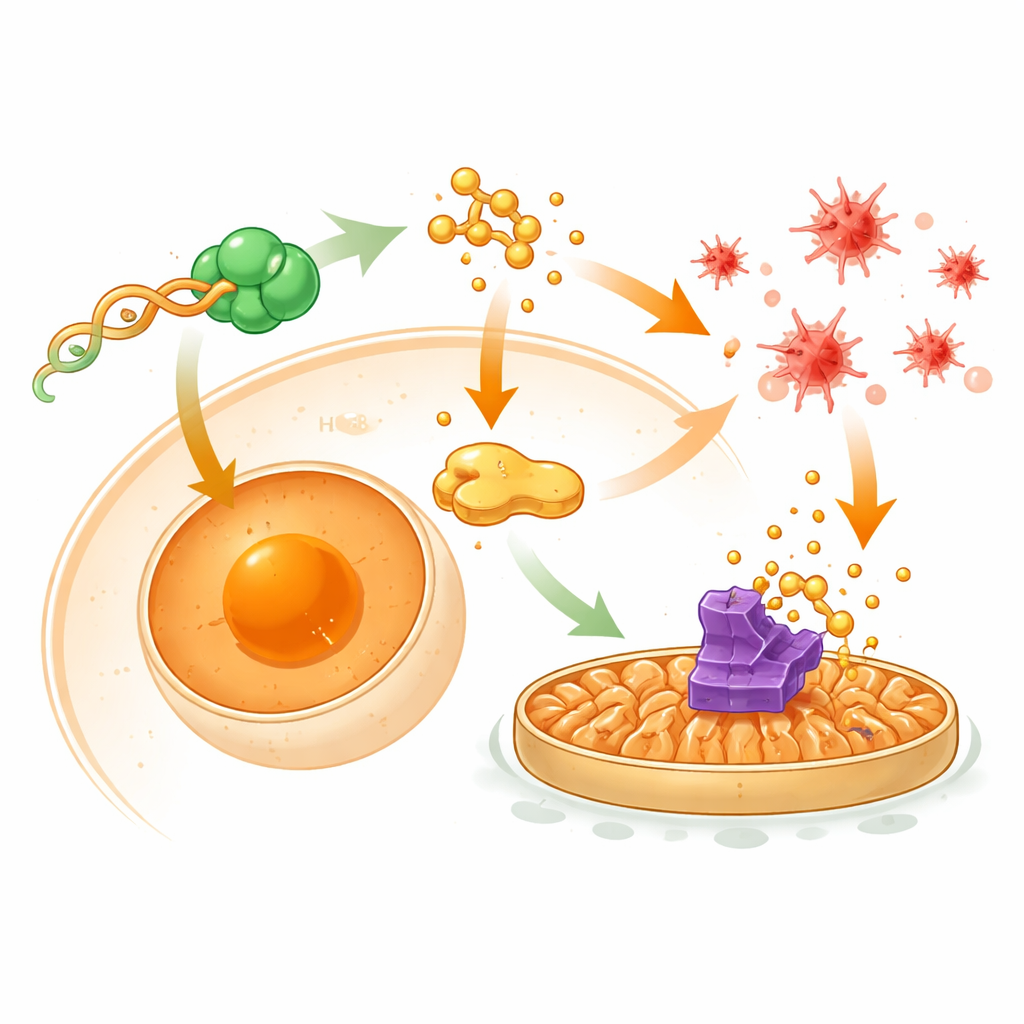
El circuito de control oculto dentro de las células tumorales
Para entender el cableado detrás de estos efectos, los investigadores mapearon cómo tRF-Ser interactúa con proteínas y genes downstream. Descubrieron que tRF-Ser se une físicamente a una proteína que se fija al ADN llamada CNBP y mantiene más CNBP atrapada en el citoplasma en lugar de en el núcleo. Cuando CNBP llega al núcleo, normalmente activa un gen chaperona llamado HSPA8, que a su vez ayuda a mantener GPX4 y sostiene señales promotoras de EMT que involucran la proteína β‑catenina. Al retener CNBP fuera del núcleo, tRF-Ser reduce los niveles de HSPA8, debilita el traslado de β‑catenina al núcleo y permite que otra proteína, STUB1, marque a GPX4 para su destrucción. Esta cascada reduce simultáneamente la EMT vinculada a la invasión y elimina una barrera contra la ferroptosis, haciendo a las células cancerosas más vulnerables al daño oxidativo y a la quimioterapia.
Qué significa esto para futuros tratamientos
En conjunto, el trabajo revela un eje regulador compacto —tRF-Ser, CNBP y HSPA8— que conecta crecimiento tumoral, comportamiento metastásico, muerte celular y respuesta a fármacos en el cáncer gástrico. En términos cotidianos, tRF-Ser actúa como un agente de tráfico molecular, desviando un factor promotor del crecimiento (CNBP) lejos del centro de control celular para que no pueda activar un programa de supervivencia (a través de HSPA8 y GPX4). Restaurar o imitar a tRF-Ser, o dirigirse a sus asociados downstream, podría por tanto aumentar la eficacia de fármacos existentes como el 5‑fluorouracilo y ayudar a superar la resistencia al tratamiento. Aunque se necesita más trabajo antes de la aplicación clínica, este estudio destaca cómo fragmentos diminutos de ARN pueden contener las claves para inclinar a las células cancerosas desde la supervivencia hacia la autodestrucción.
Cita: Jiao, J., Wang, G., Liu, J. et al. A new candidate tumor suppressor tRF-Ser inhibits gastric cancer progression by regulating the CNBP/HSPA8 axis. Cell Death Dis 17, 379 (2026). https://doi.org/10.1038/s41419-026-08608-1
Palabras clave: cáncer gástrico, ARN supresor tumoral, ferroptosis, resistencia a la quimioterapia, eje HSPA8 CNBP