Clear Sky Science · it
Un nuovo candidato oncosoppressore tRF-Ser inibisce la progressione del cancro gastrico regolando l’asse CNBP/HSPA8
Perché questo è importante per il cancro allo stomaco
Il cancro dello stomaco (gastrico) resta uno dei tumori più letali al mondo, in parte perché i tumori spesso resistono alla chemioterapia e si diffondono in modo aggressivo. Questo studio svela una difesa naturale precedentemente sconosciuta nelle cellule gastriche: un piccolo frammento di RNA chiamato tRF-Ser che aiuta a tenere sotto controllo i tumori. Dimostrando come questa molecola rallenta la crescita tumorale, favorisce una forma di morte cellulare guidata dal ferro e rende la chemioterapia più efficace, la ricerca indica nuove strategie per trattare pazienti i cui tumori sono difficili da controllare.
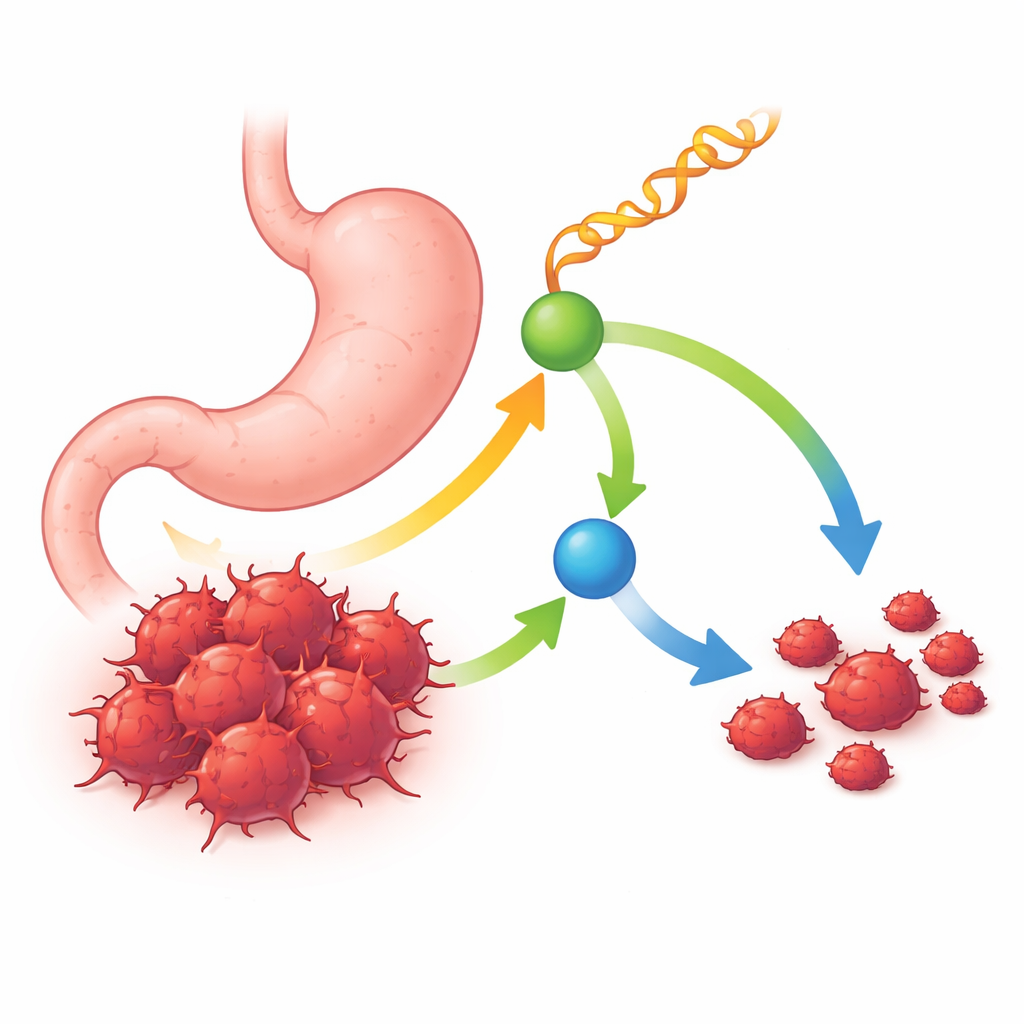
Un piccolo RNA con un grande ruolo protettivo
I ricercatori hanno iniziato confrontando le piccole molecole di RNA nei tumori gastrici umani e nel tessuto sano adiacente. Si sono concentrati su una classe speciale chiamata frammenti derivati da tRNA—brevi pezzi ricavati dagli RNA adattatori che costruiscono le proteine. Tra molti candidati, è emerso un frammento: tRF-Ser, che risultava costantemente più basso nei campioni tumorali e nelle linee cellulari del cancro gastrico rispetto al tessuto normale. I pazienti i cui tumori contenevano più tRF-Ser tendevano a vivere più a lungo e presentavano tumori più piccoli, meno avanzati e con meno metastasi linfonodali. Questi schemi suggerivano che tRF-Ser agisca come un oncosoppressore naturale che si perde con l’aggravarsi della malattia.
Come tRF-Ser rallenta crescita e diffusione del tumore
Per verificare cosa faccia realmente tRF-Ser, il gruppo ha aumentato o bloccato i suoi livelli in cellule di cancro gastrico coltivate in laboratorio. Quando tRF-Ser veniva incrementato, le cellule tumorali si dividevano più lentamente, formavano meno colonie e presentavano un arresto precoce del ciclo cellulare, prima della duplicazione del DNA. Anche la loro capacità di migrare e invadere membrane era ridotta, e marcatori chiave del programma di transizione epitelio-mesenchimale (EMT)—che favorisce la diffusione tumorale—calavano. Quando tRF-Ser veniva ridotto, accadeva l’opposto: le cellule crescevano più rapidamente, diventavano più invasive e mostravano caratteristiche EMT più marcate. Nei topi, cellule tumorali ingegnerizzate per produrre più tRF-Ser formavano tumori sottocutanei più piccoli e meno metastasi polmonari, confermando che questo piccolo RNA può limitare il cancro in organismi vivi.
Riprogrammare le vie dello stress e della morte cellulare nei tumori
Oltre a rallentare la crescita, tRF-Ser spinge le cellule tumorali verso una forma di morte cellulare dipendente dal ferro e guidata dai lipidi nota come ferroptosi. Sotto trattamento con un farmaco che induce ferroptosi, le cellule ricche di tRF-Ser mostravano più danno ossidativo, mitocondri più compromessi e livelli più bassi di un enzima protettivo chiave chiamato GPX4, mentre uno schema opposto appariva quando tRF-Ser era scarso. Lo studio ha anche analizzato le risposte al 5-fluorouracile, una chemioterapia standard per il cancro gastrico. Le cellule con più tRF-Ser erano più facilmente uccise dal farmaco, mentre quelle con meno tRF-Ser risultavano più resistenti. La sovraespressione di tRF-Ser combinata con 5-fluorouracile e un induttore di ferroptosi ha prodotto gli effetti più marcati di riduzione tumorale nei topi, insieme a chiari segni biochimici di aumento del danno ossidativo all’interno dei tumori.
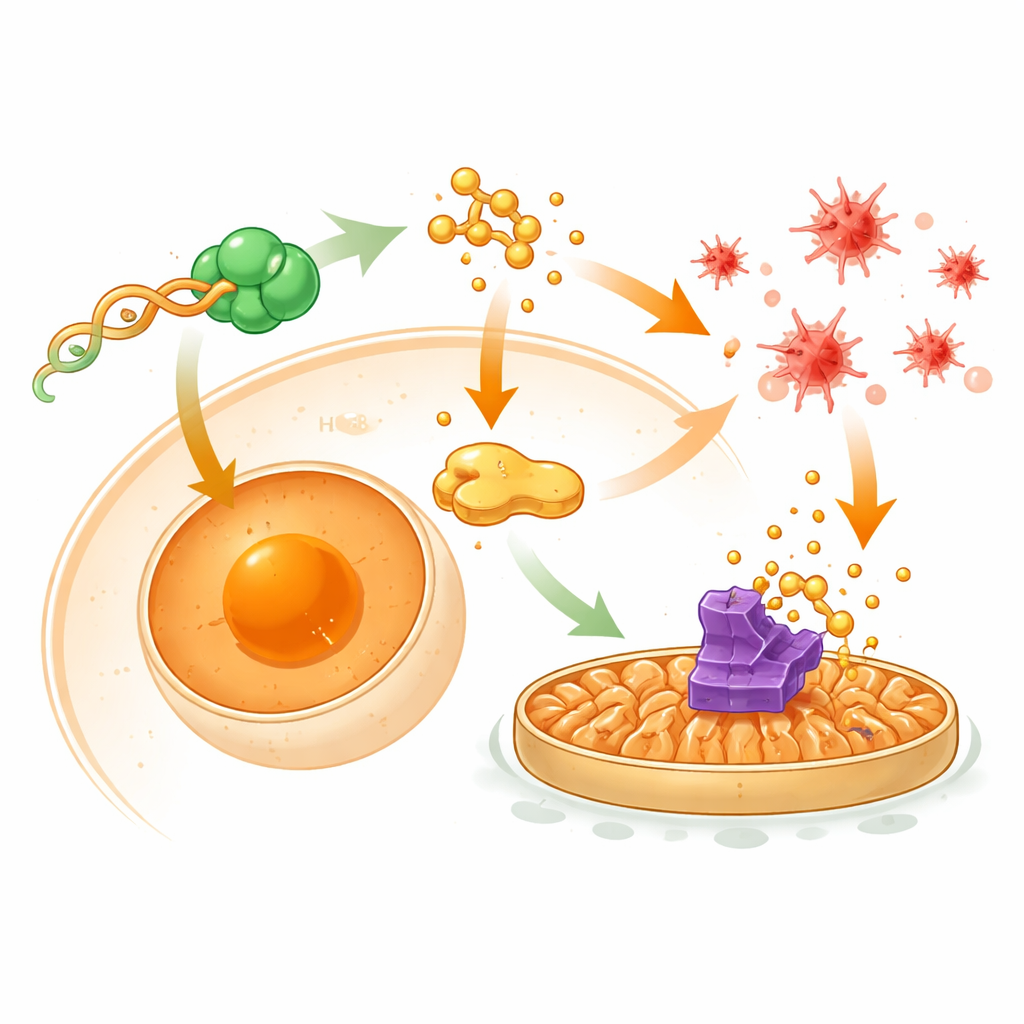
Il circuito di controllo nascosto nelle cellule tumorali
Per comprendere il cablaggio dietro questi effetti, i ricercatori hanno mappato come tRF-Ser interagisce con proteine e geni a valle. Hanno scoperto che tRF-Ser si lega fisicamente a una proteina legante il DNA chiamata CNBP e favorisce il suo sequestro nel citoplasma anziché nel nucleo. Quando CNBP raggiunge il nucleo, normalmente attiva un gene chaperone chiamato HSPA8, che a sua volta contribuisce a mantenere GPX4 e sostiene segnali EMT guidati dalla proteina β-catenina. Trattenendo CNBP fuori dal nucleo, tRF-Ser riduce i livelli di HSPA8, indebolisce il trasporto di β-catenina nel nucleo e permette a un’altra proteina, STUB1, di marcare GPX4 per la degradazione. Questa cascata attenua contemporaneamente l’EMT associata all’invasione e rimuove un freno sulla ferroptosi, rendendo le cellule tumorali più vulnerabili al danno ossidativo e alla chemioterapia.
Cosa significa per i trattamenti futuri
Complessivamente, il lavoro rivela un asse regolatorio compatto—tRF-Ser, CNBP e HSPA8—that mette in relazione crescita tumorale, comportamento metastatico, morte cellulare e risposta ai farmaci nel cancro gastrico. In termini pratici, tRF-Ser funziona come un agente di traffico molecolare, deviando un fattore pro-crescita (CNBP) lontano dal centro di controllo della cellula in modo che non possa attivare un programma di sopravvivenza (tramite HSPA8 e GPX4). Ripristinare o mimare tRF-Ser, o colpire i suoi partner a valle, potrebbe quindi rendere farmaci esistenti come il 5-fluorouracile più efficaci e aiutare a superare la resistenza al trattamento. Pur richiedendo ulteriori studi prima dell’uso clinico, questo lavoro evidenzia come piccoli frammenti di RNA possano contenere le chiavi per spingere le cellule tumorali dalla sopravvivenza verso l’autodistruzione.
Citazione: Jiao, J., Wang, G., Liu, J. et al. A new candidate tumor suppressor tRF-Ser inhibits gastric cancer progression by regulating the CNBP/HSPA8 axis. Cell Death Dis 17, 379 (2026). https://doi.org/10.1038/s41419-026-08608-1
Parole chiave: cancro gastrico, RNA oncosoppressore, ferroptosi, resistenza chemioterapica, asse HSPA8 CNBP