Clear Sky Science · tr
Mide kanserinin ilerlemesini CNBP/HSPA8 eksenini düzenleyerek engelleyen yeni bir aday tümör baskılayıcısı tRF-Ser
Mide kanseri için neden önemli
Mide (gastric) kanseri, tümörlerin sıklıkla kemoterapiye direnç göstermesi ve agresifçe yayılması nedeniyle dünya çapında en ölümcül kanserlerden biri olmaya devam ediyor. Bu çalışma, mide hücreleri içinde daha önce bilinmeyen doğal bir savunmayı ortaya koyuyor: tümörleri kontrol altında tutmaya yardımcı olan küçük bir RNA parçacığı olan tRF-Ser. Bu molekülün kanser büyümesini nasıl yavaşlattığını, demir kaynaklı bir hücre ölümü biçimini nasıl teşvik ettiğini ve kemoterapinin etkinliğini nasıl artırdığını göstererek, kontrolü zor tümörleri olan hastaların tedavisine yönelik yeni stratejilere işaret ediyor.
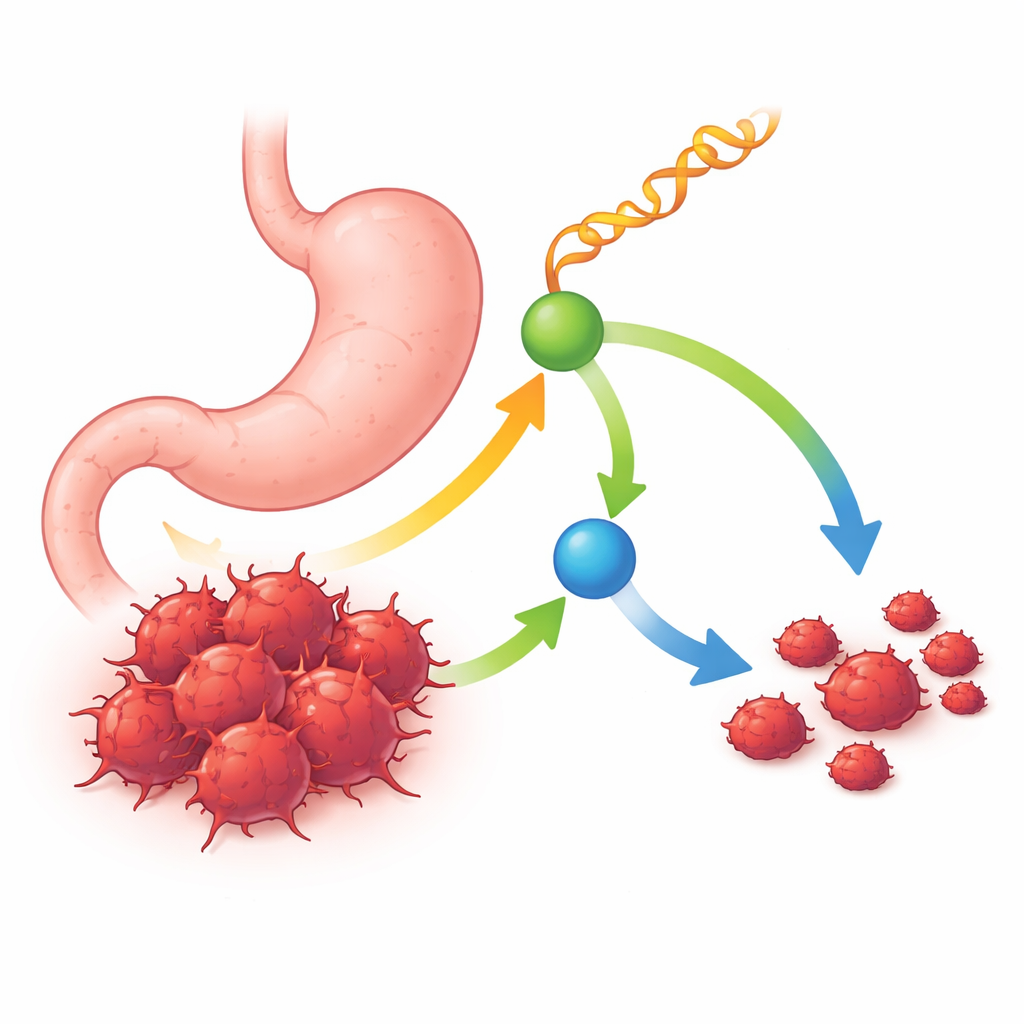
Büyük koruyucu role sahip küçük bir RNA
Araştırmacılar, insan mide tümörlerindeki ve çevrelerindeki sağlıklı dokulardaki küçük RNA moleküllerini karşılaştırarak işe başladılar. Hücrenin protein üretiminde görev alan adaptör RNA'lardan kesilen kısa parçalar olan tRNA kaynaklı fragmanlar adlı özel bir sınıfa odaklandılar. Birçok aday arasından öne çıkan bir fragman vardı: tRF-Ser; tümör örneklerinde ve mide kanseri hücre hatlarında normal dokuya kıyasla tutarlı şekilde daha düşük bulundu. Tümörlerinde daha fazla tRF-Ser olan hastalar genellikle daha uzun yaşamış ve daha küçük, daha az ilerlemiş tümörlere ve daha az lenf düğümü metastazına sahipti. Bu desenler, tRF-Ser'in hastalık kötüleştikçe kaybolan doğal bir tümör baskılayıcı gibi davrandığını düşündürdü.
tRF-Ser tümör büyümesini ve yayılmasını nasıl yavaşlatıyor
tRF-Ser'in gerçekte ne yaptığını test etmek için ekip, laboratuvarda büyütülen mide kanseri hücrelerinde bu molekülün düzeylerini artırdı veya engelledi. tRF-Ser artırıldığında, kanser hücreleri daha yavaş bölündü, daha az koloni oluşturdu ve DNA kopyalanmadan önce hücre döngüsünde erken aşamada durmaya daha yatkın hale geldi. Göç ve membranları delme yetenekleri de azaldı ve tümörlerin yayılmasına yardımcı olan epitel‑mezenkimal dönüşüm (EMT) adlı şekil değiştirme programının önemli belirteçleri düştü. tRF-Ser azaltıldığında ise tersine ilişkili etkiler görüldü: hücreler daha hızlı büyüdü, daha invazif hale geldi ve daha güçlü EMT özellikleri sergiledi. Farelerde, ek tRF-Ser üreten şekilde değiştirilmiş tümör hücreleri daha küçük subkutan tümörler ve daha az akciğer metastazı oluşturdu; bu da bu küçük RNA'nın canlı organizmalarda kanseri sınırlayabildiğini doğruladı.
Kanserin stres ve ölüm yollarını yeniden kablolamak
Sadece büyümeyi yavaşlatmanın ötesinde, tRF-Ser kanser hücrelerini ferroptoz olarak bilinen demir bağımlı, lipid kaynaklı bir hücre ölüm biçimine yönlendiriyor. Ferroptoz tetikleyici bir ilaçla tedavi altında, tRF-Ser açısından zengin hücreler daha fazla oksidatif hasar, daha bozulmuş mitokondriler ve GPX4 adlı önemli koruyucu bir enzimin daha düşük düzeylerini gösterdi; tRF-Ser az olduğunda ise tersine bir desen ortaya çıktı. Çalışma ayrıca mide kanseri için standart bir kemoterapi olan 5‑florourasil'e yanıtları inceledi. Daha fazla tRF-Ser'e sahip hücreler ilaçla daha kolay öldürülürken, tRF-Ser'i daha az olan hücreler daha dirençliydi. tRF-Ser aşırı ekspresyonunu hem 5‑florourasil hem de bir ferroptoz indükleyicisi ile birleştirmek, farelerde en güçlü tümör küçülme etkilerini üretti ve tümörlerin içinde artmış oksidatif hasara dair belirgin biyokimyasal işaretler ortaya koydu.
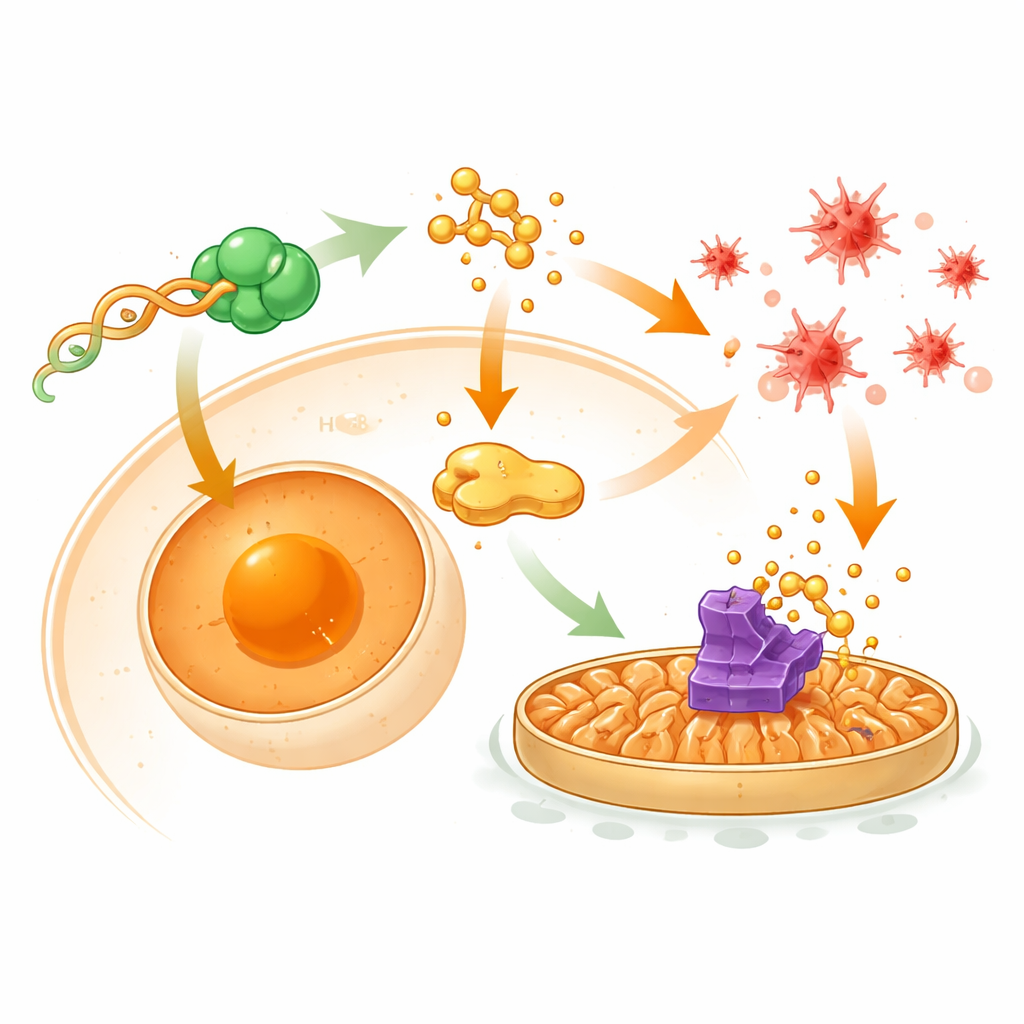
Tümör hücreleri içindeki gizli kontrol devresi
Bu etkilerin ardındaki bağlantıları anlamak için araştırmacılar tRF-Ser'in proteinlerle ve aşağı akış genlerle nasıl etkileştiğini haritaladı. tRF-Ser'in CNBP adı verilen bir DNA-bağlayıcı proteinle fiziksel olarak bağlandığını ve onu çekirdek yerine hücre sitoplazmasında daha fazla tutulmuş halde tuttuğunu buldular. CNBP çekirdeğe ulaştığında normalde HSPA8 adlı bir şaperon genini etkinleştirir; HSPA8 ise GPX4'ü korumaya yardımcı olur ve β‑katenin'i içeren EMT'yi tetikleyen sinyalleri destekler. tRF-Ser CNBP'yi çekirdek dışında tutarak HSPA8 düzeylerini düşürüyor, β‑katenin'in çekirdeğe geçişini zayıflatıyor ve başka bir protein olan STUB1'in GPX4'ü yıkım için işaretlemesine izin veriyor. Bu kaskad aynı anda invazyonla ilişkili EMT'yi bastırıyor ve ferroptoz üzerinde bir fren görevi gören korumayı kaldırarak kanser hücrelerini oksidatif hasar ve kemoterapiye karşı daha savunmasız hale getiriyor.
Gelecekteki tedaviler için ne anlama geliyor
Bir arada ele alındığında, bu çalışma tümör büyümesi, metastatik davranış, hücre ölümü ve ilaç yanıtını mide kanserinde birbirine bağlayan kompakt bir düzenleyici eksen — tRF-Ser, CNBP ve HSPA8 — ortaya koyuyor. Günlük bir benzetmeyle, tRF-Ser pro‑büyüme faktörü (CNBP)'yi hücrenin kontrol merkezinden uzaklaştırarak hayatta kalma programını (HSPA8 ve GPX4 aracılığıyla) açmasını engelleyen moleküler bir trafik görevlisi gibi davranıyor. tRF-Ser'i yeniden sağlamak veya taklit etmek ya da onun aşağı akış ortaklarını hedeflemek, 5‑florourasil gibi mevcut ilaçları daha etkili kılabilir ve tedavi direncinin üstesinden gelmeye yardımcı olabilir. Klinik kullanımdan önce daha fazla çalışma gerekli olsa da bu çalışma, küçük RNA parçalarının kanser hücrelerini hayatta kalmadan kendini yok etmeye itme anahtarlarını elinde tutabileceğini vurguluyor.
Atıf: Jiao, J., Wang, G., Liu, J. et al. A new candidate tumor suppressor tRF-Ser inhibits gastric cancer progression by regulating the CNBP/HSPA8 axis. Cell Death Dis 17, 379 (2026). https://doi.org/10.1038/s41419-026-08608-1
Anahtar kelimeler: mide kanseri, tümör baskılayıcı RNA, ferroptoz, kemorezistans, HSPA8 CNBP ekseni