Clear Sky Science · zh
14-3-3γ 敲低促进人体间充质基质细胞的基质矿化
更坚固的骨骼为何始于意想不到的地方
我们的骨骼在一生中不断重建,骨形成细胞行为的微小变化可能决定骨骼是健康还是脆弱。该研究关注一种鲜为人知的细胞辅助蛋白——14-3-3γ,结果显示在人体脂肪来源的干细胞中降低其表达,反而能使它们构建出更丰富、更矿化的类骨基质。理解这个细胞内的制动系统,可能为治疗骨质流失和改善骨修复开启新途径。
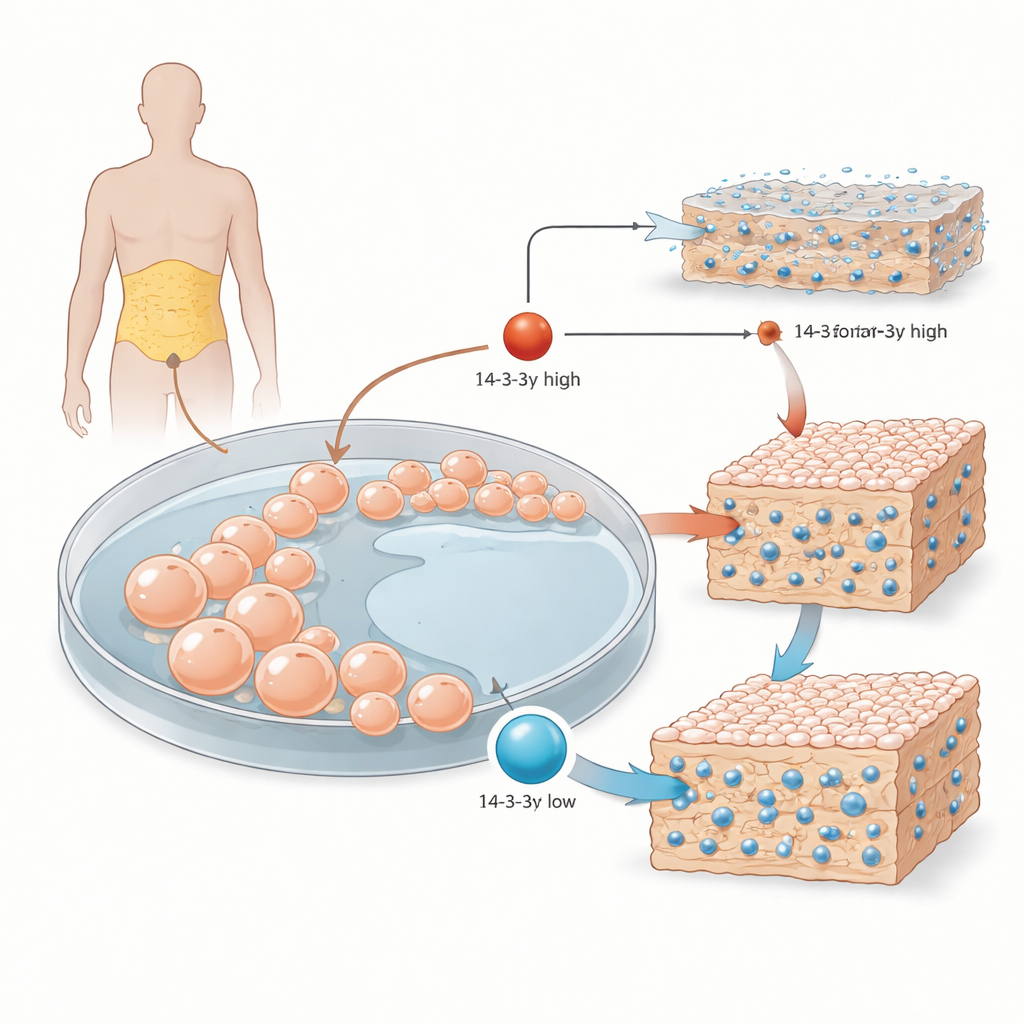
从体脂到成骨细胞
研究者从人体脂肪组织中分离出间充质基质细胞。这类多能细胞可根据所接收的信号分化为骨、软骨或脂肪。在体外实验中,研究团队用标准的诱骨组合刺激这些细胞,并追踪三个主要阶段:早期增殖、细胞周围支架的成熟,以及通过矿物沉积实现的最终硬化。他们关注14-3-3γ,这是一类作为分子组织者的蛋白家族成员之一,能与多种伙伴结合并调节它们在细胞内的活性与定位。
成骨过程中不断变化的“制动器”
当干细胞被推动向成骨方向分化时,14-3-3γ的水平并非保持不变。在中期阶段,即细胞加速合成胶原和其他基质成分时,14-3-3γ水平升高。随后当基质开始通过吸收钙和磷而硬化时,其水平下降。这种波动式的表达模式提示14-3-3γ可能在成骨的不同步骤中进行微调,而不是承担单一固定的角色。
把旋钮向下拧会促进硬化
为验证这一想法,研究团队用工程病毒在细胞内降低或提高14-3-3γ的表达。当14-3-3γ被降低时,一种早期成骨标志酶——碱性磷酸酶活性增强;到了基质硬化阶段,周围基质中含有更多的钙晶体和更多的胶原纤维。相反,强制使细胞产生额外的14-3-3γ则产生相反效果:基质在矿物质和胶原方面变得匮乏。有趣的是,一些成骨的经典基因调控因子,比如RUNX2蛋白和骨钙蛋白、骨桥蛋白的基因,并未与14-3-3γ简单同步升降,这表明该蛋白通过比直接开启或关闭主要基因更细微的途径发挥作用。
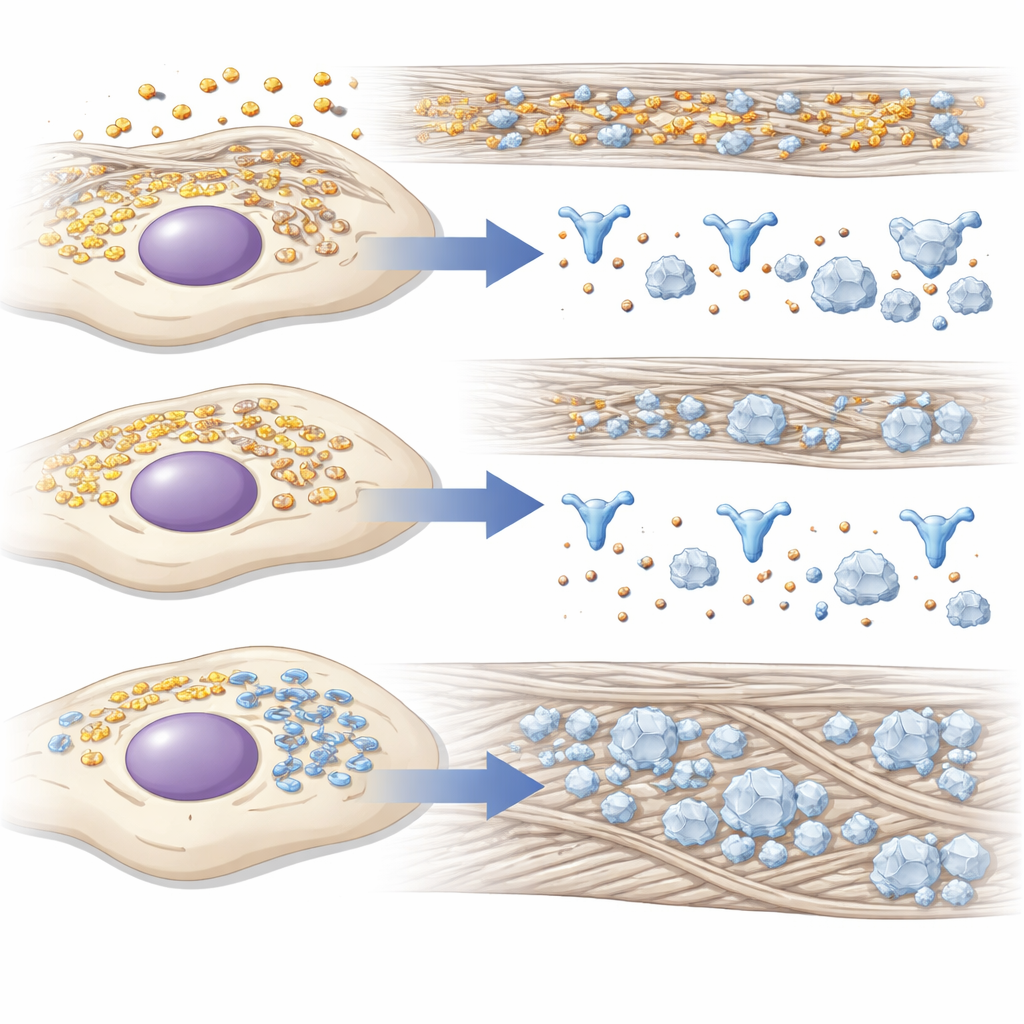
来自细胞“工厂车间”的线索
由于成骨需要大量蛋白生产并精细处理钙和磷,研究者在敲低14-3-3γ时检查了全局蛋白质的变化。通过质谱分析,他们发现与能量利用和低氧反应相关的蛋白趋于减少,而与蛋白折叠、细胞内膜网络的应激以及骨发育相关的蛋白则趋于增加。许多上调的蛋白帮助折叠和加工I型胶原或在细胞外组织胶原,从而为矿物沉积创建更好的支架。显微观察补充了另一层信息:在诱导成骨期间,14-3-3γ从弥散分布转移并集中于内质网附近——细胞主要的蛋白“工厂”,暗示它有助于那里运输和质量控制的管理。
这对未来骨疗法的意义
综合来看,结果将14-3-3γ描绘为对骨基质最终硬化起内在制动作用的因子。当它在恰当时机被适度降低时,干细胞会沉积更多胶原与矿物,较充分地成熟为成骨细胞;而当其水平保持偏高时,这一成熟过程则受到抑制。鉴于14-3-3家族成员已可被小分子调控,学会如何在人体干细胞中选择性调节14-3-3γ,或许最终能为治疗骨质疏松、愈合缓慢的骨折或其他骨重塑失衡的疾病提供思路,同时也提醒我们即便是微小的分子组织者也能对骨骼健康产生重大影响。
引用: Rivera, L., Müller, S., Uhart, M. et al. 14-3-3γ Knockdown promotes matrix mineralization in human mesenchymal stromal cells. Cell Death Dis 17, 415 (2026). https://doi.org/10.1038/s41419-026-08540-4
关键词: 骨矿化, 间充质干细胞, 成骨, 支架胶原, 细胞信号蛋白