Clear Sky Science · fr
Réduction de 14-3-3γ favorise la minéralisation de la matrice chez les cellules stromales mésenchymateuses humaines
Pourquoi des os plus solides commencent parfois là où on ne s’y attend pas
Nos os sont constamment remaniés tout au long de la vie, et de petits décalages dans le comportement des cellules formant l’os peuvent faire la différence entre un squelette sain et des os fragiles. Cette étude examine une protéine auxiliaire cellulaire peu connue, appelée 14-3-3γ, et montre que la réduire dans des cellules souches dérivées de tissu adipeux humain les pousse à produire une matrice de type osseux plus riche et plus minéralisée. Comprendre ce système de freinage interne pourrait ouvrir de nouvelles voies pour traiter la perte osseuse et améliorer la réparation osseuse.
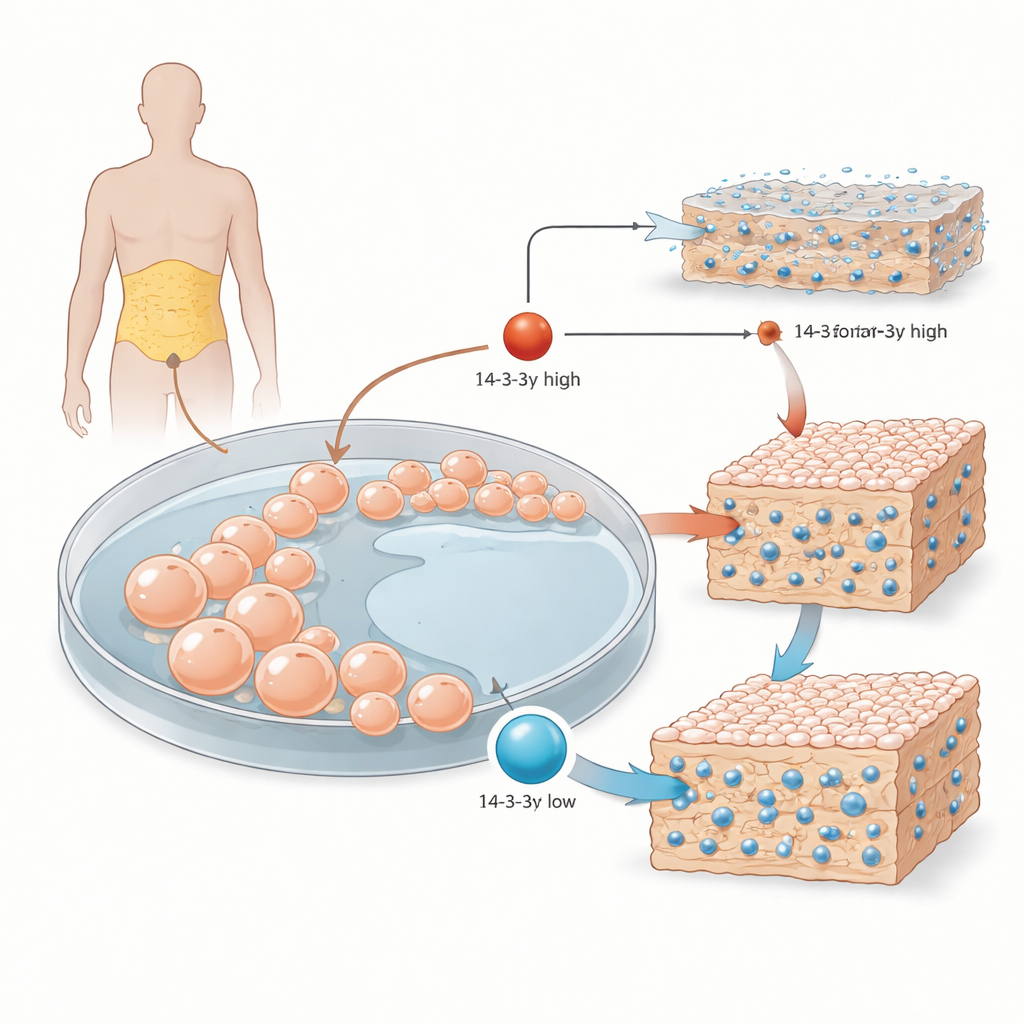
De la graisse corporelle aux cellules bâtisseuses d’os
Les chercheurs ont commencé par des cellules stromales mésenchymateuses prélevées dans du tissu adipeux humain. Ces cellules polyvalentes peuvent se différencier en os, en cartilage ou en graisse, selon les signaux qu’elles reçoivent. En laboratoire, l’équipe les a exposées à un cocktail standard inducteur d’os et a suivi trois étapes principales : croissance précoce, maturation de l’échafaudage qui entoure les cellules, puis durcissement final de cet échafaudage par des dépôts minéraux. Ils se sont concentrés sur 14-3-3γ, un membre d’une famille de protéines qui agissent comme des organisateurs moléculaires, en se liant à de nombreux partenaires et en orientant leur activité et leur localisation à l’intérieur de la cellule.
Un frein qui varie durant la formation osseuse
Lorsque les cellules souches étaient poussées vers la lignée osseuse, les niveaux de 14-3-3γ ne restaient pas constants. Pendant la phase intermédiaire, lorsque les cellules augmentent la production de collagène et d’autres composants de la matrice, les niveaux de 14-3-3γ augmentaient. Plus tard, au moment où la matrice commence à se durcir en incorporant du calcium et du phosphate, ses niveaux diminuaient. Ce profil en vagues suggère que 14-3-3γ pourrait affiner différentes étapes de la formation osseuse plutôt que d’assurer un rôle unique et fixe.
Faible expression = plus de durcissement
Pour tester cette hypothèse, l’équipe a utilisé des virus modifiés pour baisser ou augmenter 14-3-3γ dans les cellules. Lorsque 14-3-3γ était réduit, une enzyme osseuse précoce appelée phosphatase alcaline devenait plus active, et au stade de durcissement, la matrice environnante contenait davantage de cristaux de calcium et plus de fibres de collagène. À l’inverse, forcer la production excessive de 14-3-3γ appauvrissait la matrice en minéraux et en collagène. Fait intéressant, certains régulateurs classiques de la formation osseuse, tels que la protéine RUNX2 et les gènes codant pour l’ostéocalcine et l’ostéopontine, n’évoluaient pas simplement en parallèle avec 14-3-3γ, ce qui suggère que cette protéine agit par des voies plus subtiles que la simple activation ou répression de gènes majeurs.
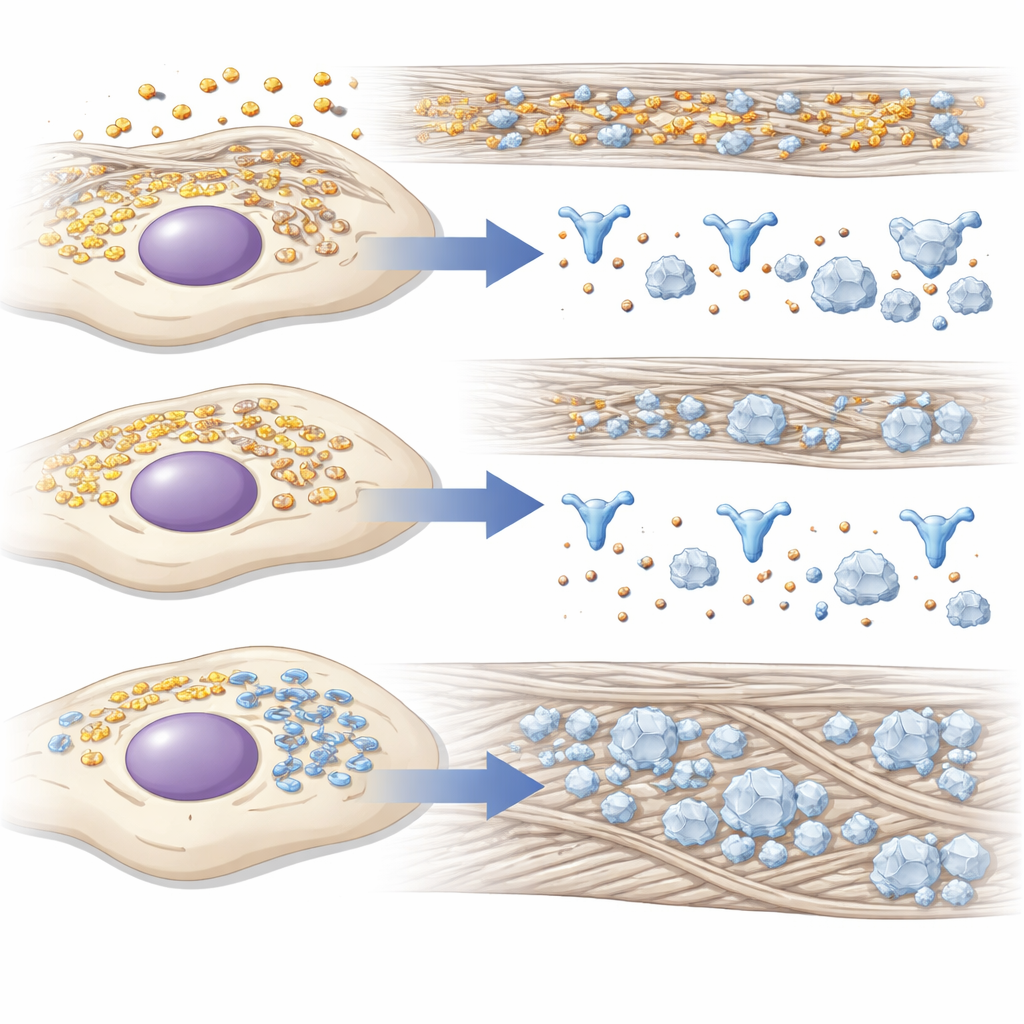
Indices depuis l’atelier intracellulaire
Comme la construction osseuse nécessite une production protéique massive et une gestion précise du calcium et du phosphate, les chercheurs ont examiné les changements protéiques globaux lors de la réduction de 14-3-3γ. Par spectrométrie de masse, ils ont constaté que les protéines liées à l’utilisation d’énergie et aux réponses à l’hypoxie avaient tendance à diminuer, tandis que celles associées au repliement des protéines, au stress du réseau membranaire interne de la cellule et au développement osseux avaient tendance à augmenter. Beaucoup des protéines sur-régulées aident à replier et à traiter le collagène de type I ou à l’organiser à l’extérieur de la cellule, créant un meilleur échafaudage pour les dépôts minéraux. La microscopie a apporté une couche supplémentaire : pendant l’induction osseuse, 14-3-3γ passait d’une distribution diffuse à une concentration près du réticulum endoplasmique, la principale usine à protéines de la cellule, suggérant qu’elle aide à gérer le trafic et le contrôle qualité à cet endroit.
Ce que cela implique pour les thérapies osseuses futures
Pris dans leur ensemble, les résultats présentent 14-3-3γ comme un frein interne au durcissement final de la matrice osseuse. Lorsque ses niveaux sont abaissés au bon moment, les cellules souches déposent plus de collagène et de minéral, achevant mieux leur maturation en cellules formatrices d’os. Lorsque ses niveaux restent élevés, cette maturation est freinée. Étant donné que des membres de la famille 14-3-3 peuvent déjà être ciblés par de petites molécules, apprendre à moduler sélectivement 14-3-3γ dans les cellules souches humaines pourrait éventuellement contribuer à des traitements de l’ostéoporose, des fractures à cicatrisation lente ou d’autres troubles du remodelage osseux, tout en nous rappelant que de petits organisateurs moléculaires peuvent avoir de grands effets sur la santé squelettique.
Citation: Rivera, L., Müller, S., Uhart, M. et al. 14-3-3γ Knockdown promotes matrix mineralization in human mesenchymal stromal cells. Cell Death Dis 17, 415 (2026). https://doi.org/10.1038/s41419-026-08540-4
Mots-clés: minéralisation osseuse, cellules souches mésenchymateuses, ostéogenèse, échafaudage collagène, protéines de signalisation cellulaire