Clear Sky Science · it
La deplezione di 14-3-3γ favorisce la mineralizzazione della matrice nelle cellule stromali mesenchimali umane
Perché ossa più forti nascono in luoghi inaspettati
Le nostre ossa vengono continuamente ricostruite nel corso della vita, e piccole variazioni nel comportamento delle cellule che formano l’osso possono fare la differenza tra uno scheletro sano e ossa fragili. Questo studio esamina una proteina ausiliaria poco conosciuta a livello cellulare, chiamata 14-3-3γ, e mostra che ridurne l’espressione nelle cellule staminali derivate dal tessuto adiposo umano le porta a costruire una matrice di tipo osseo più ricca e maggiormente mineralizzata. Comprendere questo sistema di freno interno potrebbe aprire nuove strade per trattare la perdita di massa ossea e migliorare la riparazione ossea.
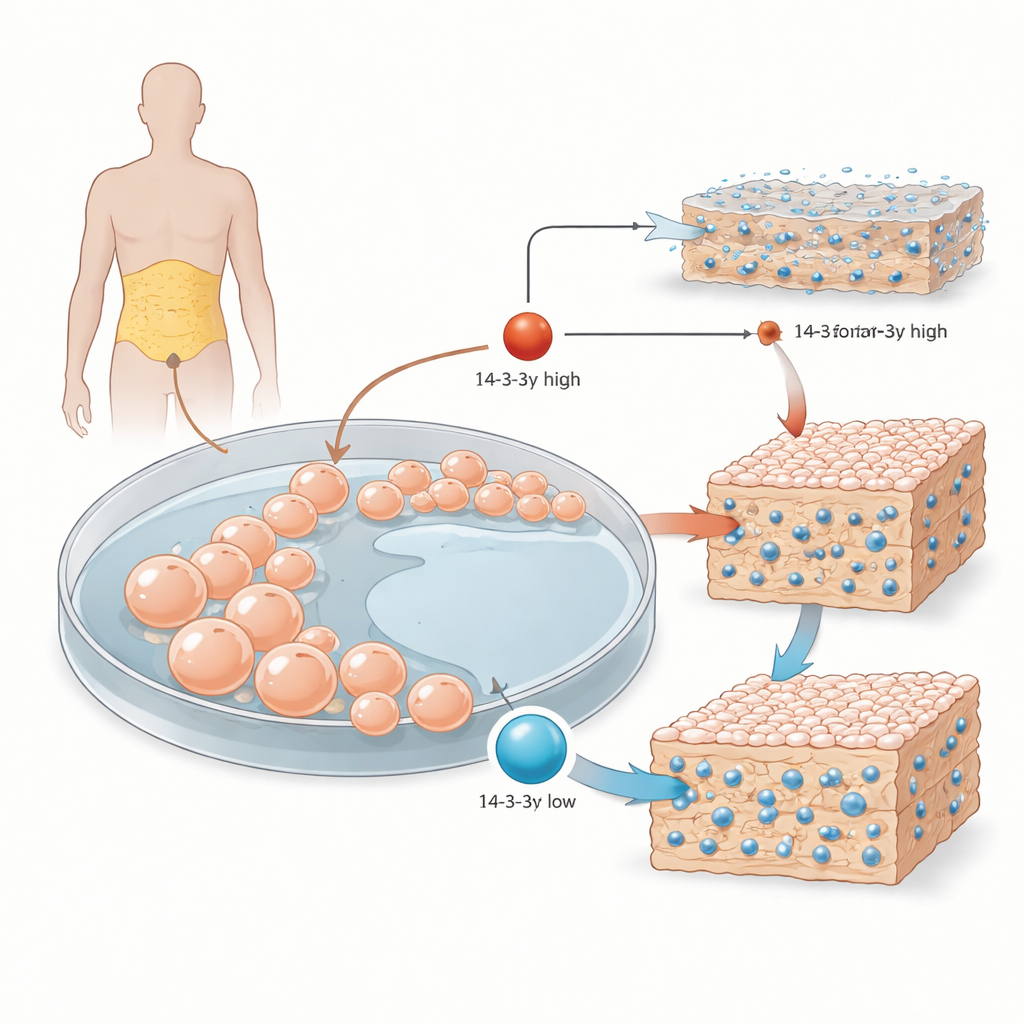
Dal grasso corporeo alle cellule che costruiscono osso
I ricercatori hanno iniziato con cellule stromali mesenchimali prelevate da tessuto adiposo umano. Queste cellule versatili possono trasformarsi in osso, cartilagine o grasso, a seconda dei segnali che ricevono. In laboratorio il gruppo le ha esposte a un cocktail standard che induce la formazione ossea e ha seguito tre fasi principali: crescita iniziale, maturazione dell’impalcatura che circonda le cellule e indurimento finale di quell’impalcatura con depositi minerali. Si sono concentrati su 14-3-3γ, membro di una famiglia di proteine che funzionano come organizzatori molecolari, legando molti partner diversi e orientandone l’attività e la localizzazione all’interno della cellula.
Un freno che cambia durante la formazione ossea
Man mano che le cellule staminali venivano indirizzate verso il fenotipo osteoblastico, i livelli di 14-3-3γ non restavano costanti. Durante la fase intermedia, quando le cellule aumentano la produzione di collagene e di altri componenti della matrice, i livelli di 14-3-3γ aumentavano. Più tardi, quando la matrice comincia a indurirsi assorbendo calcio e fosfato, i suoi livelli diminuivano. Questo andamento a onda suggerisce che 14-3-3γ potrebbe sintonizzare finemente diversi step della formazione ossea, più che svolgere un ruolo unico e fisso.
Abbassare la manopola potenzia l’indurimento
Per mettere alla prova questa ipotesi, il gruppo ha usato virus ingegnerizzati per ridurre o aumentare 14-3-3γ all’interno delle cellule. Quando 14-3-3γ veniva abbassata, un marcatore osseo precoce, l’enzima fosfatasi alcalina, risultava più attivo e, al raggiungimento della fase di indurimento, la matrice circostante conteneva più cristalli di calcio e più fibre di collagene. Al contrario, forzare le cellule a produrre 14-3-3γ in eccesso aveva l’effetto opposto: la matrice era più povera di minerali e di collagene. È interessante che alcuni classici interruttori genetici dell’osteogenesi, come la proteina RUNX2 e i geni per osteocalcina e osteopontina, non variassero semplicemente in parallelo con 14-3-3γ, suggerendo che questa proteina agisca attraverso vie più sottili che non si limitano ad attivare o spegnere grandi geni.
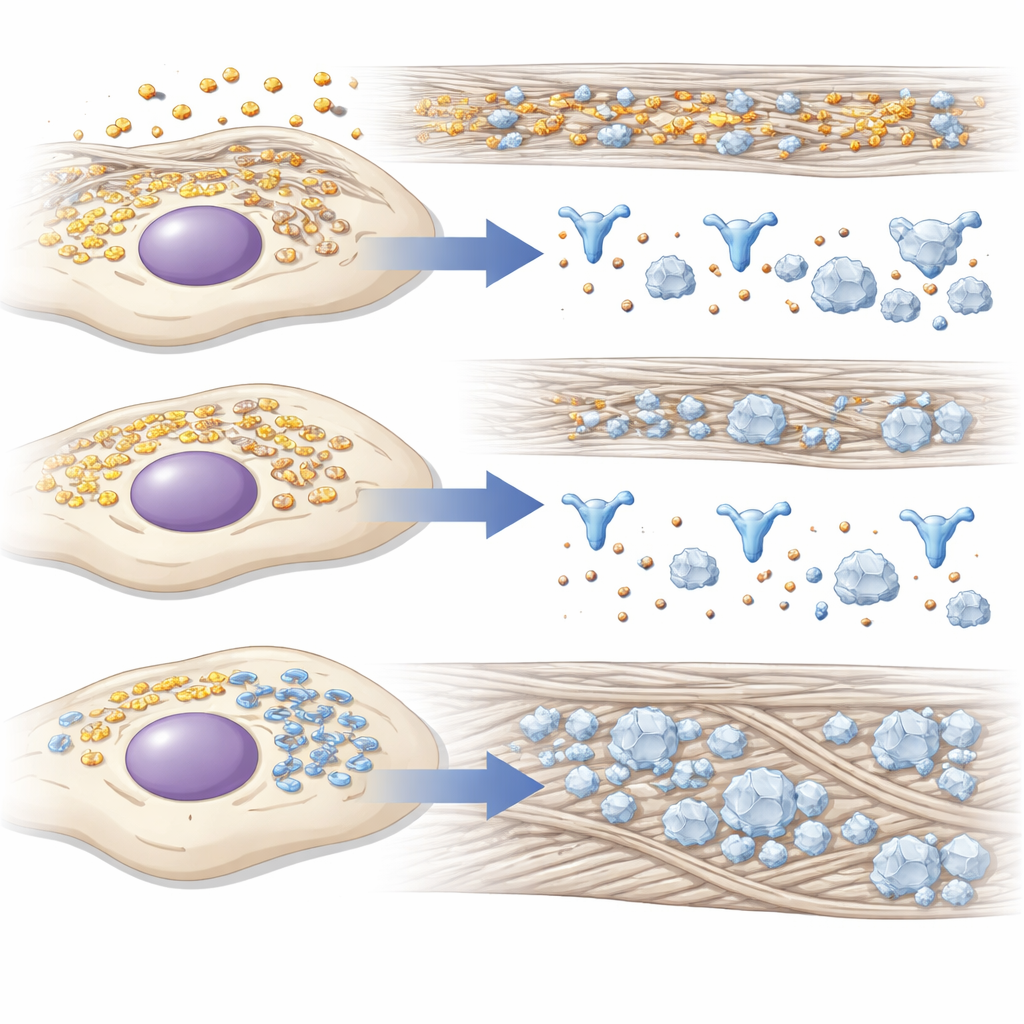
Indizi dal “piano di produzione” della cellula
Poiché costruire osso richiede una massiccia produzione proteica e una precisa gestione di calcio e fosfato, i ricercatori hanno esaminato i cambiamenti proteici globali quando 14-3-3γ veniva deplezionata. Tramite spettrometria di massa hanno constatato che le proteine legate all’uso di energia e alle risposte a basso ossigeno tendevano a diminuire, mentre aumentavano quelle associate al ripiegamento delle proteine, allo stress nel network di membrane interne della cellula e allo sviluppo osseo. Molte delle proteine upregolate assistono nel ripiegamento e nel processamento del collagene di tipo I o ne organizzano l’assemblaggio al di fuori della cellula, creando un’impalcatura migliore per i depositi minerali. La microscopia ha aggiunto un altro livello di informazione: durante l’induzione osteogenica, 14-3-3γ si spostava da una distribuzione diffusa a una concentrazione vicino al reticolo endoplasmatico, la principale “fabbrica” proteica della cellula, suggerendo che aiuti a gestire il traffico e il controllo qualità lì.
Cosa significa per le terapie ossee future
Nel complesso, i risultati ritraggono 14-3-3γ come un freno intrinseco sull’indurimento finale della matrice ossea. Quando i suoi livelli vengono abbassati al momento giusto, le cellule staminali depositano più collagene e minerale, maturando in modo più completo verso il fenotipo osteogenico. Se i suoi livelli restano elevati, questa maturazione viene rallentata. Poiché membri della famiglia 14-3-3 possono già essere modulati da piccole molecole, imparare a sintonizzare selettivamente 14-3-3γ nelle cellule staminali umane potrebbe a lungo termine contribuire a trattamenti per osteoporosi, fratture che guariscono lentamente o altri disturbi del rimodellamento osseo, ricordandoci anche che anche piccoli organizzatori molecolari possono avere grandi effetti sulla salute scheletrica.
Citazione: Rivera, L., Müller, S., Uhart, M. et al. 14-3-3γ Knockdown promotes matrix mineralization in human mesenchymal stromal cells. Cell Death Dis 17, 415 (2026). https://doi.org/10.1038/s41419-026-08540-4
Parole chiave: mineralizzazione ossea, cellule staminali mesenchimali, osteogenesi, impalcatura di collagene, proteine di segnalazione cellulare