Clear Sky Science · de
14-3-3γ-Downregulation fördert die Matrixmineralisierung in humanen mesenchymalen Stromazellen
Warum stärkere Knochen an unerwarteten Orten beginnen
Unsere Knochen werden ein Leben lang ständig erneuert, und schon kleine Veränderungen im Verhalten knochenbildender Zellen können den Unterschied zwischen einem gesunden Skelett und brüchigen Knochen ausmachen. Diese Studie untersucht ein wenig bekanntes zelluläres Hilfsprotein, genannt 14-3-3γ, und zeigt, dass dessen Herabsetzung in aus Fett gewonnenen menschlichen Stammzellen tatsächlich dazu führt, dass sie eine reichere, stärker mineralisierte knochenähnliche Matrix bilden. Das Verständnis dieses internen Bremssystems könnte neue Wege für die Behandlung von Knochenschwund und die Verbesserung der Knochenheilung eröffnen.
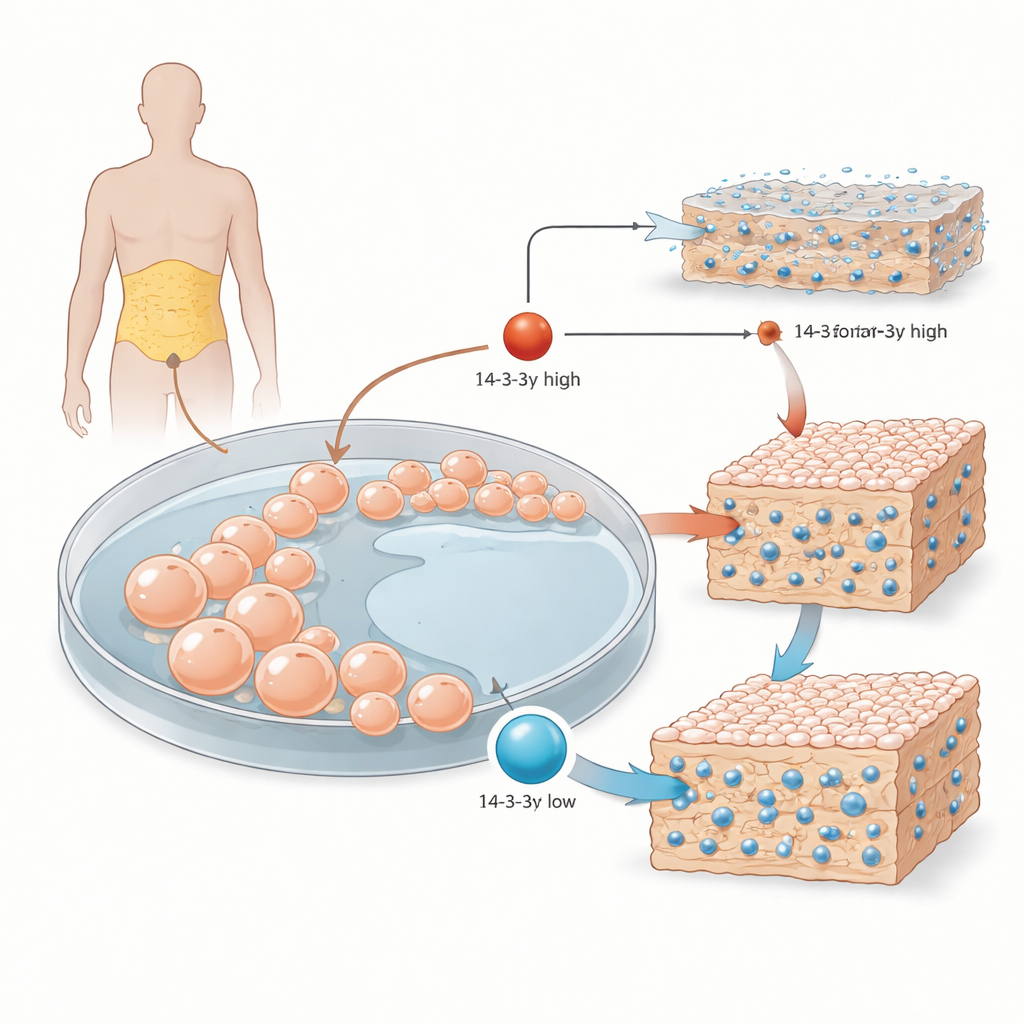
Von Körperfett zu knochenbildenden Zellen
Die Forschenden begannen mit mesenchymalen Stromazellen, die aus menschlichem Fettgewebe entnommen wurden. Diese vielseitigen Zellen können je nach empfangenen Signalen zu Knochen, Knorpel oder Fett differenzieren. Im Labor setzte das Team sie einem standardisierten knocheninduzierenden Cocktail aus und verfolgte drei Hauptphasen: frühes Wachstum, die Reifung des stützenden Gerüsts um die Zellen herum und das abschließende Verhärten dieses Gerüsts durch Mineralablagerungen. Im Fokus stand 14-3-3γ, ein Mitglied einer Proteinfamilie, die als molekulare Organisatoren wirkt, viele verschiedene Partner bindet und deren Aktivität sowie zelluläre Lokalisation steuert.
Eine wechselnde Bremse während der Knochenbildung
Als die Stammzellen in Richtung Knochenzellen gedrängt wurden, blieben die 14-3-3γ-Spiegel nicht konstant. Während der mittleren Phase, in der die Zellen die Produktion von Kollagen und anderen Matrixbestandteilen hochfahren, stiegen die 14-3-3γ-Werte an. Später, wenn die Matrix zu verhärten beginnt, indem sie Kalzium und Phosphat aufnimmt, fielen die Werte wieder. Dieses wellenartige Muster deutete darauf hin, dass 14-3-3γ verschiedene Schritte der Knochenbildung feinabstimmen könnte, statt eine einzelne, feste Rolle einzunehmen.
Den Drehregler herunterzudrehen verstärkt das Verhärten
Um diese Idee zu testen, nutzte das Team gentechnisch veränderte Viren, um 14-3-3γ innerhalb der Zellen entweder zu reduzieren oder zu erhöhen. Bei Reduktion von 14-3-3γ wurde ein frühes Knochenmarker-Enzym, die alkalische Phosphatase, aktiver, und bis die Kulturen die Verhärtungsphase erreichten, enthielt die umgebende Matrix mehr Calciumkristalle und mehr Kollagenfasern. Im Gegensatz dazu hatte die erzwungene Überproduktion von 14-3-3γ den gegenteiligen Effekt: Die Matrix war ärmer an Mineralien und Kollagen. Interessanterweise stiegen klassische genetische Schalter der Knochenbildung, wie das RUNX2-Protein und die Gene für Osteocalcin und Osteopontin, nicht einfach synchron mit 14-3-3γ an oder ab, was darauf hindeutet, dass dieses Protein über subtilere Wege wirkt als nur das Ein- oder Ausschalten großer Gene.
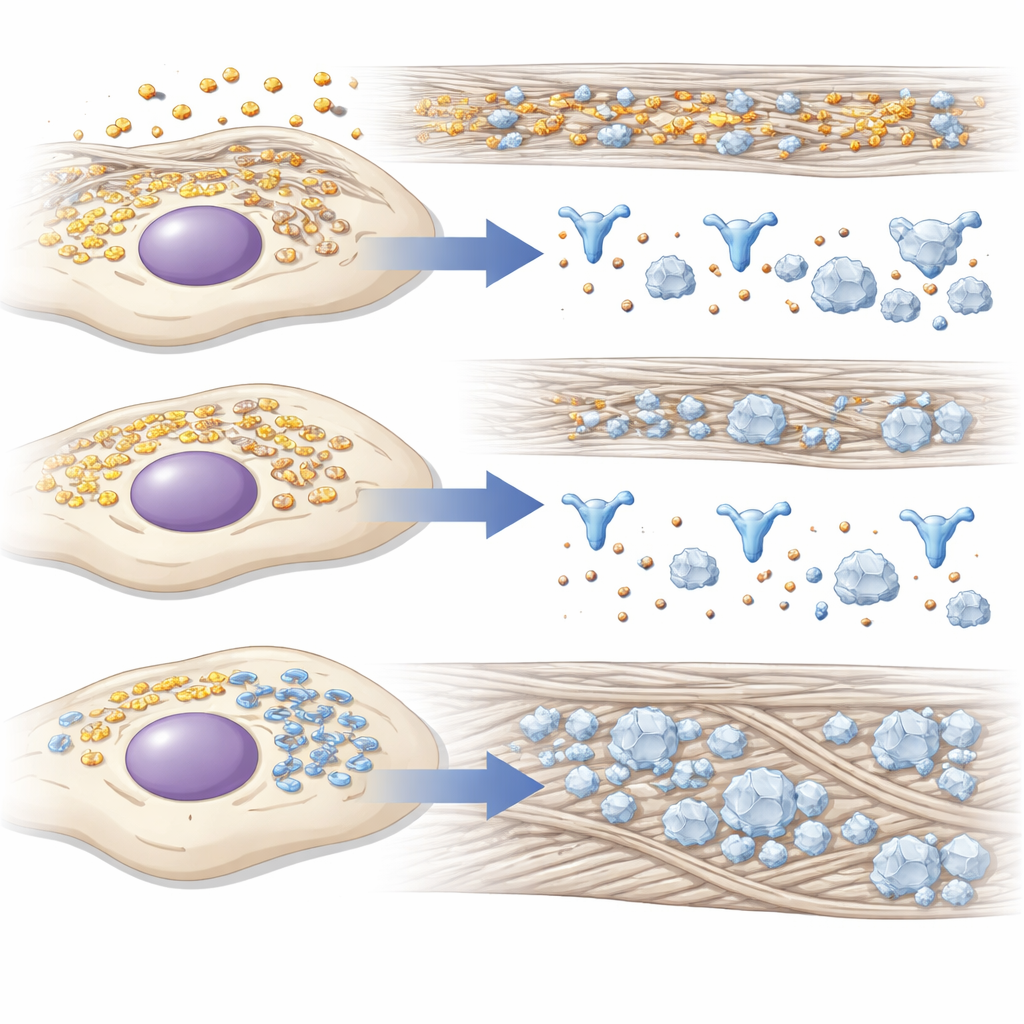
Hinweise aus der Fabrikhalle der Zelle
Da Knochenaufbau massive Proteinproduktion und eine sorgfältige Handhabung von Kalzium und Phosphat erfordert, untersuchten die Forschenden globale Proteinveränderungen nach 14-3-3γ-Downregulation. Mittels Massenspektrometrie fanden sie, dass Proteine, die mit Energieverbrauch und Reaktionen auf niedrigen Sauerstoffgehalt verknüpft sind, tendenziell abnahmen, während solche, die mit Proteinfaltung, Stress im inneren Membrannetzwerk der Zelle und Knochenentwicklung zusammenhängen, zunahmen. Viele dieser hochregulierten Proteine helfen dabei, Typ‑I‑Kollagen zu falten und zu verarbeiten oder es außerhalb der Zelle zu organisieren und so ein besseres Gerüst für Mineralablagerungen zu schaffen. Die Mikroskopie ergänzte diese Befunde: Während der Knocheninduktion verlagerte sich 14-3-3γ von einer diffusen Verteilung hin zu einer Konzentration in der Nähe des endoplasmatischen Retikulums, der Hauptproteinfabrik der Zelle, was darauf hindeutet, dass es dort den Verkehr und die Qualitätskontrolle mitsteuert.
Was das für künftige Knochentherapien bedeutet
Insgesamt zeichnen die Ergebnisse 14-3-3γ als eine eingebaute Bremse für das abschließende Verhärten der Knochenmatrix. Wird sein Spiegel zur richtigen Zeit angemessen gesenkt, lagern Stammzellen mehr Kollagen und Mineral ein und reifen vollständiger zu knochenbildenden Zellen heran. Bleibt sein Spiegel hoch, wird diese Reifung gebremst. Da Mitglieder der 14-3-3-Familie bereits durch kleine Moleküle anvisiert werden können, könnte das gezielte Einstellen von 14-3-3γ in humanen Stammzellen langfristig zu Behandlungen bei Osteoporose, schlecht heilenden Frakturen oder anderen Störungen beitragen, bei denen das Knochenremodelling gestört ist — und erinnert zugleich daran, dass selbst winzige molekulare Organisatoren große Auswirkungen auf die Skelettgesundheit haben können.
Zitation: Rivera, L., Müller, S., Uhart, M. et al. 14-3-3γ Knockdown promotes matrix mineralization in human mesenchymal stromal cells. Cell Death Dis 17, 415 (2026). https://doi.org/10.1038/s41419-026-08540-4
Schlüsselwörter: Knochenmineralisierung, mesenchymale Stammzellen, Osteogenese, Gerüst Kollagen, Zellsignalisierungsproteine