Clear Sky Science · ar
تثبيط 14-3-3γ يعزز تمعدن المصفوفة في الخلايا الطُّرَحِيَّة الميزنشيمية البشرية
لماذا تبدأ العظام الأقوى في أماكن غير متوقعة
تعاد بناء عظامنا باستمرار طوال الحياة، وتغييراتٍ طفيفة في سلوك الخلايا المكونة للعظم قد تفرق بين هيكل عظمي سليم وعظام هشة. تدرس هذه الورقة بروتينًا مساعدًا خلويًا قليلَ المعرفة يُدعى 14-3-3γ، وتُظهر أن تقليل مستوياته في خلايا جذعية مستمدة من النسيج الدهني البشري يجعلها فعليًا تُنشئ مصفوفة أشبه بالعظم أكثر ثراءً وتمعدنًا. قد يفتح فهم هذا النظام الفرامل الداخلي طرقًا جديدة لعلاج فقدان العظم وتحسين إصلاح العظام.
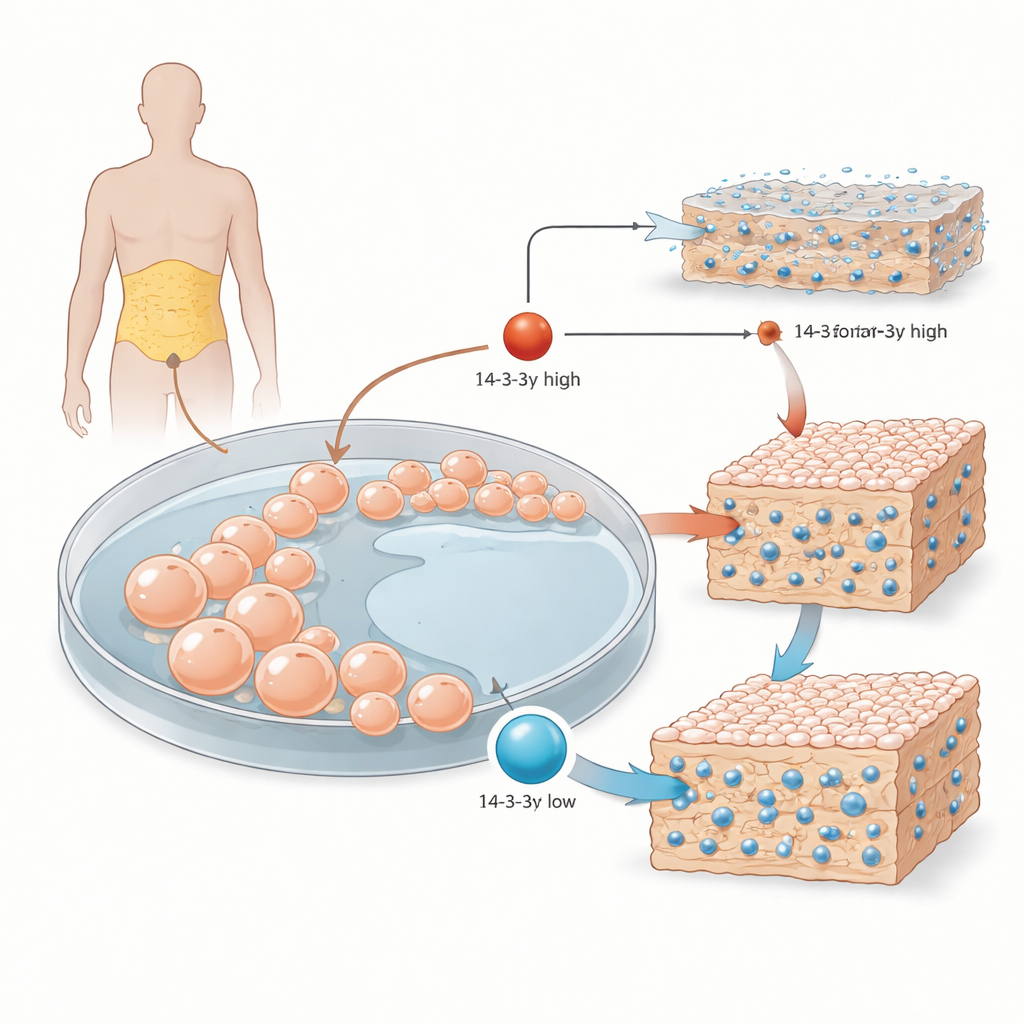
من دهون الجسم إلى خلايا بانية للعظم
بدأ الباحثون بالخلايا الطُّرَحِيَّة الميزنشيمية المأخوذة من نسيج دهني بشري. هذه الخلايا المتعددة الاستخدامات يمكن أن تتحول إلى عظم أو غضروف أو دهن حسب الإشارات التي تستقبلها. في المختبر، عرَّض الفريق الخلايا لخلطة قياسية محفزة لتكوّن العظم وتتبّع ثلاث مراحل رئيسية: النمو المبكر، ونضج السقالة الداعمة حول الخلايا، والتصلّب النهائي لتلك السقالة عبر ترسّب المعادن. ركزوا على 14-3-3γ، عضو من عائلة بروتينات تعمل كمنظِّمات جزيئية، تربط شركاء متعدّدين وتوجّه نشاطهم وموقعهم داخل الخلية.
فرملة متغيرة أثناء تكوّن العظم
عندما دُفعت الخلايا الجذعية نحو أن تصبح خلايا عظمية، لم تظل مستويات 14-3-3γ ثابتة. خلال المرحلة الوسطى، عندما تزداد خلايا إنتاج الكولاجين ومكونات المصفوفة الأخرى، ارتفعت مستويات 14-3-3γ. لاحقًا، عندما تبدأ المصفوفة في التصلّب عبر امتصاص الكالسيوم والفوسفات، انخفضت مستوياته. يشير هذا النمط الموجي إلى أن 14-3-3γ قد يقوم بضبط دقيق لمراحل مختلفة من تكوّن العظم بدل أن يؤدي دورًا ثابتًا واحدًا.
خفضه يعزز التصلب
لاختبار هذه الفكرة، استخدم الفريق فيروسات مهندسة لتقليل أو زيادة 14-3-3γ داخل الخلايا. عند تقليل 14-3-3γ، أصبح إنزيم علامة العظم المبكرة ألفا قاعدية الفوسفاتاز أكثر نشاطًا، وبحلول مرحلة التصلب احتوت المصفوفة المحيطة على مزيد من بلورات الكالسيوم وألياف الكولاجين. بالمقابل، أدى إجبار الخلايا على إنتاج 14-3-3γ إضافي إلى التأثير المعاكس: أصبحت المصفوفة أفقر في المعادن والكولاجين. ومن المثير للاهتمام أن بعض مفاتيح التعبير الجيني الكلاسيكية في تكوّن العظم، مثل بروتين RUNX2 والجينات المشفرة للأوستيوكالسين والأوستيوبانتين، لم ترتفع أو تنخفض ببساطة مع 14-3-3γ، ما يرجح أن هذا البروتين يعمل عبر مسارات أكثر دقة من مجرد تشغيل أو إيقاف الجينات الرئيسية.
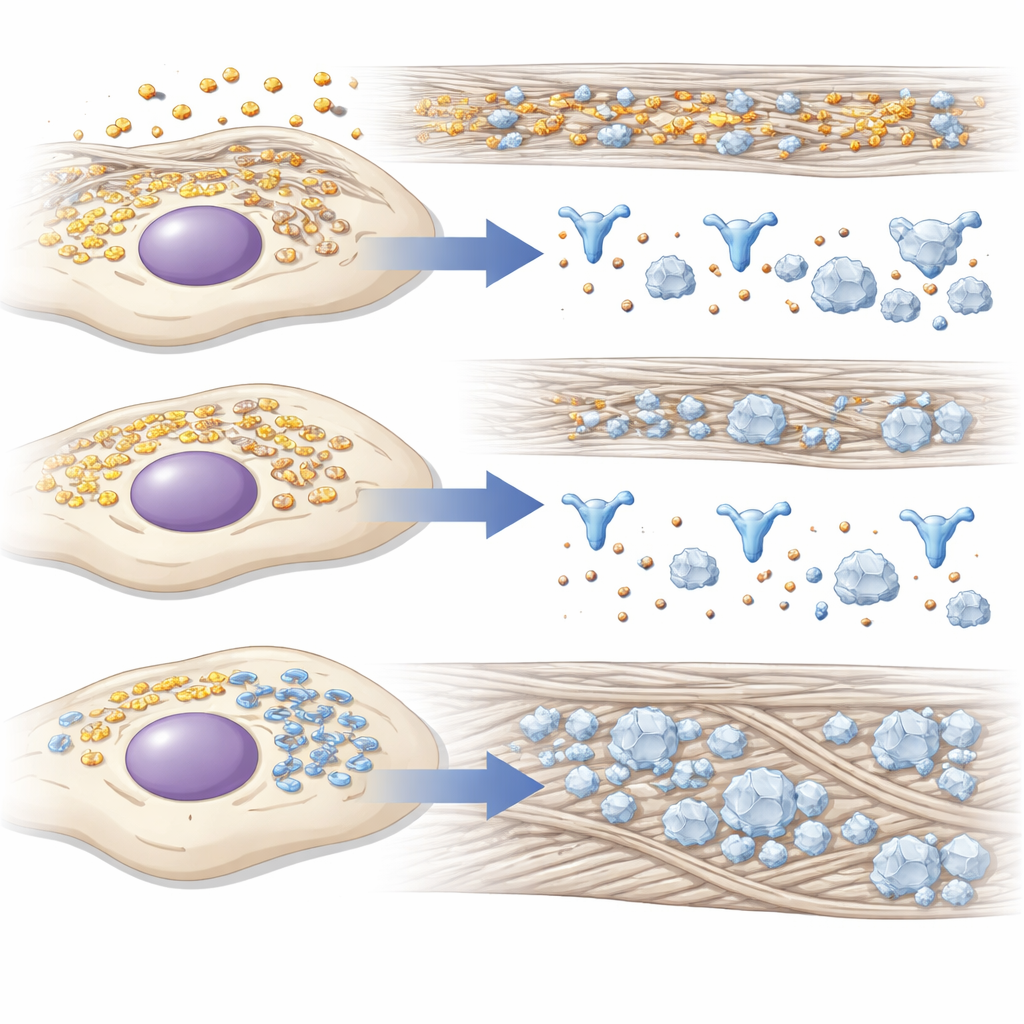
دلائل من «مصنع» الخلية
نظرًا لأن بناء العظم يتطلب إنتاجًا هائلاً من البروتينات وتعاملًا دقيقًا مع الكالسيوم والفوسفات، نظر الباحثون إلى التغيرات البروتينية الكلية عند تثبيط 14-3-3γ. باستخدام مطيافية الكتلة، وجدوا أن البروتينات المرتبطة باستخدام الطاقة والاستجابة لانخفاض الأكسجين كانت تميل إلى الانخفاض، في حين أن البروتينات المرتبطة طي البروتينات، والإجهاد في شبكة الأغشية الداخلية للخلية، وتطوّر العظم كانت تميل إلى الارتفاع. كثير من هذه البروتينات المرفوعة تساعد على طي ومعالجة الكولاجين من النوع الأول أو تنظيمه خارج الخلية، مكوِّنة سقالة أفضل لترسّب المعادن. أضافت المجهرية طبقة أخرى: أثناء تحريض تكوّن العظم، تحرَّك 14-3-3γ من توزيع مشتت إلى تركيز قرب الشبكة الإندوبلازمية، مصنع البروتين الرئيسي في الخلية، موحيًا بأنه يساهم في إدارة المرور ومراقبة الجودة هناك.
ما معنى ذلك لعلاجات العظام المستقبلية
مجتمعة، ترسم النتائج صورة 14-3-3γ كفرامل مدمجة على التصلّب النهائي لمصفوفة العظم. عندما تُخفض مستوياته في الوقت المناسب بشكل مناسب، تودع الخلايا الجذعية مزيدًا من الكولاجين والمعادن، وتتمايز بشكل أكمل إلى خلايا بانية للعظم. وعندما تبقى المستويات مرتفعة، يُعيق ذلك النضج. ونظرًا إلى أن أعضاء عائلة 14-3-3 يمكن استهدافها بالفعل بجزيئات صغيرة، فإن تعلّم كيفية ضبط 14-3-3γ انتقائيًا في الخلايا الجذعية البشرية قد يسهم في النهاية في علاجات لهشاشة العظام أو الكسور بطيئة الالتئام أو اضطرابات أخرى يختل فيها إعادة تشكيل العظم، وفي الوقت نفسه يذكرنا أن حتى المنظِّمات الجزيئية الصغيرة قد يكون لها تأثيرات كبيرة على صحة الهيكل العظمي.
الاستشهاد: Rivera, L., Müller, S., Uhart, M. et al. 14-3-3γ Knockdown promotes matrix mineralization in human mesenchymal stromal cells. Cell Death Dis 17, 415 (2026). https://doi.org/10.1038/s41419-026-08540-4
الكلمات المفتاحية: تمعدن العظم, الخلايا الجذعية الميزنشيمية, تكوُّن العظم, سقالة الكولاجين, بروتينات إشارة الخلية