Clear Sky Science · es
La reducción de 14-3-3γ promueve la mineralización de la matriz en células madre mesenquimales humanas
Por qué huesos más fuertes empiezan en sitios inesperados
Nuestros huesos se reconstruyen constantemente a lo largo de la vida, y pequeños cambios en el comportamiento de las células formadoras de hueso pueden marcar la diferencia entre un esqueleto sano y huesos frágiles. Este estudio examina una proteína auxiliar celular poco conocida, llamada 14-3-3γ, y muestra que reducirla en células madre derivadas de grasa humana en realidad las hace construir una matriz similar al hueso más rica y más mineralizada. Entender este sistema de freno interno podría abrir nuevas vías para tratar la pérdida ósea y mejorar la reparación ósea.
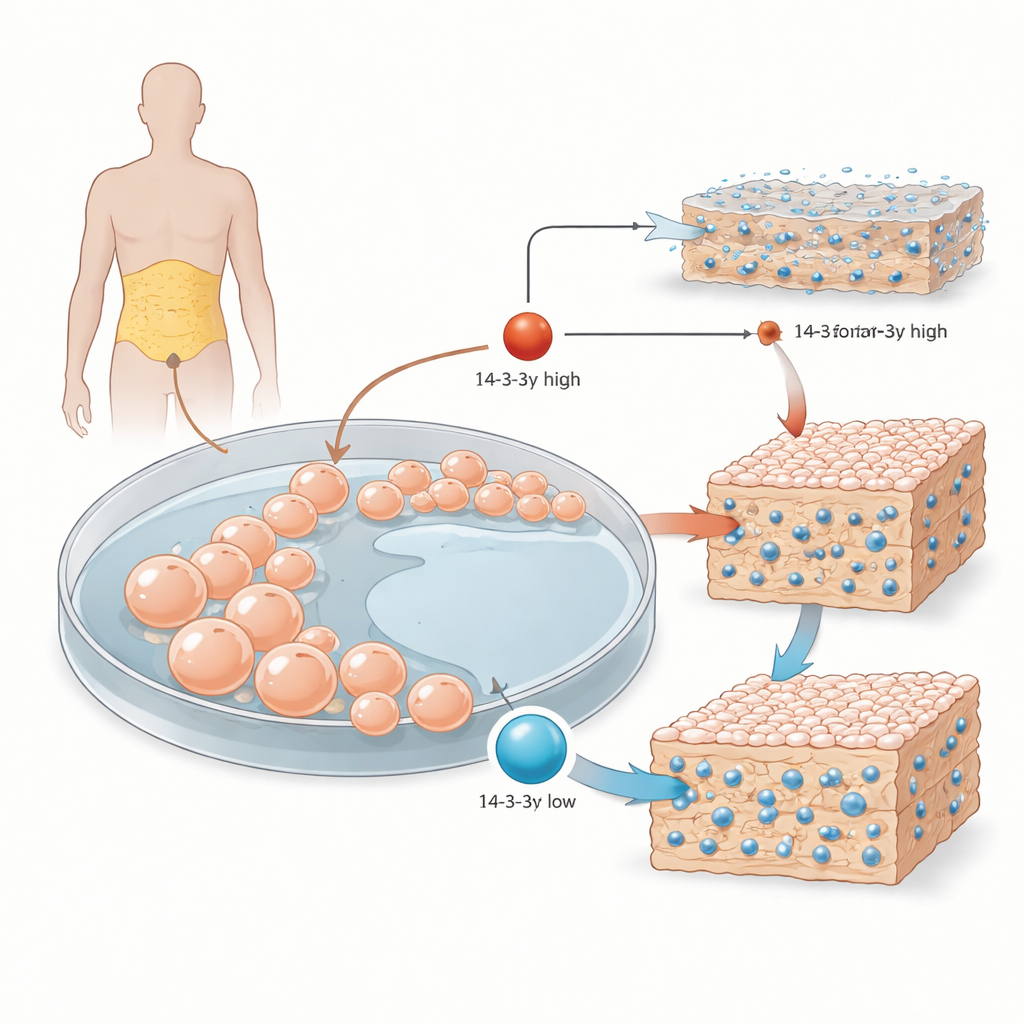
De la grasa corporal a células formadoras de hueso
Los investigadores comenzaron con células estromales mesenquimales tomadas de tejido graso humano. Estas células versátiles pueden convertirse en hueso, cartílago o grasa, según las señales que reciban. En el laboratorio, el equipo las expuso a un cóctel estándar inductivo de hueso y siguió tres etapas principales: crecimiento inicial, maduración del andamiaje que rodea a las células y endurecimiento final de ese andamiaje con depósitos minerales. Se centraron en 14-3-3γ, un miembro de una familia de proteínas que actúan como organizadores moleculares, uniéndose a muchos socios distintos y orientando su actividad y localización dentro de la célula.
Un freno cambiante durante la formación ósea
A medida que las células madre se empujaban hacia convertirse en osteoblastos, los niveles de 14-3-3γ no se mantuvieron constantes. Durante la fase intermedia, cuando las células aumentan la producción de colágeno y otros componentes de la matriz, los niveles de 14-3-3γ subieron. Más tarde, cuando la matriz comienza a endurecerse mediante la incorporación de calcio y fosfato, sus niveles disminuyeron. Este patrón ondulante sugiere que 14-3-3γ podría afinar distintos pasos de la formación ósea en lugar de ejercer un único papel fijo.
Bajar el control aumenta el endurecimiento
Para probar esta idea, el equipo usó virus diseñados para reducir o aumentar 14-3-3γ dentro de las células. Cuando 14-3-3γ se redujo, una enzima marcadora temprana de hueso llamada fosfatasa alcalina se volvió más activa y, cuando los cultivos alcanzaron la fase de endurecimiento, la matriz circundante contenía más cristales de calcio y más fibras de colágeno. En contraste, forzar a las células a producir exceso de 14-3-3γ produjo el efecto opuesto: la matriz quedó más pobre en minerales y colágeno. De forma interesante, algunos interruptores genéticos clásicos de la formación ósea, como la proteína RUNX2 y los genes de osteocalcina y osteopontina, no subieron y bajaron a la par de 14-3-3γ, lo que sugiere que esta proteína actúa por vías más sutiles que no se limitan a encender o apagar genes principales.
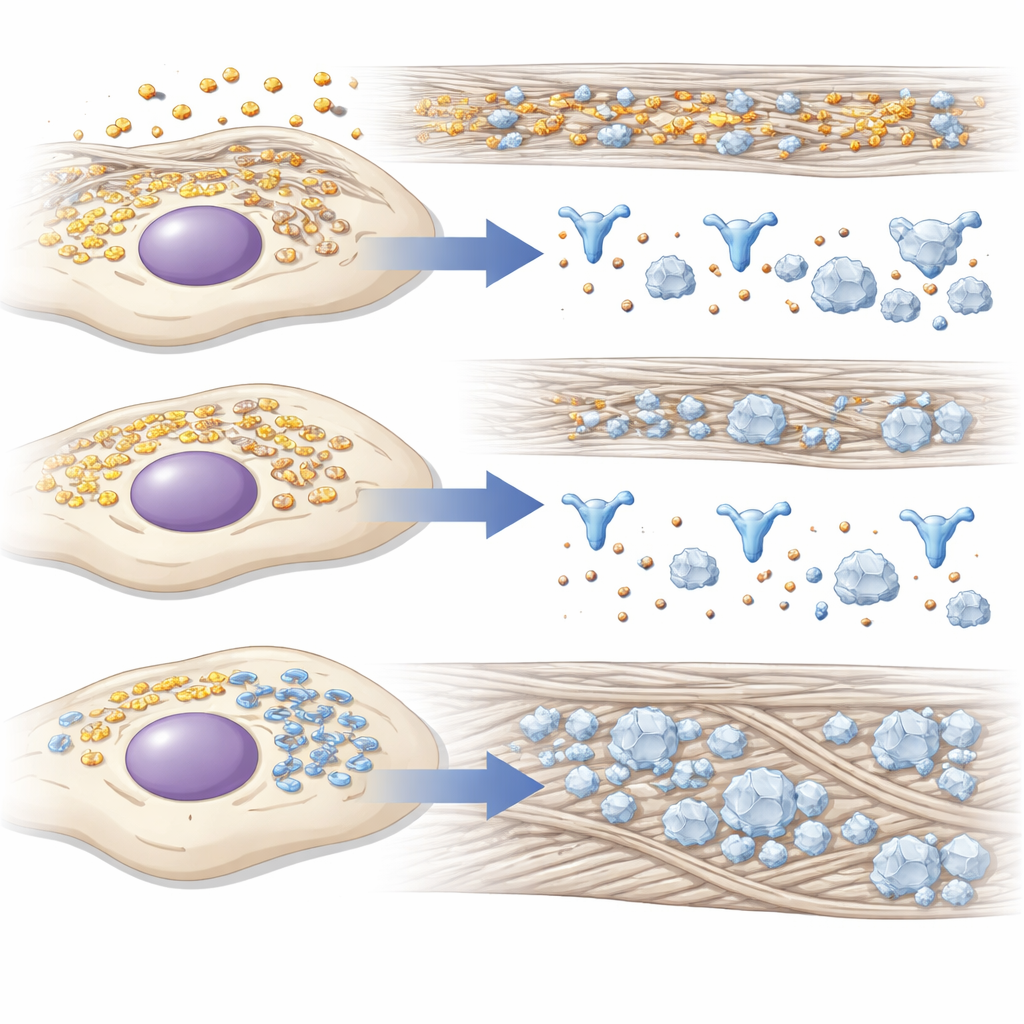
Pistas desde la línea de producción celular
Dado que construir hueso requiere una producción masiva de proteínas y un manejo cuidadoso de calcio y fosfato, los investigadores analizaron los cambios proteicos globales cuando 14-3-3γ fue reducido. Mediante espectrometría de masas, encontraron que las proteínas vinculadas al uso de energía y a las respuestas a baja oxigenación tendían a disminuir, mientras que las asociadas al plegamiento de proteínas, al estrés en la red de membranas internas de la célula y al desarrollo óseo tendían a aumentar. Muchas de estas proteínas sobreexpresadas ayudan a plegar y procesar el colágeno tipo I u organizarlo fuera de la célula, creando un mejor andamiaje para los depósitos minerales. La microscopía añadió otra capa: durante la inducción ósea, 14-3-3γ pasó de una distribución difusa a concentrarse cerca del retículo endoplásmico, la principal fábrica de proteínas celular, lo que sugiere que ayuda a gestionar el tráfico y el control de calidad allí.
Qué significa esto para futuras terapias óseas
En conjunto, los resultados describen a 14-3-3γ como un freno incorporado en el endurecimiento final de la matriz ósea. Cuando sus niveles se reducen de forma adecuada en el momento oportuno, las células madre depositan más colágeno y mineral, madurando más completamente hacia células formadoras de hueso. Si sus niveles se mantienen altos, esta maduración se ve retenida. Dado que miembros de la familia 14-3-3 ya pueden ser dirigidos por pequeñas moléculas, aprender a sintonizar selectivamente 14-3-3γ en células madre humanas podría contribuir en el futuro a tratamientos para la osteoporosis, fracturas de consolidación lenta u otros trastornos en los que el remodelado óseo falla, y nos recuerda que incluso pequeños organizadores moleculares pueden tener grandes efectos sobre la salud esquelética.
Cita: Rivera, L., Müller, S., Uhart, M. et al. 14-3-3γ Knockdown promotes matrix mineralization in human mesenchymal stromal cells. Cell Death Dis 17, 415 (2026). https://doi.org/10.1038/s41419-026-08540-4
Palabras clave: mineralización ósea, células madre mesenquimales, osteogénesis, andscaffold collagen, proteínas de señalización celular