Clear Sky Science · he
דיכוי 14-3-3γ מקדם מינרליזציה של המטריצה בתאי סטרומה מזנכימליים אנושיים
מדוע עצמות חזקות מתחילות במקומות בלתי צפויים
העצמות שלנו מתחדשות כל הזמן לאורך החיים, ושינויים זעירים בהתנהגות התאים בוני העצם יכולים להיות ההבדל בין שלד בריא לבין עצמות שבירות. המחקר הזה בוחן חלבון עזר תאי פחות מוכר בשם 14-3-3γ ומראה שהפחתתו בתאי גזע שמקורם ברקמת שומן אנושית למעשה גורמת להם לבנות מטריצה דמוית עצם עשירה וממינרלזת יותר. הבנת מערכת הבלימה הפנימית הזו עשויה לפתוח דרכים חדשות לטיפול באובדן עצם ולשיפור תיקון העצם.
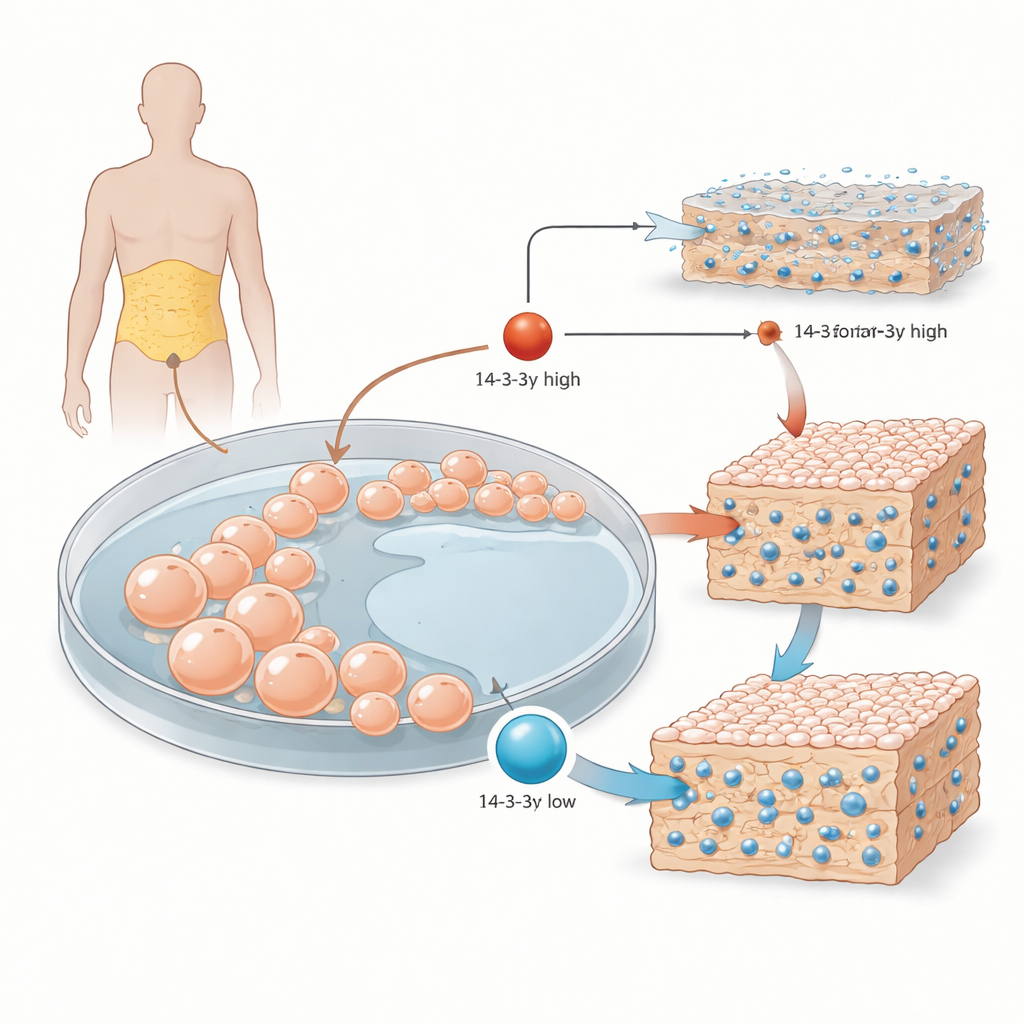
מרקמת שומן לתאים בוני עצם
החוקרים התחילו מתאי סטרומה מזנכימליים שנלקחו מרקמת שומן אנושית. תאים ורסטיליים אלה יכולים להתמיין לעצם, לסחוס או לשומן, בהתאם לאותות שהם מקבלים. במעבדה הצוות חשף אותם לתרכובת סטנדרטית המעודדת יצירת עצם ועקב אחר שלושה שלבים מרכזיים: גדילה מוקדמת, הבשלה של הרקמה התומכת סביב התאים, והקשחת סופית של אותה מטריצה על ידי משקעים מינרליים. הם התמקדו ב‑14-3-3γ, חבר במשפחת חלבונים המשמשת כמארג מולקולרי, נקשרת לשותפים רבים ומכוונת את פעילותם ומיקומם בתוך התא.
בלם משתנה במהלך יצירת העצם
כאשר תאי הגזע הונחו לכיוון תאי עצם, רמות 14-3-3γ לא נשארו קבועות. בשלב האמצעי, כאשר התאים מגבירים את ייצור הקולגן ושאר מרכיבי המטריצה, רמות 14-3-3γ עלו. מאוחר יותר, כאשר המטריצה החלה להקשות על ידי קליטת סידן ופוספט, רמותיו ירדו. תבנית גלים זו הצביעה על כך ש‑14-3-3γ עשוי לכוונן בשלבים שונים של יצירת העצם במקום למלא תפקיד אחד קבוע.
כיבוי העוצמה מקדם ההקשחה
כדי לבחון רעיון זה השתמש הצוות בנגיפים מהנדסים להורדת או להגברת 14-3-3γ בתוך התאים. כאשר 14-3-3γ הומרץ, האנזים המוקדם של העצם בשם אלקלין פוספטאז הפך פעיל יותר, ובשלב ההקשחה המכילה הקולטורה הכילה יותר גבישי סידן וסיבים של קולגן. בניגוד לכך, כופה על התאים לייצר עודף 14-3-3γ הביא להשפעה הפוכה: המטריצה הפכה לעשירה פחות במינרלים וקולגן. באופן מעניין, כמה מתגי הגן הקלאסיים של יצירת עצם, כגון חלבון RUNX2 והגנים לאוסטאוקלצין ואוסטאופונטין, לא עלו וירדו בקורלציה ישירה עם 14-3-3γ, מה שמרמז שחלבון זה פועל דרך מסלולים יותר עדינים מאשר רק הדלקה או כיבוי של גנים מרכזיים.
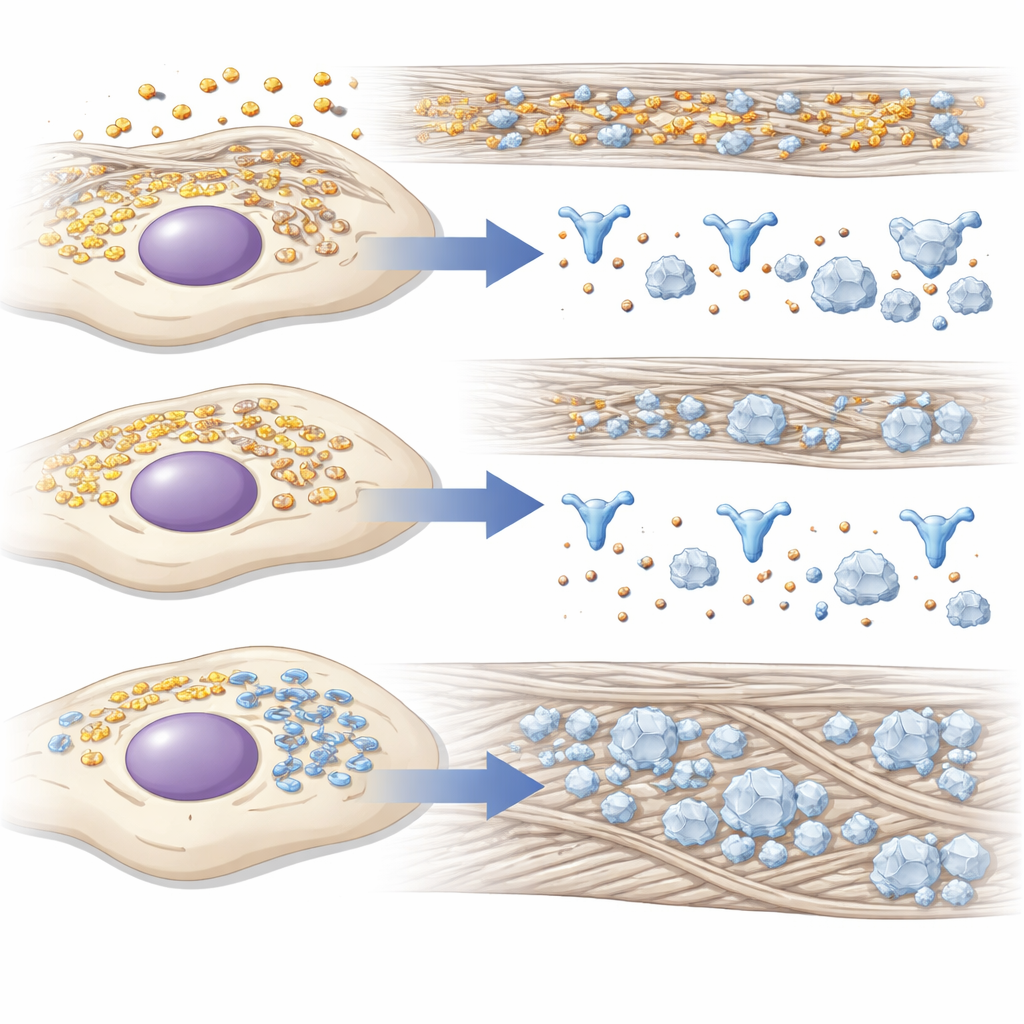
רמזים ממפעל החלבונים של התא
מכיוון שבניית עצם דורשת ייצור מסיבי של חלבונים וטיפול מדויק בסידן ובפוספט, החוקרים בחנו שינויים גלובליים בחלבונים כאשר 14-3-3γ הושתק. באמצעות ספקטרומטריית מסה הם מצאו שחלבונים המקושרים לשימוש באנרגיה ולתגובות לחוסר חמצן נוטים לרדת, בעוד שחלבונים הקשורים לקיפול חלבונים, ללחצים ברשת הממברנות הפנימית של התא ולפיתוח העצם נוטים לעלות. רבים מהחלבונים שעולים מסייעים בקיפול ועיבוד של קולגן מסוג I או בארגונו מחוץ לתא, ויוצרים סוליה טובה יותר למשקעים מינרליים. מיקרוסקופיה הוסיפה שכבה נוספת: במהלך גירוי יצירת העצם, 14-3-3γ עבר מהפצה מפוזרת לריכוז קרוב לרשת האנדופלזמטית, מפעל החלבונים העיקרי של התא, מה שמרמז שהוא מסייע בניהול התנועה ובבקרת האיכות שם.
מה משמעות הדבר לטיפולים עתידיים בעצם
במבט כולל, התוצאות מציירות את 14-3-3γ כבלם פנימי על ההקשחה הסופית של מטריצת העצם. כאשר רמותיו מוקטנות בזמן המתאים, תאי הגזע משקעים יותר קולגן ומינרל, ומתמיינים במלואם לתאים בוני עצם. כאשר רמותיו נשארות גבוהות, הבשלות הזו מעוכבת. מכיוון שניתן כבר למקד חברי משפחת 14-3-3 על ידי מולקולות קטנות, לימוד הדרך לכוונן באופן סלקטיבי את 14-3-3γ בתאי גזע אנושיים עשוי בסופו של דבר לתרום לטיפולים באוסטיאופורוזיס, בשברים שמתרפאים לאט או בהפרעות אחרות שבהן רה‑מודולציה של העצם משתבשת, ובו בזמן להזכיר לנו שגם מארגנים מולקולריים זעירים יכולים להשפיע במידה רבה על בריאות השלד.
ציטוט: Rivera, L., Müller, S., Uhart, M. et al. 14-3-3γ Knockdown promotes matrix mineralization in human mesenchymal stromal cells. Cell Death Dis 17, 415 (2026). https://doi.org/10.1038/s41419-026-08540-4
מילות מפתח: מינרליזציה של עצם, תאי גזע מזנכימליים, אוסטאוגנזה, ספוג רקמת קולגן, חלבוני איתות תאיים