Clear Sky Science · zh
双重抑制 mTOR 与 HSP90 增强顺铂疗效并克服卵巢癌耐药性
这项研究的重要性
上皮性卵巢癌是最致命的妇科恶性肿瘤之一,主要原因是许多肿瘤最终对以顺铂为基础的标准化疗失去反应。一旦出现耐药,治疗选择有限,生存显著下降。本研究探索了一种新策略:同时打击癌细胞内两个关键的应激与生长系统,使顽固肿瘤重新对顺铂敏感。
当常规药物失效时
包括卵巢癌、肺癌和头颈癌在内的多种常见癌症,常使用顺铂及相关铂类药物治疗。这类药物主要通过损伤快速分裂细胞的 DNA,使其走向自我毁灭。然而,随着时间推移,癌细胞会适应:更有效地泵出药物、更好地修复 DNA 损伤或关闭细胞死亡信号,从而产生所谓的铂耐药。在卵巢癌患者中,超过一半最初对治疗反应良好的患者最终以耐药复发,而针对这种耐药性有效的治疗手段稀缺。
发现癌细胞内的隐蔽开关
为了解耐药卵巢癌细胞内发生了哪些变化,研究人员使用了一种称为磷蛋白组学的技术,映射蛋白质上成千上万的化学“开/关”开关。比较铂敏感和铂耐药的卵巢癌细胞系,他们发现有 542 种蛋白存在差异。两个主要的调控枢纽凸显出来:驱动细胞生长与存活的 mTOR 信号通路,以及以转录因子 HSF1 及其伴侣 HSP90、HSP70、HSP40 为核心的应激反应通路,这些伴护蛋白如伴侣蛋白一样稳定许多其他蛋白。在耐药细胞中,这些系统比敏感细胞更为活跃、开关更多;在铂耐药的肺癌细胞和患者的原代细胞中也出现了类似模式。
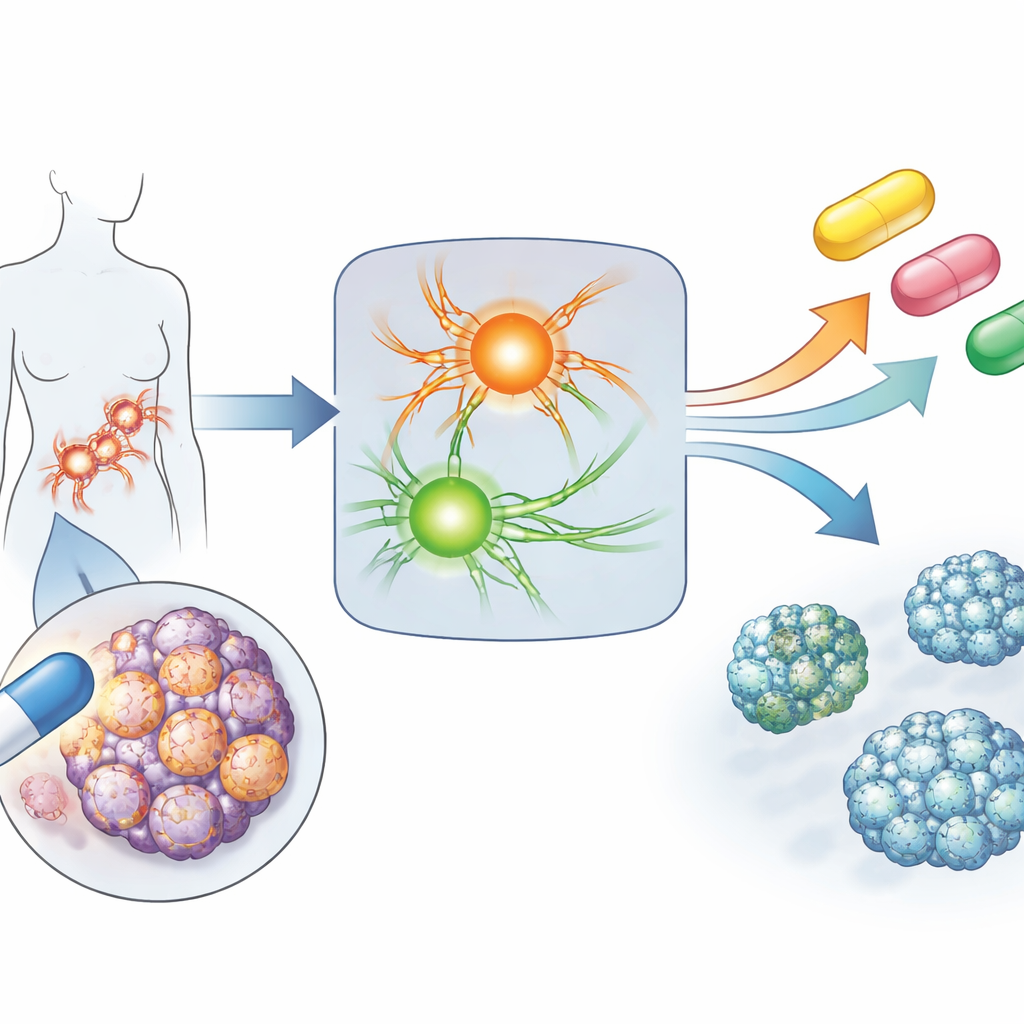
把应激“帮手”变成阿喀琉斯之踵
团队随后检验了关闭这些过度活跃枢纽是否能暴露耐药肿瘤的弱点。他们聚焦于关键伴护蛋白 HSP90 与中心生长调节因子 mTOR。通过基因工程,他们显示去除 HSP90 使耐药的肺癌细胞对顺铂更敏感,而向先前敏感的卵巢癌细胞中强制表达额外的 HSP90 则使其更难被杀死且不易出现 DNA 损伤。这些实验支持了这样一个观点:铂耐药在一定程度上依赖于增强的 HSP90 与 mTOR 活性,耐药细胞可能异常依赖这些通路来应对持续的药物应激。
用三药策略使肿瘤重新变得敏感
基于这些发现,研究人员尝试了一种三管齐下的治疗方案:顺铂联合 ganetespib(一种 HSP90 抑制剂)和 temsirolimus(一种已获部分癌症适应证的 mTOR 抑制剂)。在多种平板培养的卵巢癌模型、能更好模拟真实肿瘤的三维微组织以及携带耐药肿瘤的小鼠模型中,这一三联组合显示出强烈的协同效应。它显著抑制癌细胞生长,几乎消除克隆形成,并导致肿瘤样微组织明显缩小。在携带顺铂耐药的卵巢癌或肺癌移植瘤的小鼠中,三药方案几乎阻止了肿瘤生长,在一个模型中总体肿瘤负荷减少约 85%,并显著延长生存期,同时体重下降可控且未见主要毒性迹象。
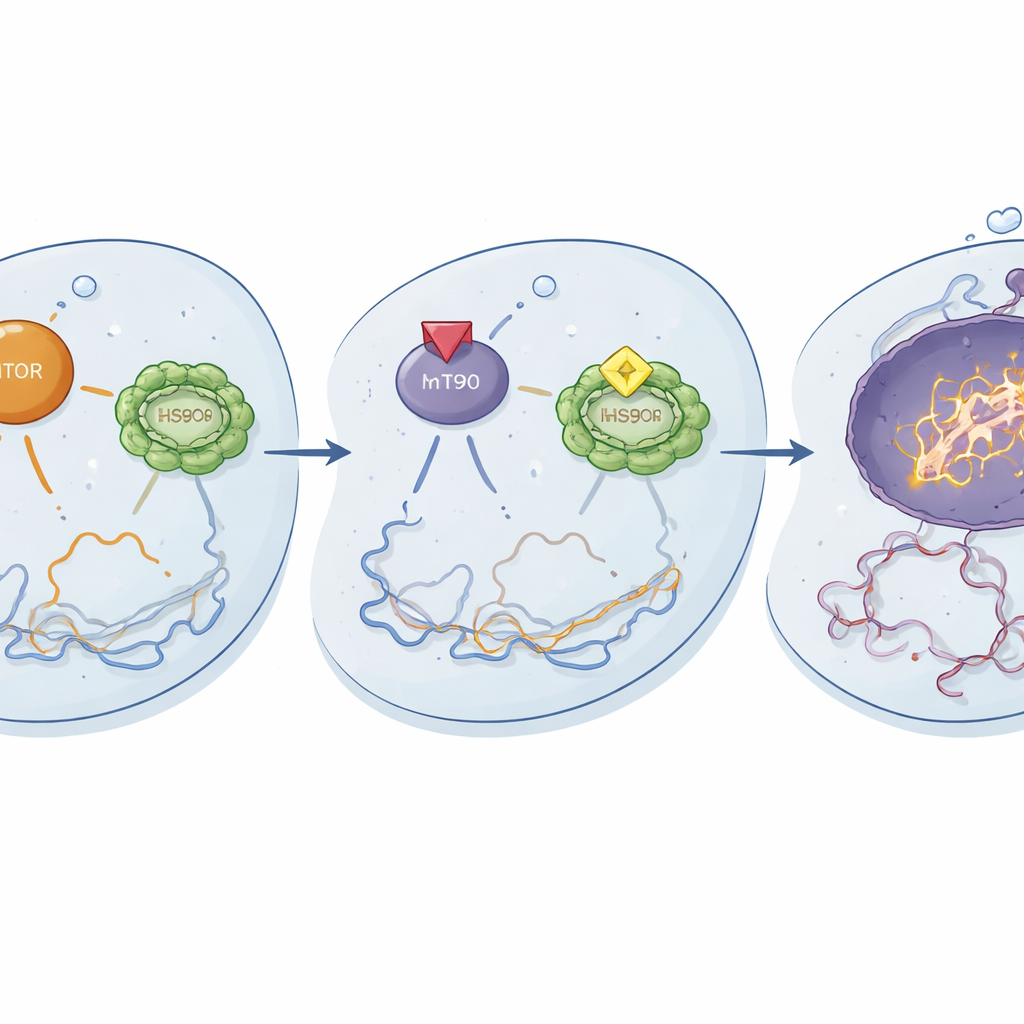
这种新组合在细胞内如何起作用
机制研究揭示了分子水平上的变化。联合使用 ganetespib 和 temsirolimus 能抑制 mTOR 通路关键组分的激活,并降低 HSF1 及其伴护蛋白(包括 HSP90)的活性。这种双重关闭似乎拆解了耐药细胞的重要生存与应激处理电路。因此,顺铂引发了更严重的 DNA 损伤(由更多的 DNA 断裂标志物显示),并触发了更强烈的凋亡——即受控的自毁程序。早期的磷蛋白变化在 24 小时内出现,并在 48 小时变得更明显,表明三联疗法迅速将信号网络从生存导向重编程为细胞死亡。
这对患者可能意味着什么
从实际角度看,这项工作提出了一种新方法,通过利用肿瘤对 mTOR 信号和 HSP90 驱动的应激保护的依赖,来应对对铂化疗失去反应的癌症。尽管先前单独使用 HSP90 或 mTOR 抑制剂的临床试验收效有限,但此处的证据表明,将两者与顺铂联合使用可能使先前耐药的肿瘤重新变得脆弱。作者主张未来 临床研究应在铂耐药的卵巢癌及其他癌种中测试这种三联方案,并优先选择那些肿瘤在这些通路上显示高活性的患者。如果成功,这一策略可能为当前治疗选择有限的患者群体开启延长生存的新途径。
引用: Lombardi, R., Addi, L., Pucci, B. et al. Dual inhibition of mTOR and HSP90 enhances cisplatin efficacy and overcomes resistance in ovarian cancer. Cell Death Dis 17, 417 (2026). https://doi.org/10.1038/s41419-026-08533-3
关键词: 卵巢癌, 顺铂耐药, mTOR 抑制, HSP90 抑制剂, 联合治疗