Clear Sky Science · pt
Inibição dupla de mTOR e HSP90 melhora a eficácia da cisplatina e supera resistência no câncer de ovário
Por que esta pesquisa importa
O carcinoma epitelial de ovário está entre os cânceres ginecológicos mais letais, em grande parte porque muitos tumores acabam deixando de responder à quimioterapia padrão à base do agente de platina cisplatina. Quando essa resistência surge, as opções de tratamento ficam limitadas e a sobrevida cai drasticamente. Este estudo explora uma maneira de tornar novamente sensíveis à cisplatina tumores resistentes, atacando simultaneamente dois sistemas internos chave de estresse e crescimento nas células cancerígenas.
Quando os medicamentos padrão deixam de funcionar
Muitos cânceres comuns, incluindo ovário, pulmão e cabeça e pescoço, são tratados com cisplatina e outros fármacos à base de platina. Esses medicamentos atuam principalmente danificando o DNA de células que se dividem rapidamente, levando-as à autodestruição. Ao longo do tempo, entretanto, as células cancerígenas podem se adaptar. Elas expulsam o fármaco com mais eficiência, reparam melhor os danos ao DNA ou desligam sinais de morte, levando à chamada resistência à platina. Para mulheres com câncer de ovário, mais da metade das que respondem bem inicialmente ao tratamento eventualmente recai com doença resistente, para a qual terapias eficazes são raras.
Encontrando interruptores ocultos dentro das células cancerígenas
Para entender o que muda nas células de câncer de ovário resistentes, os pesquisadores usaram uma técnica chamada fosfoproteômica, que mapeia milhares de “interruptores” químicos de liga/desliga em proteínas. Comparando linhagens de câncer de ovário sensíveis e resistentes à platina, encontraram 542 proteínas que diferiam entre as duas. Dois grandes centros de controle se destacaram: a via de sinalização mTOR, que impulsiona o crescimento e a sobrevivência celular, e uma via de resposta ao estresse centrada no fator HSF1 e suas proteínas auxiliares HSP90, HSP70 e HSP40, que atuam como chaperonas estabilizadoras de muitas outras proteínas. Nas células resistentes, esses sistemas estavam mais ativos e mais fortemente acionados do que nas sensíveis, e padrões semelhantes apareceram em células de câncer de pulmão resistentes à platina e em células primárias de pacientes.
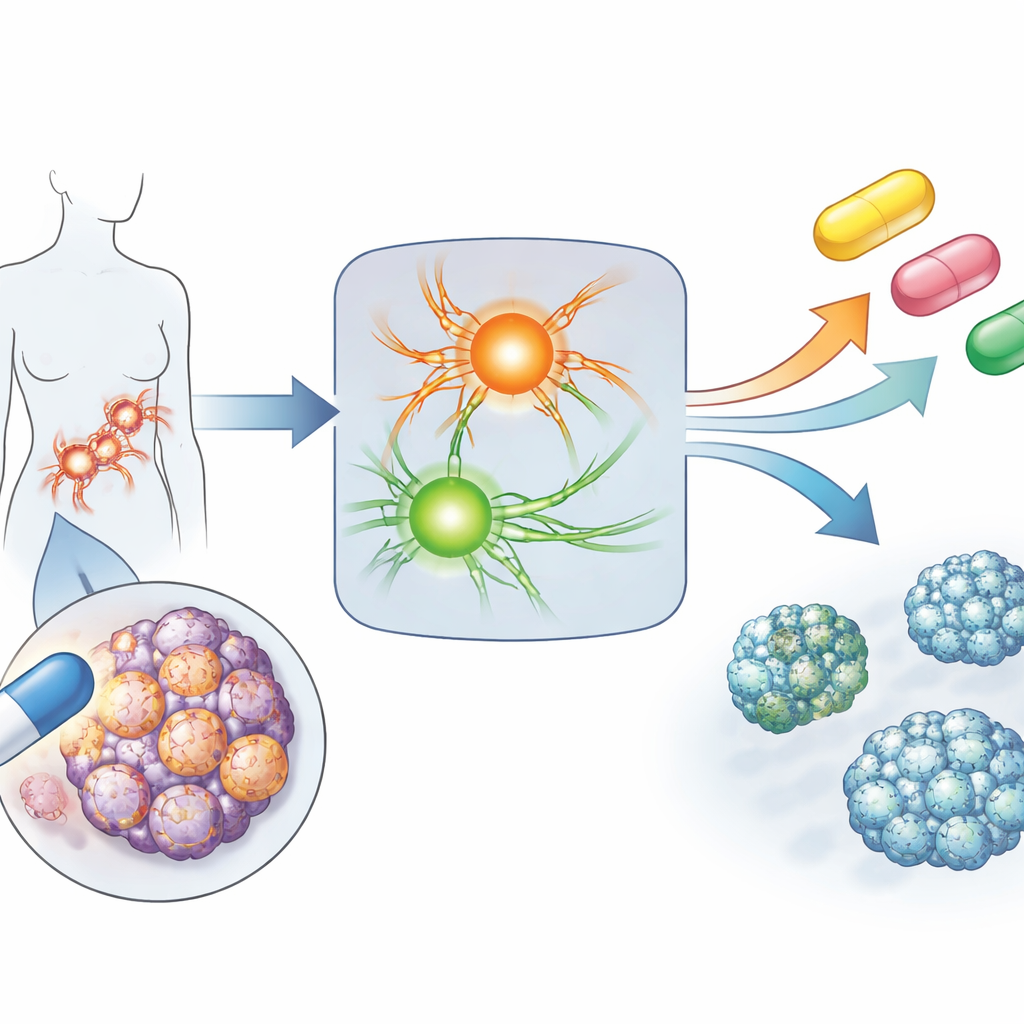
Transformando ajudantes do estresse em um calcanhar de Aquiles
A equipe então testou se desligar esses centros hiperativos poderia expor uma vulnerabilidade nos tumores resistentes. Eles focaram na HSP90, uma chaperona chave, e no mTOR, um regulador central do crescimento. Usando engenharia genética, demonstraram que remover HSP90 tornava células de câncer de pulmão resistentes mais vulneráveis à cisplatina, enquanto forçar a expressão extra de HSP90 em células de câncer de ovário previamente sensíveis as tornava mais difíceis de eliminar e menos propensas a sofrer danos no DNA. Esses experimentos sustentam a ideia de que a resistência à platina depende, ao menos em parte, da atividade aumentada de HSP90 e mTOR e de que as células resistentes podem ser particularmente dependentes dessas vias para sobreviver ao estresse contínuo do fármaco.
Uma estratégia tripla para re-sensibilizar tumores
Com base nesses achados, os pesquisadores testaram um tratamento em três frentes: cisplatina combinada com ganetespibe, um inibidor de HSP90, e temsirolimo, um inibidor de mTOR já aprovado para alguns cânceres. Em múltiplos modelos de câncer de ovário cultivados em placas, em microtecidos tridimensionais que imitam melhor tumores reais, e em camundongos portadores de tumores resistentes, essa combinação tripla mostrou forte sinergia. Reduziu fortemente o crescimento celular, quase eliminou a formação de colônias e causou redução marcante de microtecidos tumorais. Em camundongos com enxertos de câncer de ovário ou de pulmão resistentes à cisplatina, o regime triplo quase interrompeu o crescimento tumoral, diminuiu a carga tumoral total em cerca de 85% em um modelo e prolongou significativamente a sobrevida, tudo com perda de peso aceitável e sem sinais maiores de toxicidade.
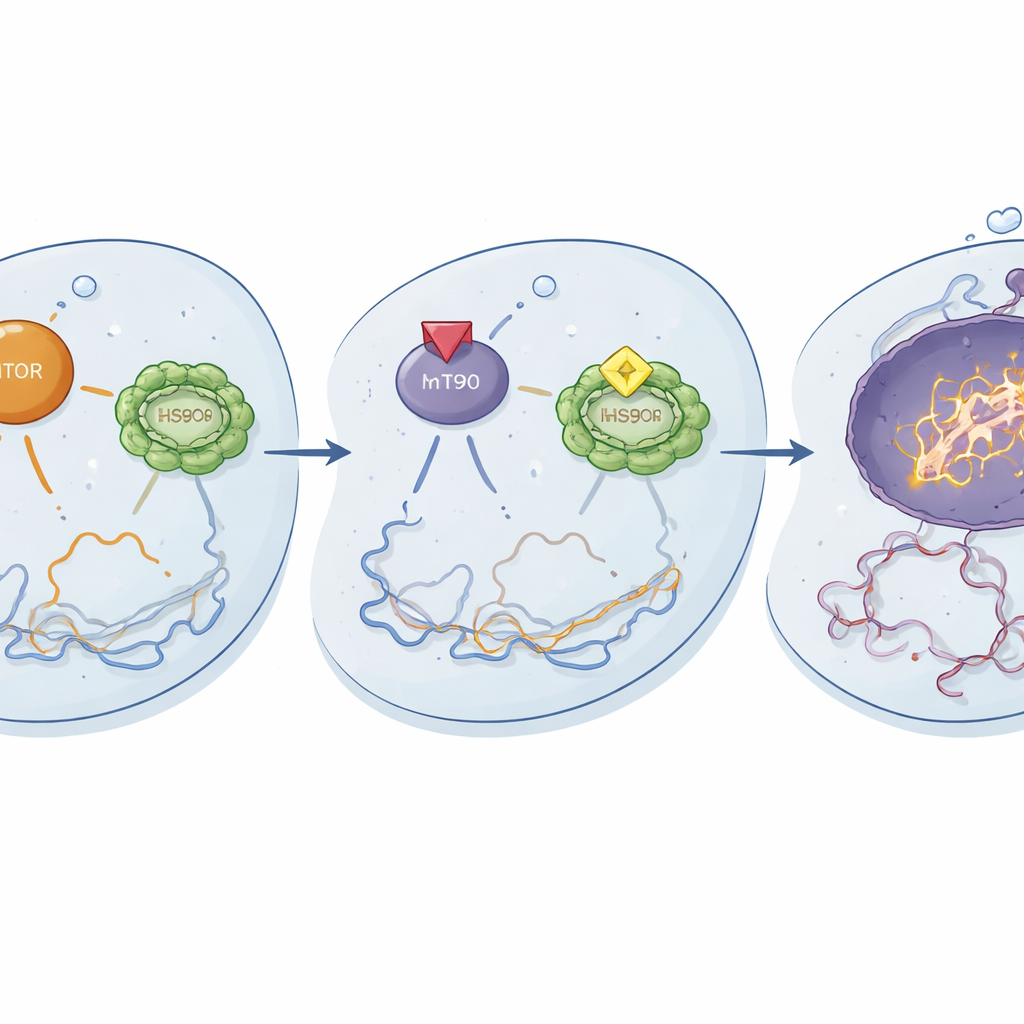
Como a nova combinação age dentro da célula
Estudos mecanísticos revelaram o que ocorria em nível molecular. Quando usados juntos, ganetespibe e temsirolimo reduziram a ativação de componentes-chave da via mTOR e diminuíram a atividade de HSF1 e de suas chaperonas parceiras, incluindo HSP90. Esse desligamento duplo pareceu desmontar circuitos importantes de sobrevivência e manejo de estresse nas células resistentes. Como resultado, a cisplatina causou danos ao DNA mais intensos, evidenciados por aumento de marcadores de quebras de DNA, e desencadeou apoptose mais robusta, o programa controlado de autodestruição. Mudanças iniciais em fosfoproteínas surgiram dentro de 24 horas e se intensificaram em 48 horas, sugerindo que a terapia tripla reconfigura rapidamente as redes de sinalização do lado da sobrevivência para o da morte celular.
O que isso pode significar para pacientes
Na prática, este trabalho propõe uma nova maneira de enfrentar cânceres que não respondem mais à quimioterapia à base de platina, explorando sua dependência da sinalização mTOR e da proteção ao estresse mediada por HSP90. Enquanto testes anteriores com inibidores isolados de HSP90 ou mTOR mostraram benefício limitado, as evidências aqui sugerem que combinar ambos com cisplatina pode converter um tumor previamente resistente em um que volta a ser vulnerável ao tratamento. Os autores defendem que futuros estudos clínicos devem avaliar essa abordagem tripla em pacientes com câncer de ovário e outros tumores resistentes à platina, idealmente selecionando aqueles cujos tumores exibam alta atividade nessas vias. Se bem-sucedida, essa estratégia poderia abrir uma nova via para estender a vida de pacientes com poucas opções atualmente.
Citação: Lombardi, R., Addi, L., Pucci, B. et al. Dual inhibition of mTOR and HSP90 enhances cisplatin efficacy and overcomes resistance in ovarian cancer. Cell Death Dis 17, 417 (2026). https://doi.org/10.1038/s41419-026-08533-3
Palavras-chave: câncer de ovário, resistência à cisplatina, inibição de mTOR, inibidores de HSP90, terapia combinada