Clear Sky Science · ru
Двойное подавление mTOR и HSP90 усиливает эффективность цисплатина и преодолевает резистентность при раке яичников
Почему это исследование важно
Эпителиальный рак яичников — один из наиболее смертоносных гинекологических злокачественных новообразований, во многом потому, что многие опухоли со временем перестают отвечать на стандартную химиотерапию на основе платиносодержащего препарата цисплатина. После появления такой резистентности варианты лечения ограничены, и выживаемость резко снижается. В этом исследовании изучается новый подход, который снова сделать стойкие опухоли чувствительными к цисплатину, одновременно воздействуя на две ключевые внутриклеточные системы стресса и роста.
Когда стандартные препараты перестают действовать
Многие распространённые виды рака, включая рак яичников, лёгких и головы и шеи, лечат цисплатином и связанными с ним платиновыми препаратами. Эти препараты в основном действуют, повреждая ДНК быстро делящихся клеток и направляя их на путь самоуничтожения. Со временем клетки рака могут адаптироваться: они более эффективно выкачивают препарат, лучше восстанавливают повреждения ДНК или отключают сигналы гибели, что приводит к так называемой платиновой резистентности. Для женщин с раком яичников более половины тех, кто изначально хорошо ответил на лечение, в итоге рецидивируют с резистентной болезнью, для которой эффективных терапий мало.
Поиск скрытых переключателей внутри раковых клеток
Чтобы понять, что меняется в резистентных клетках рака яичников, исследователи использовали метод фосфопротеомики, который картирует тысячи химических «вкл/выкл» переключателей на белках. Сравнивая клетки, чувствительные и резистентные к платиноидам, они выявили 542 белка с различиями между двумя группами. Выделились два крупных контрольных узла: сигнальный путь mTOR, обеспечивающий рост и выживание клеток, и стресс-ответ, сосредоточенный вокруг фактора HSF1 и его шаперонов HSP90, HSP70 и HSP40, которые стабилизируют множество других белков. В резистентных клетках эти системы были более активны и сильнее «включены», чем в чувствительных, а схожие закономерности наблюдались в резистентных к платиноидам клетках лёгкого и в первичных клетках пациентов.
Превращение помощников при стрессе в ахиллесову пяту
Команда затем проверила, не откроет ли выключение этих сверхактивных узлов слабое место резистентных опухолей. Они сосредоточились на HSP90, ключевом шапероне, и mTOR, центральном регуляторе роста. С помощью генной инженерии показали, что удаление HSP90 делает резистентные клетки рака лёгкого более уязвимыми к цисплатину, тогда как принудительное увеличение HSP90 в ранее чувствительных клетках рака яичников делает их труднее убиваемыми и снижает склонность к повреждению ДНК. Эти эксперименты поддерживают идею, что платиновая резистентность частично опирается на усиленную активность HSP90 и mTOR, и что резистентные клетки могут особенно зависеть от этих путей для выживания при продолжающемся лекарственном стрессе.
Тройная стратегия для повторного восстановления чувствительности опухолей
Опираясь на эти находки, исследователи испробовали трёхзвенную терапию: цисплатин в сочетании с ганетеспибом, ингибитором HSP90, и темсиролимусом, ингибитором mTOR, уже одобренным для некоторых видов рака. В нескольких моделях рака яичников в культурах, в трёхмерных микротканевых структурах, которые лучше имитируют настоящие опухоли, и у мышей с резистентными опухолями эта тройная комбинация показала сильную синергию. Она резко сократила рост раковых клеток, почти устранила формирование колоний и вызвала заметное уменьшение микротканевых структур, подобным опухолям. У мышей с трансплантатами резистентного рака яичников или лёгких режим из трёх препаратов почти остановил рост опухоли, уменьшил общую опухолевую нагрузку примерно на 85 % в одной модели и существенно продлил выживание при приемлемой потере веса и без серьёзных признаков токсичности.
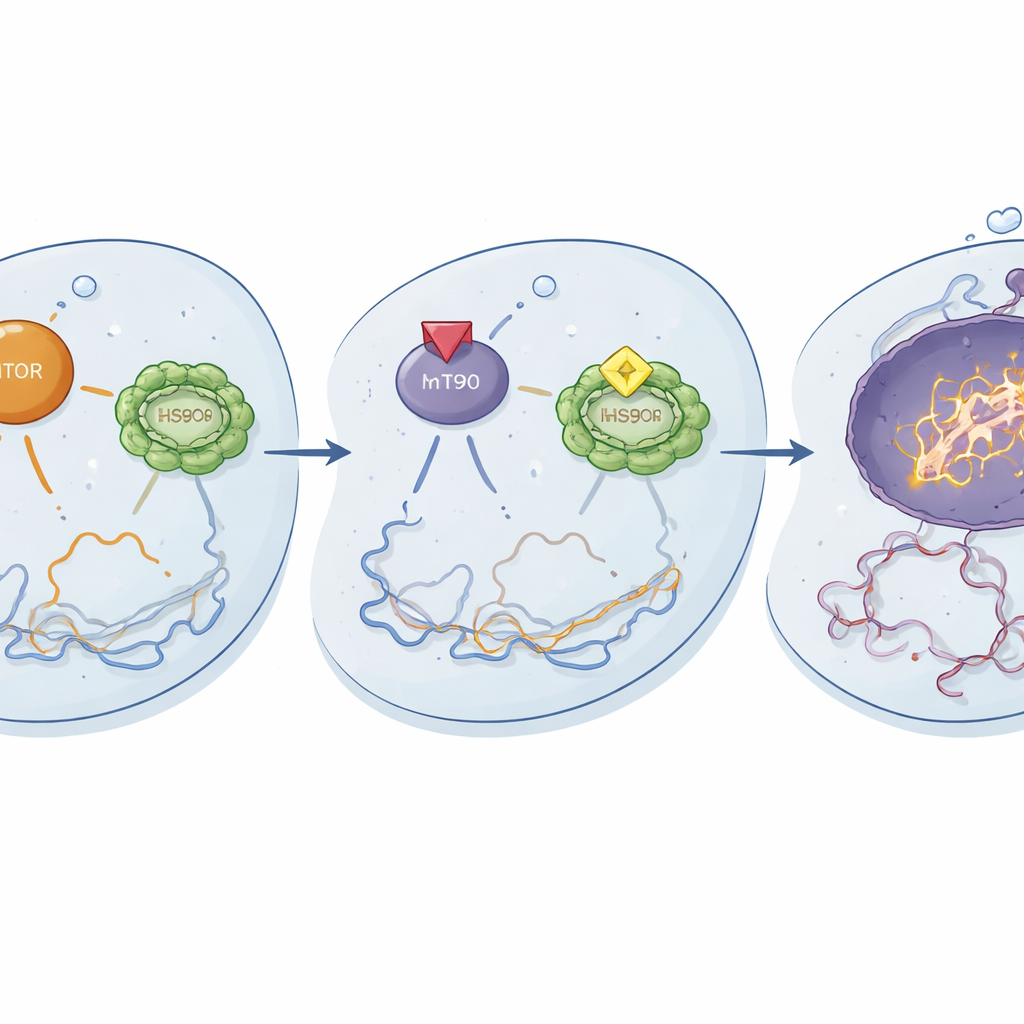
Как новая комбинация действует внутри клетки
Механистические исследования показали молекулярные основания этих эффектов. При совместном применении ганетеспиб и темсиролимус уменьшали активацию ключевых компонентов пути mTOR и снижали активность HSF1 и его шаперонов, включая HSP90. Это двойное отключение, по-видимому, разрушало важные цепи выживания и управления стрессом в резистентных клетках. В результате цисплатин вызывал более интенсивные повреждения ДНК, что подтверждалось увеличением маркеров разрывов ДНК, и провоцировал более выраженную апоптозу, программу контролируемого самоуничтожения. Ранние изменения фосфопротеинов появлялись в течение 24 часов и становились более выраженными к 48 часам, что указывает на то, что тройная терапия быстро перенастраивает сигнальные сети в сторону гибели клетки, а не выживания.
Что это может значить для пациентов
С практической точки зрения эта работа предлагает новый способ бороться с опухолями, которые больше не реагируют на платиновую химиотерапию, используя их зависимость от сигнaling mTOR и HSP90‑опосредованной защиты от стресса. В то время как ранние испытания ингибиторов HSP90 или mTOR по отдельности дали ограниченные преимущества, представленные данные указывают, что сочетание обоих с цисплатином может превратить ранее резистентную опухоль обратно в уязвимую для лечения. Авторы предлагают, чтобы будущие клинические исследования проверили этот тройной подход у пациентов с платинорезистентным раком яичников и другими опухолями, по возможности отбирая тех, чьи опухоли демонстрируют высокую активность этих путей. В случае успеха такая стратегия могла бы открыть новый путь для продления жизни пациентов, у которых сейчас мало вариантов терапии.
Цитирование: Lombardi, R., Addi, L., Pucci, B. et al. Dual inhibition of mTOR and HSP90 enhances cisplatin efficacy and overcomes resistance in ovarian cancer. Cell Death Dis 17, 417 (2026). https://doi.org/10.1038/s41419-026-08533-3
Ключевые слова: рак яичников, резистентность к цисплатину, ингибирование mTOR, ингибиторы HSP90, комбинированная терапия