Clear Sky Science · fr
Double inhibition de mTOR et HSP90 améliore l’efficacité du cisplatine et surmonte la résistance dans le cancer de l’ovaire
Pourquoi cette recherche est importante
Le carcinome épithélial de l’ovaire est l’un des cancers gynécologiques les plus mortels, en grande partie parce que de nombreuses tumeurs finissent par ne plus répondre à la chimiothérapie standard à base de cisplatine. Une fois cette résistance installée, les options thérapeutiques sont limitées et la survie chute fortement. Cette étude explore une nouvelle approche pour rendre à nouveau sensibles au cisplatine des tumeurs réfractaires en ciblant simultanément deux systèmes internes clés de stress et de croissance des cellules cancéreuses.
Quand les médicaments standards cessent de fonctionner
De nombreux cancers fréquents, dont les cancers de l’ovaire, du poumon et des voies aérodigestives supérieures, sont traités par le cisplatine et des composés apparentés. Ces médicaments agissent principalement en endommageant l’ADN des cellules à division rapide, les poussant vers l’autodestruction. Avec le temps, cependant, les cellules cancéreuses peuvent s’adapter. Elles expulsent le médicament plus efficacement, réparent mieux les lésions de l’ADN ou désactivent les signaux de mort, aboutissant à la résistance aux platines. Pour les patientes atteintes d’un cancer de l’ovaire, plus de la moitié de celles qui répondent initialement bien au traitement rechutent ensuite avec une maladie résistante, pour laquelle les thérapies efficaces sont rares.
Trouver des interrupteurs cachés à l’intérieur des cellules cancéreuses
Pour comprendre ce qui change dans les cellules de cancer de l’ovaire résistantes, les chercheurs ont utilisé une technique appelée phosphoprotéomique, qui cartographie des milliers d’interrupteurs chimiques « on/off » sur les protéines. En comparant des lignées cellulaires sensibles et résistantes aux platines, ils ont identifié 542 protéines différentielles. Deux principaux centres de contrôle se sont détachés : la voie de signalisation mTOR, qui stimule la croissance et la survie cellulaires, et une voie de réponse au stress centrée sur le facteur HSF1 et ses protéines auxiliaires HSP90, HSP70 et HSP40, qui agissent comme des chaperons stabilisant de nombreuses autres protéines. Dans les cellules résistantes, ces systèmes étaient plus actifs et davantage activés que dans leurs homologues sensibles, et des schémas similaires ont été observés dans des cellules de cancer du poumon résistantes aux platines et dans des cellules primaires issues de patientes.
Transformer les chaperons de stress en talon d’Achille
L’équipe a ensuite testé si l’inhibition de ces centres hyperactifs pouvait révéler une faiblesse dans les tumeurs résistantes. Elle s’est concentrée sur HSP90, un chaperon clé, et mTOR, un régulateur central de la croissance. Par ingénierie génétique, ils ont montré que la suppression de HSP90 rendait les cellules de cancer du poumon résistantes plus vulnérables au cisplatine, tandis que la surexpression de HSP90 dans des cellules d’ovaire auparavant sensibles les rendait plus difficiles à tuer et moins sujettes aux dommages de l’ADN. Ces expériences étayent l’idée que la résistance aux platines dépend, au moins en partie, d’une activité accrue de HSP90 et de mTOR et que les cellules résistantes peuvent être particulièrement dépendantes de ces voies pour survivre au stress médicamenteux.
Une stratégie à trois médicaments pour resensibiliser les tumeurs
À partir de ces éléments, les chercheurs ont testé un traitement à trois volets : le cisplatine associé au ganetespib, un inhibiteur de HSP90, et au temsirolimus, un inhibiteur de mTOR déjà approuvé pour certains cancers. Dans plusieurs modèles de cancer de l’ovaire cultivés en milieu cellulaire, dans des microtissus tridimensionnels qui reproduisent mieux les tumeurs réelles, et chez des souris porteuses de tumeurs résistantes, cette combinaison triple a montré une synergie marquée. Elle a fortement réduit la croissance cellulaire, presque éliminé la formation de colonies et provoqué un rétrécissement notable des microtissus tumoraux. Chez des souris greffées avec des tumeurs d’ovaire ou du poumon résistantes au cisplatine, le régime triple a quasiment arrêté la croissance tumorale, réduit la charge tumorale globale d’environ 85 % dans un modèle et prolongé significativement la survie, le tout avec une perte de poids acceptable et sans signes majeurs de toxicité.
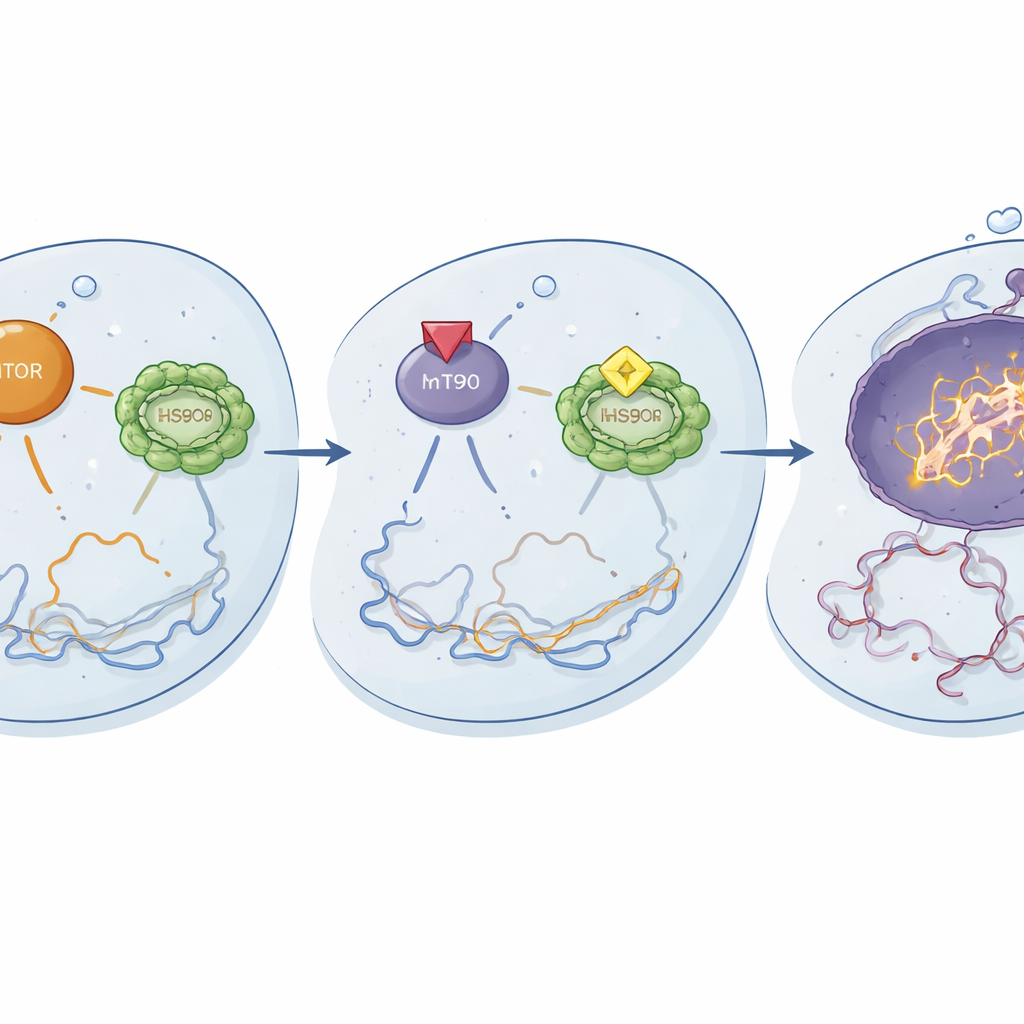
Comment la nouvelle combinaison agit à l’intérieur de la cellule
Des études mécanistiques ont révélé ce qui se passait au niveau moléculaire. Utilisés ensemble, le ganetespib et le temsirolimus ont atténué l’activation des composantes clés de la voie mTOR et réduit l’activité de HSF1 et de ses partenaires chaperons, dont HSP90. Cette double inhibition semblait démanteler des circuits essentiels de survie et de gestion du stress dans les cellules résistantes. En conséquence, le cisplatine a provoqué des dommages à l’ADN plus intenses, comme en témoignent des marqueurs accrus de cassures d’ADN, et déclenché une apoptose plus prononcée, le programme d’autodestruction contrôlée. Des changements précoces de phosphoprotéines sont apparus dès 24 heures et se sont accentués à 48 heures, suggérant que la thérapie triple reconfigure rapidement les réseaux de signalisation, les détournant de la survie vers la mort cellulaire.
Ce que cela pourrait signifier pour les patientes
Concrètement, ce travail propose une nouvelle façon d’attaquer des cancers qui ne répondent plus à la chimiothérapie aux platines en exploitant leur dépendance au signalement mTOR et à la protection contre le stress pilotée par HSP90. Alors que des essais antérieurs d’inhibiteurs de HSP90 ou de mTOR seuls ont montré un bénéfice limité, les preuves présentées ici suggèrent que la combinaison des deux avec le cisplatine pourrait reconvertir une tumeur auparavant résistante en une tumeur vulnérable au traitement. Les auteurs estiment que des études cliniques futures devraient tester cette approche triple chez des patientes atteintes de cancers résistants aux platines, idéalement en sélectionnant celles dont les tumeurs présentent une activité élevée de ces voies. Si elle se révèle efficace, une telle stratégie pourrait ouvrir une nouvelle voie pour prolonger la vie de patientes pour lesquelles les options actuelles sont peu nombreuses.
Citation: Lombardi, R., Addi, L., Pucci, B. et al. Dual inhibition of mTOR and HSP90 enhances cisplatin efficacy and overcomes resistance in ovarian cancer. Cell Death Dis 17, 417 (2026). https://doi.org/10.1038/s41419-026-08533-3
Mots-clés: cancer de l’ovaire, résistance au cisplatine, inhibition de mTOR, inhibiteurs de HSP90, thérapie combinée