Clear Sky Science · it
Doppia inibizione di mTOR e HSP90 potenzia l’efficacia del cisplatino e supera la resistenza nel carcinoma ovarico
Perché questa ricerca è importante
Il carcinoma ovarico epiteliale è uno dei tumori ginecologici più letali, in gran parte perché molti tumori finiscono per non rispondere più alla chemioterapia standard a base del farmaco al platino cisplatino. Quando si sviluppa questa resistenza, le opzioni terapeutiche sono limitate e la sopravvivenza diminuisce rapidamente. Questo studio esplora un nuovo modo per rendere nuovamente sensibili al cisplatino i tumori difficili, colpendo simultaneamente due sistemi interni chiave per la gestione dello stress e la crescita delle cellule cancerose.
Quando i farmaci standard smettono di funzionare
Molti tumori comuni, compresi quelli ovarici, polmonari e della testa e del collo, vengono trattati con cisplatino e farmaci correlati a base di platino. Questi agenti agiscono principalmente danneggiando il DNA delle cellule che si dividono rapidamente, spingendole verso l’autodistruzione. Col tempo, però, le cellule tumorali possono adattarsi. Possono espellere il farmaco più efficacemente, riparare meglio i danni al DNA o disattivare i segnali di morte cellulare, portando alla cosiddetta resistenza al platino. Nelle donne con carcinoma ovarico, più della metà di quelle che rispondono inizialmente bene alla terapia va incontro a recidiva con malattia resistente, per la quale le terapie efficaci sono scarse.
Trovare interruttori nascosti all’interno delle cellule tumorali
Per capire cosa cambiava nelle cellule del carcinoma ovarico resistenti, i ricercatori hanno utilizzato una tecnica chiamata fosfoproteomica, che mappa migliaia di interruttori chimici "on/off" sulle proteine. Confrontando linee cellulari sensibili e resistenti al platino, hanno individuato 542 proteine che differivano tra le due. Sono emersi due principali nodi di controllo: la via di segnalazione mTOR, che guida crescita e sopravvivenza cellulare, e una via di risposta allo stress centrata sul fattore HSF1 e sui suoi coadiuvanti HSP90, HSP70 e HSP40, che agiscono come chaperoni stabilizzando molte altre proteine. Nelle cellule resistenti, questi sistemi risultavano più attivi e maggiormente attivati rispetto ai corrispondenti sensibili, e pattern simili sono stati osservati in cellule di carcinoma polmonare resistenti al platino e in cellule primarie prelevate dai pazienti.
Trasformare i chaperoni dello stress in un tallone d’Achille
Il gruppo ha quindi testato se spegnere questi hub iperattivi potesse rivelare una vulnerabilità nei tumori resistenti. Si sono concentrati su HSP90, un chaperone chiave, e su mTOR, un regolatore centrale della crescita. Mediante ingegneria genetica hanno dimostrato che l’eliminazione di HSP90 rendeva le cellule di carcinoma polmonare resistenti più vulnerabili al cisplatino, mentre l’espressione forzata di HSP90 in cellule ovariche precedentemente sensibili le rendeva più difficili da eliminare e meno soggette a danni al DNA. Questi esperimenti supportano l’idea che la resistenza al platino dipenda, almeno in parte, dall’aumentata attività di HSP90 e mTOR e che le cellule resistenti possano essere particolarmente dipendenti da queste vie per sopravvivere allo stress farmacologico continuo.
Una strategia tripletta per ri-sensibilizzare i tumori
Basandosi su queste intuizioni, i ricercatori hanno testato una terapia a tre punte: cisplatino combinato con ganetespib, un inibitore di HSP90, e temsirolimus, un inibitore di mTOR già approvato per alcuni tumori. In molteplici modelli di carcinoma ovarico coltivati in piastre, in microtessuti tridimensionali che riproducono meglio i tumori reali e in topi portatori di tumori resistenti, questa combinazione tripla ha mostrato una forte sinergia. Ha ridotto drasticamente la crescita cellulare, quasi eliminato la formazione di colonie e causato un marcato restringimento dei microtessuti simili a tumori. In topi con innesti di carcinoma ovarico o polmonare resistenti al cisplatino, il regime a tre farmaci ha quasi arrestato la crescita tumorale, ridotto il carico tumorale complessivo di circa l’85% in un modello e prolungato significativamente la sopravvivenza, il tutto con cali di peso accettabili e senza segni evidenti di tossicità grave.
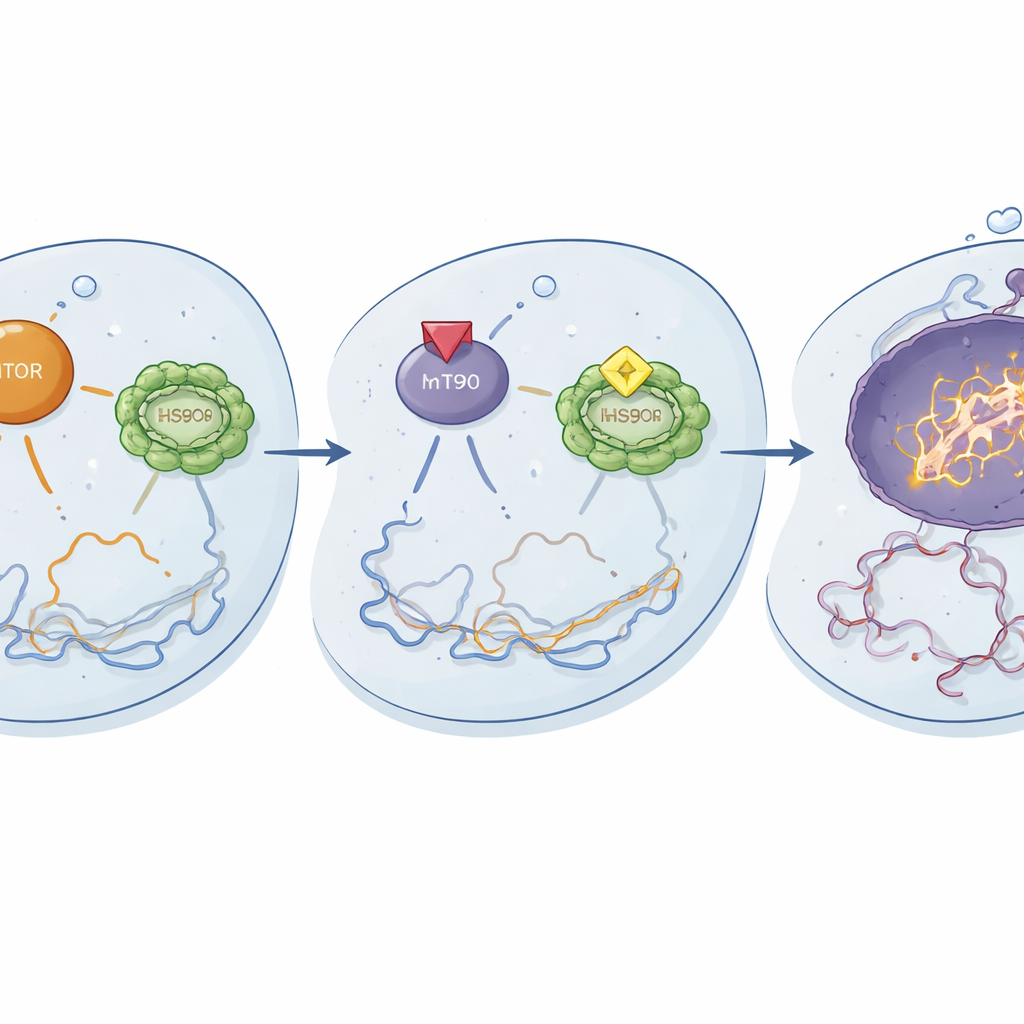
Come funziona la nuova combinazione all’interno della cellula
Studi meccanicistici hanno rivelato cosa succedeva a livello molecolare. Quando usati insieme, ganetespib e temsirolimus attenuavano l’attivazione di componenti chiave della via mTOR e riducevano l’attività di HSF1 e dei suoi partner chaperoni, incluso HSP90. Questo doppio spegnimento pareva smantellare circuiti importanti per la sopravvivenza e la gestione dello stress nelle cellule resistenti. Di conseguenza, il cisplatino provocava danni al DNA più intensi, come mostrato dall’aumento dei marcatori di rottura del DNA, e innescava un’apoptosi più marcata, il programma di autodistruzione controllata. I primi cambiamenti nei fosfoproteine apparivano entro 24 ore e si accentuavano a 48 ore, suggerendo che la terapia tripla riorganizza rapidamente le reti di segnalazione spostandole dalla sopravvivenza verso la morte cellulare.
Cosa potrebbe significare per i pazienti
In termini pratici, questo lavoro propone un nuovo approccio per affrontare i tumori che non rispondono più alla chemioterapia a base di platino sfruttando la loro dipendenza dalla segnalazione mTOR e dalla protezione contro lo stress mediata da HSP90. Sebbene studi precedenti su inibitori di HSP90 o di mTOR singolarmente abbiano mostrato benefici limitati, le prove qui presentate suggeriscono che combinare entrambi con il cisplatino potrebbe convertire un tumore precedentemente resistente in uno nuovamente vulnerabile al trattamento. Gli autori sostengono che futuri studi clinici dovrebbero testare questo approccio triplo nei pazienti con tumori resistenti al platino, idealmente selezionando quelli i cui tumori mostrano elevata attività in queste vie. Se avrà successo, una tale strategia potrebbe aprire una nuova via per prolungare la vita di pazienti per i quali le opzioni attuali sono poche.
Citazione: Lombardi, R., Addi, L., Pucci, B. et al. Dual inhibition of mTOR and HSP90 enhances cisplatin efficacy and overcomes resistance in ovarian cancer. Cell Death Dis 17, 417 (2026). https://doi.org/10.1038/s41419-026-08533-3
Parole chiave: carcinoma ovarico, resistenza al cisplatino, inibizione di mTOR, inibitori di HSP90, terapia combinata