Clear Sky Science · pl
Podwójna inhibicja mTOR i HSP90 zwiększa skuteczność cisplatyny i pokonuje oporność w raku jajnika
Dlaczego te badania są ważne
Rak nabłonkowy jajnika jest jednym z najbardziej śmiertelnych nowotworów ginekologicznych, głównie dlatego, że wiele guzów ostatecznie przestaje reagować na standardową chemioterapię opartą na leku platynowym — cisplatynie. Gdy pojawia się ta oporność, opcje leczenia są ograniczone, a przeżycie drastycznie spada. W pracy tej badacze sprawdzają nową strategię przywracania wrażliwości opornych guzów na cisplatynę poprzez jednoczesne uderzenie w dwa kluczowe wewnątrzkomórkowe systemy odpowiedzialne za stres i wzrost komórek nowotworowych.
Kiedy standardowe leki przestają działać
Wiele powszechnych nowotworów, w tym rak jajnika, płuc i nowotwory głowy i szyi, leczonych jest cisplatyną i pokrewnymi lekami platynowymi. Działają one głównie przez uszkadzanie DNA szybko dzielących się komórek, popychając je w kierunku samodestrukcji. Z czasem jednak komórki nowotworowe potrafią się adaptować. Skuteczniej wypompowują lek, sprawniej naprawiają uszkodzenia DNA lub wyłączają sygnały śmierci, co prowadzi do tzw. oporności platynowej. U pacjentek z rakiem jajnika ponad połowa tych, które początkowo dobrze reagowały na leczenie, ostatecznie ma nawrót choroby opornej — dla której skuteczne terapie są rzadkie.
Odnajdywanie ukrytych przełączników w komórkach nowotworowych
Aby zrozumieć, co zmienia się w komórkach opornych, badacze zastosowali technikę fosfoproteomiki, która mapuje tysiące chemicznych „włączników/wyłączników” na białkach. Porównując linie komórkowe wrażliwe i oporne na platynę, znaleziono 542 białka różniące się między nimi. Wyraźnie wyróżniły się dwa główne węzły kontrolne: szlak sygnałowy mTOR, który napędza wzrost i przetrwanie komórek, oraz odpowiedź na stres skupiona wokół czynnika HSF1 i jego współpracowników HSP90, HSP70 i HSP40 — białek opiekuńczych stabilizujących wiele innych białek. W komórkach opornych te systemy były bardziej aktywne i silniej włączone niż w komórkach wrażliwych, a podobne wzorce zaobserwowano w opornych komórkach raka płuca oraz w komórkach pierwotnych pochodzących od pacjentów.
Przemiana „pomocników stresu” w piętę Achillesową
Zespół sprawdził następnie, czy wyłączenie tych nadaktywowanych węzłów ujawni słabość w opornych guzach. Skoncentrowano się na HSP90, kluczowym białku opiekuńczym, oraz mTOR, centralnym regulatorze wzrostu. Dzięki inżynierii genetycznej wykazano, że usunięcie HSP90 zwiększa wrażliwość opornych komórek raka płuca na cisplatynę, podczas gdy wprowadzenie nadmiaru HSP90 do wcześniej wrażliwych komórek raka jajnika czyniło je trudniejszymi do zabicia i mniej podatnymi na uszkodzenia DNA. Eksperymenty te potwierdziły koncepcję, że oporność na platynę zależy przynajmniej częściowo od zwiększonej aktywności HSP90 i mTOR, a komórki oporne mogą być szczególnie zależne od tych szlaków, by przetrwać ciągły stres wywołany lekiem.
Strategia potrójnej terapii przywracająca wrażliwość guzów
Na podstawie tych obserwacji badacze zastosowali trójelementowe leczenie: cisplatynę w połączeniu z ganetespibem — inhibitorem HSP90 — oraz temsirolimusem — inhibitorem mTOR zatwierdzonym już w niektórych nowotworach. W wielu modelach raka jajnika hodowanych na płytce, w trójwymiarowych mikrostrukturach lepiej naśladujących rzeczywiste guzy oraz u myszy z opornymi nowotworami, to potrójne połączenie wykazało silną synergię. Znacząco zahamowało wzrost komórek nowotworowych, niemal wyeliminowało formowanie kolonii i spowodowało wyraźne kurczenie się mikrostruktur przypominających guzy. U myszy z przeszczepami opornymi na cisplatynę raka jajnika lub płuca, schemat trzech leków niemal zatrzymał wzrost guza, zmniejszył łączny ciężar nowotworu o około 85% w jednym modelu i istotnie wydłużył przeżycie, przy akceptowalnej utracie masy ciała i bez poważnych objawów toksyczności.
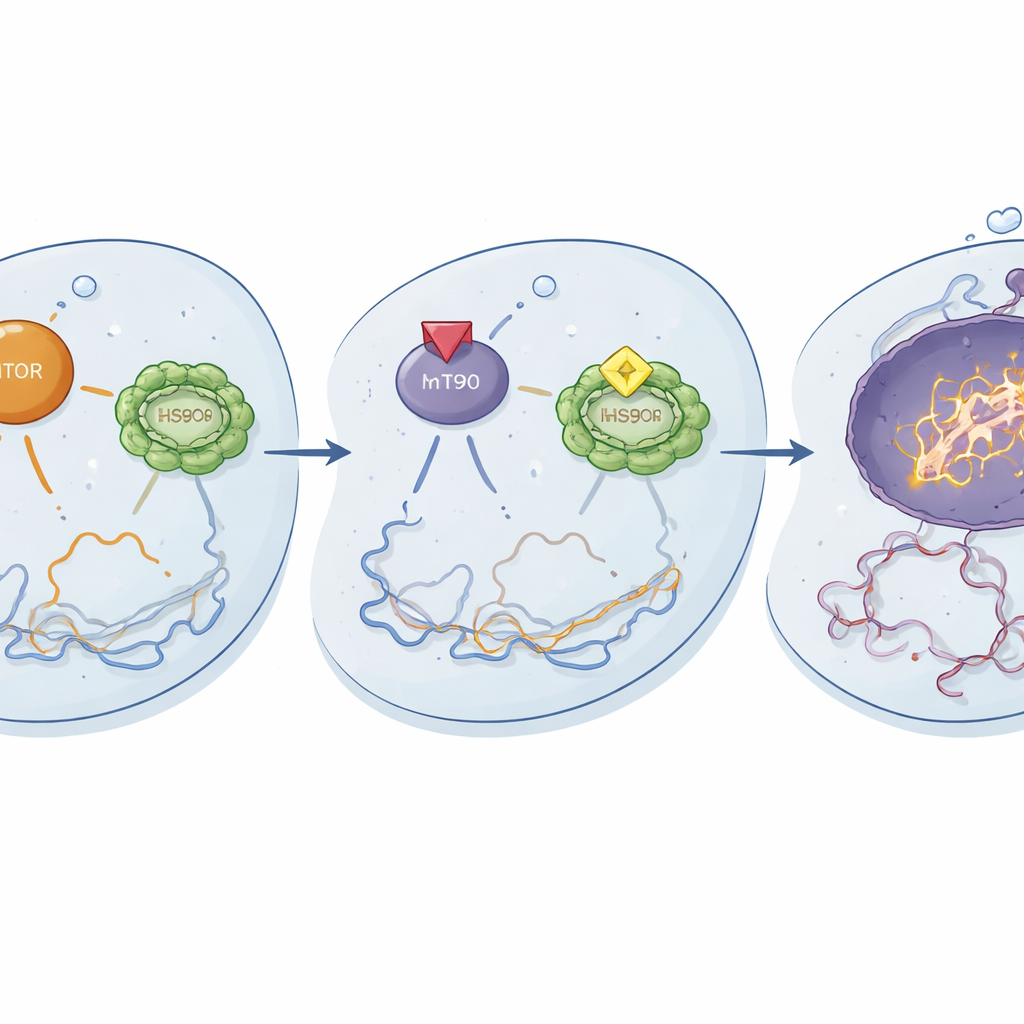
Jak nowe połączenie działa wewnątrz komórki
Badania mechanistyczne ujawniły, co działo się na poziomie molekularnym. Stosowane razem ganetespib i temsirolimus tłumiły aktywację kluczowych składników szlaku mTOR i zmniejszały aktywność HSF1 oraz jego partnerów opiekuńczych, w tym HSP90. Ta podwójna blokada zdawała się rozmontowywać ważne obwody przetrwania i radzenia sobie ze stresem w komórkach opornych. W efekcie cisplatyna powodowała silniejsze uszkodzenia DNA, co ilustrował wzrost markerów pęknięć DNA, i wywoływała silniejszą apoptozę — kontrolowany program samobójczy komórki. Wczesne zmiany w fosfoproteinach pojawiały się w ciągu 24 godzin i nasilały się do 48 godzin, co sugeruje, że potrójna terapia szybko przestawia sieci sygnałowe z utrzymania przy życiu na ścieżki prowadzące do śmierci komórkowej.
Co to może znaczyć dla pacjentów
W praktycznym ujęciu praca ta proponuje nowy sposób radzenia sobie z nowotworami, które przestały reagować na chemioterapię platynową, wykorzystując ich zależność od sygnalizacji mTOR i ochrony przed stresem napędzanej przez HSP90. Chociaż wcześniejsze próby kliniczne z inhibitorami HSP90 lub mTOR stosowanymi osobno przyniosły ograniczone korzyści, dowody przedstawione tutaj sugerują, że połączenie obu z cisplatyną może przywrócić wrażliwość wcześniej opornego guza. Autorzy wnioskują, że przyszłe badania kliniczne powinny przetestować tę potrójną strategię u pacjentów z nowotworami opornymi na platynę, najlepiej wybierając tych, których guzy wykazują wysoką aktywność tych szlaków. Jeśli się powiedzie, taka strategia mogłaby otworzyć nową drogę do przedłużenia życia pacjentów, dla których obecne opcje są ograniczone.
Cytowanie: Lombardi, R., Addi, L., Pucci, B. et al. Dual inhibition of mTOR and HSP90 enhances cisplatin efficacy and overcomes resistance in ovarian cancer. Cell Death Dis 17, 417 (2026). https://doi.org/10.1038/s41419-026-08533-3
Słowa kluczowe: rak jajnika, oporność na cisplatynę, inhibicja mTOR, inhibitory HSP90, terapia skojarzona