Clear Sky Science · sv
Dubbel blockering av mTOR och HSP90 ökar cisplastins effektivitet och övervinner resistens vid äggstockscancer
Varför denna forskning är viktig
Epitelial äggstockscancer är en av de dödligaste gynekologiska cancerformerna, till stor del eftersom många tumörer så småningom slutar svara på standardkemoterapi baserad på platina-läkemedlet cisplatin. När denna resistens uppstår är behandlingsmöjligheterna begränsade och överlevnaden sjunker kraftigt. Denna studie utforskar ett nytt sätt att göra envisa tumörer känsliga för cisplatin igen genom att samtidigt rikta in sig på två centrala stress- och tillväxtsystem i cancercellerna.
När standardläkemedel slutar fungera
Många vanliga cancerformer, inklusive äggstockscancer, lungcancer och huvud- och halscancer, behandlas med cisplatin och närbesläktade platina-baserade läkemedel. Dessa läkemedel verkar främst genom att skada DNA i snabbt delande celler och driva dem mot självdestruktion. Med tiden kan dock cancerceller anpassa sig. De pumpar ut läkemedlet mer effektivt, reparerar DNA-skador bättre eller stänger av dödssignaler, vilket leder till så kallad platinaresistens. För kvinnor med äggstockscancer återfaller mer än hälften av dem som initialt svarar väl på behandlingen med resistent sjukdom, för vilken effektiva terapier är få.
Hitta dolda brytare inne i cancerceller
För att förstå vad som förändras inne i resistenta äggstockscellinjer använde forskarna en teknik kallad fosfoproteomik, som kartlägger tusentals kemiska "av/på"-brytare på proteiner. Genom att jämföra platinkänsliga och platinresistenta äggstockscellinjer fann de 542 proteiner som skiljde sig åt mellan dem. Två stora kontrollnav framträdde: mTOR-signalvägen, som driver celltillväxt och överlevnad, och en stress-responsväg centrerad kring faktorn HSF1 och dess hjälpproteiner HSP90, HSP70 och HSP40, som fungerar som chaperoner som stabiliserar många andra proteiner. I de resistenta cellerna var dessa system mer aktiva och mer påslagna än i de känsliga motsvarigheterna, och liknande mönster syntes i platinresistenta lungceller och i primära celler från patienter.
Göra stresshjälpare till en akilleshäl
Teamet testade därefter om nedstängning av dessa överaktiva nav kunde blotta en svag punkt i resistenta tumörer. De fokuserade på HSP90, en nyckelchaperon, och mTOR, en central regulator av tillväxt. Genom genetisk modifiering visade de att borttagning av HSP90 gjorde resistenta lungceller mer sårbara för cisplatin, medan överuttryck av HSP90 i tidigare känsliga äggstocksceller gjorde dem svårare att döda och mindre benägna att uppvisa DNA-skador. Dessa experiment stöder idén att platinresistens delvis beror på uppreglerad HSP90- och mTOR-aktivitet och att resistenta celler kan vara ovanligt beroende av dessa vägar för att klara fortsatt läkemedelsstress.
En trippel-läkemedelsstrategi för att återkänsliggöra tumörer
Med dessa insikter som grund testade forskarna en tredelad behandling: cisplatin kombinerat med ganetespib, en HSP90-hämmare, och temsirolimus, en mTOR-hämmare som redan är godkänd för vissa cancerformer. I flera modeller av äggstockscancer odlad i plattor, i tredimensionella mikrovävnader som bättre efterliknar verkliga tumörer, och i möss med resistenta tumörer visade denna trippelkombination stark synergi. Den minskade kraftigt cancercellstillväxt, nästan eliminerade kolonibildning och orsakade tydlig krympning av tumörliknande mikrovävnader. I möss med cisplatinresistenta äggstocks- eller lungtumörtransplantat bromsade trippelbehandlingen nästan helt tumörtillväxten, minskade den totala tumörbördan med ungefär 85 % i en modell och förlängde överlevnaden signifikant, allt med acceptabel viktnedgång och utan större tecken på toxicitet.
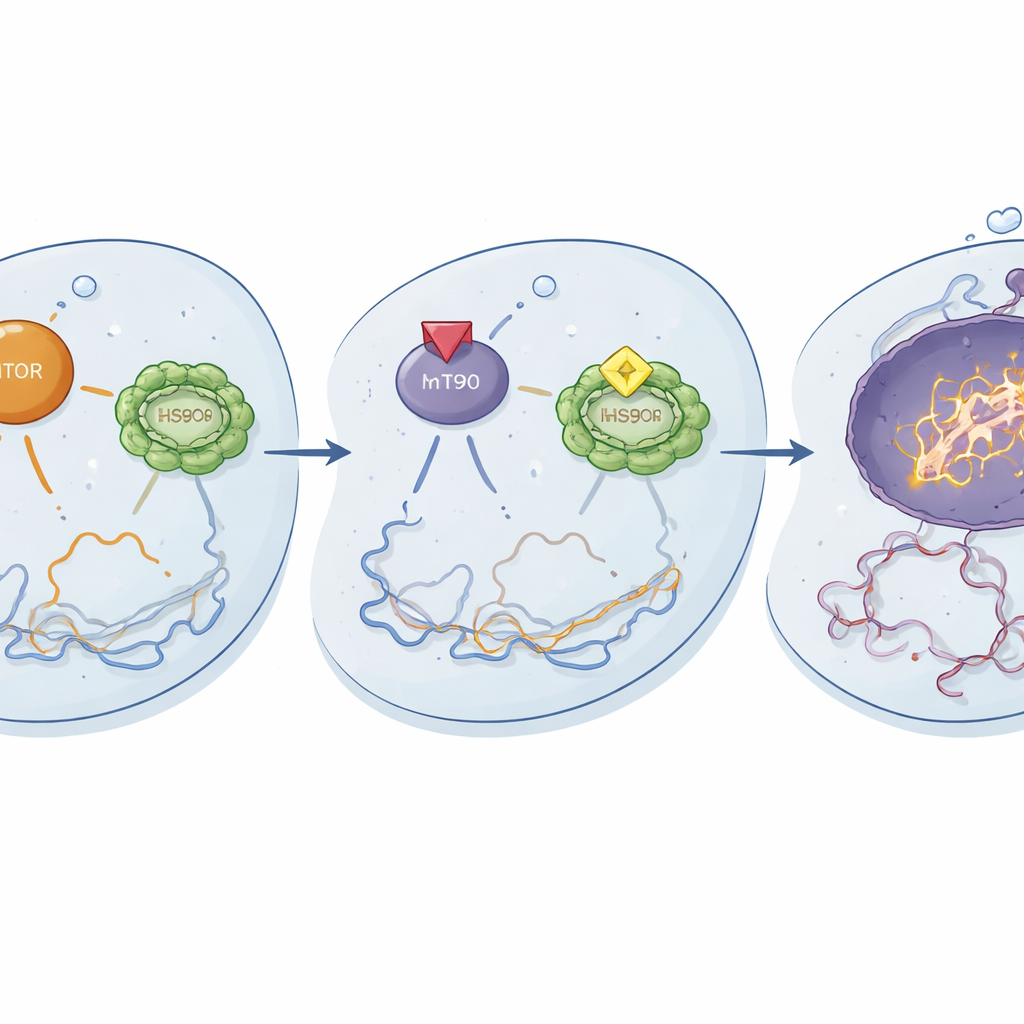
Hur den nya kombinationen verkar inne i cellen
Mekanistiska studier avslöjade vad som skedde på molekylär nivå. När ganetespib och temsirolimus användes tillsammans dämpades aktiveringen av nyckelkomponenter i mTOR-vägen och aktiviteten hos HSF1 och dess chaperonpartners, inklusive HSP90, minskade. Denna dubbla nedstängning verkade demontera viktiga överlevnads- och stresshanteringskretsar i resistenta celler. Som ett resultat orsakade cisplatin mer intensiv DNA-skada, vilket visades av ökade markörer för DNA-brott, och utlöste starkare apoptos, det kontrollerade självdestruktionsprogrammet. Tidiga förändringar i fosfoproteiner framträdde inom 24 timmar och blev mer uttalade vid 48 timmar, vilket tyder på att trippelterapin snabbt omkopplar signalnätverk från överlevnad mot celldöd.
Vad detta kan betyda för patienter
I praktiska termer föreslår detta arbete ett nytt sätt att angripa cancerformer som inte längre svarar på platina- kemoterapi genom att utnyttja deras beroende av mTOR-signalering och HSP90-driven stresskydd. Medan tidigare prövningar av enbart HSP90- eller mTOR-hämmare visat begränsad nytta, tyder bevisen här på att kombinationen av båda tillsammans med cisplatin kan göra en tidigare resistent tumör känslig för behandling igen. Författarna menar att framtida kliniska studier bör pröva denna trippelstrategi hos patienter med platinaresistent äggstockscancer och andra cancerformer, gärna med urval av de vars tumörer visar hög aktivitet i dessa vägar. Om framgångsrikt kan en sådan strategi öppna en ny väg för att förlänga livet för patienter med få nuvarande behandlingsalternativ.
Citering: Lombardi, R., Addi, L., Pucci, B. et al. Dual inhibition of mTOR and HSP90 enhances cisplatin efficacy and overcomes resistance in ovarian cancer. Cell Death Dis 17, 417 (2026). https://doi.org/10.1038/s41419-026-08533-3
Nyckelord: äggstockscancer, resistens mot cisplatin, mTOR-hämning, HSP90-hämmare, kombinationsbehandling