Clear Sky Science · zh
从肠道到大脑:来自人类到大鼠的粪菌移植对海马基因调控的影响——关于神经性厌食症的研究
为什么你的肠道可能与思维相关
神经性厌食症常被视为与食物和身体形象相关的思想与情感障碍,但越来越多的证据表明肠道中的微小生物也可能发挥作用。本研究探讨了来自神经性厌食症患者的肠道细菌在移植到大鼠后是否会影响大脑生物学。研究人员通过追踪动物肠道群落的变化以及与记忆密切相关的脑区——海马的改变,提出了一个简单却深远的问题:重新组合微生物组能否在进食障碍中对大脑产生帮助或伤害?
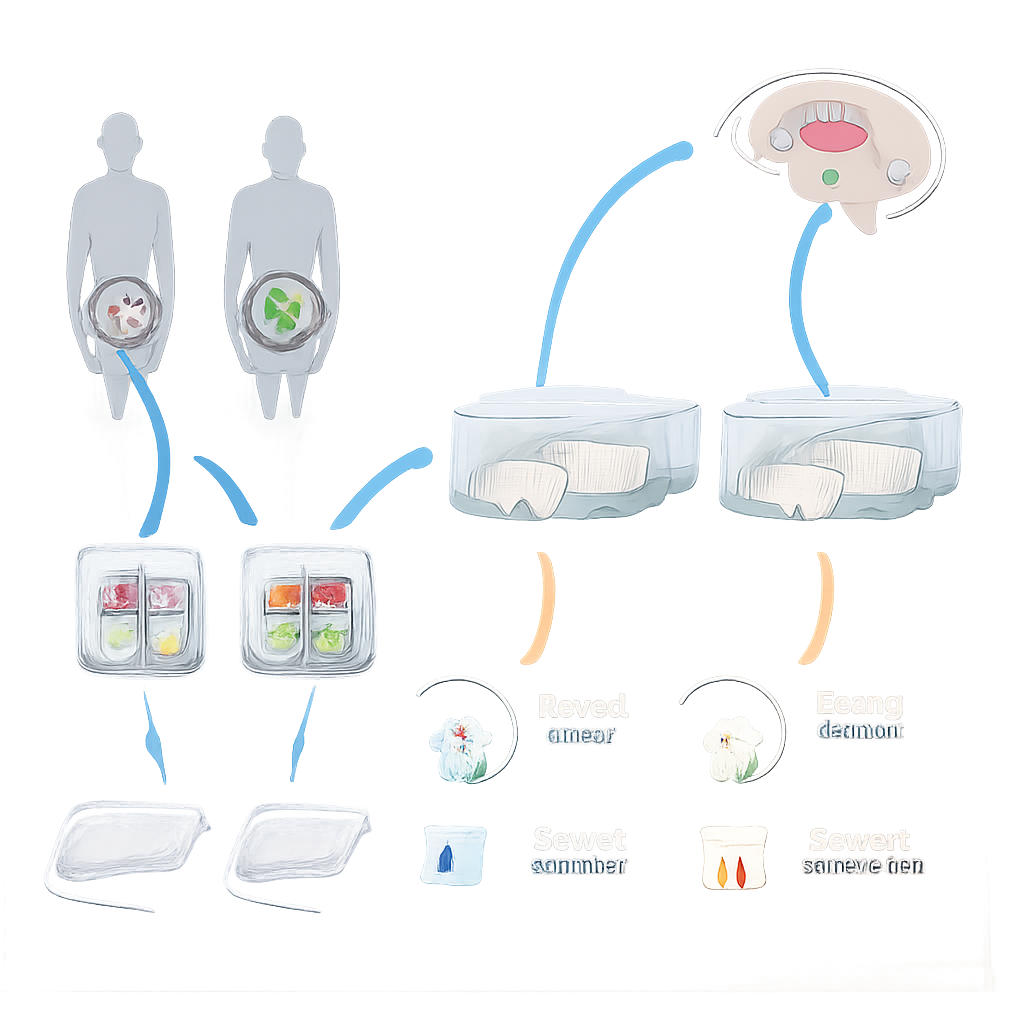
将微生物从人类转移到大鼠
研究团队使用了来自青春期女性神经性厌食患者以及年龄和性别相仿的健康对照者的粪便样本。这些样本经处理以保存活菌并随后冷冻保存。年轻雌性大鼠先在饮水中连续服用一周的抗生素混合物,以显著减少其自身的肠道细菌。在这一“清除”阶段之后,部分大鼠反复接受来自健康供体的粪菌移植(FMT),部分接受来自厌食患者供体的移植,另一些仅给予水。所有动物均可自由获取食物、水和跑轮,科学家在数周内监测它们的体重、摄食量和活动量。
肠道发生了哪些变化
抗生素处理强烈扰动了大鼠的肠道生态系统,降低了总体微生物生物量并改变了细菌群落的构成。随着时间推移,FMT在一定程度上重建了这些群落:源自人类的细菌在大鼠体内成功定植,尤其是在接受健康供体粪便的大鼠中。尽管如此,转移并不完全——只有适度比例的人类细菌类型在大鼠中建立起来。重要的是,尽管微生物组发生了这些变化,接受来自厌食患者粪便的大鼠并未出现典型的疾病样特征:它们的体重、摄食量和跑轮活动与其他组别相似。
大脑发生了哪些变化
为了解肠道变化如何可能影响大脑,研究者检查了海马——一个对学习、记忆和灵活思维至关重要的区域,而这些能力在厌食症中常受损。他们测量了关键脑细胞类型的存在情况以及与细胞生长、支持细胞和炎症相关基因的活性。单独使用抗生素会降低与少突胶质细胞(有助于神经纤维绝缘)相关基因的活性,同时减少与维持健康脑回路至关重要的生长因子Bdnf的表达,并抑制一个新细胞产生的标记(Mki67)。当大鼠接受来自健康供体的FMT时,这些负面效应在很大程度上得到逆转:Bdnf和Mki67的表达回升,海马中的炎性信号分子以与活跃修复与重塑一致的模式增加。相比之下,来自厌食患者供体的FMT未能完全恢复这些指标,使得与生长相关和炎症相关的信号相对受抑。
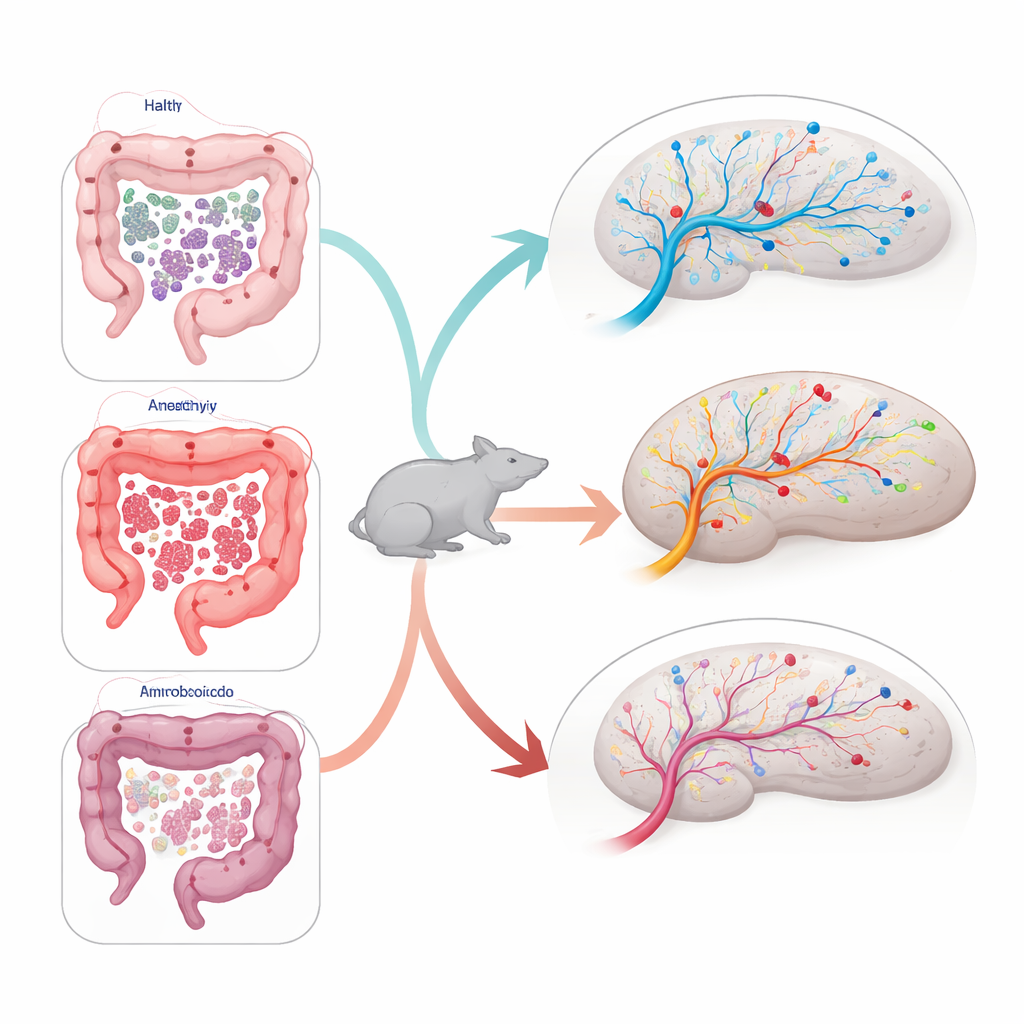
细菌与脑信号之间的关联
深入分析时,科学家探讨了特定细菌群与脑基因活性之间的关系。某些曾与情绪、代谢或炎症相关的属——例如Akkermansia、Blautia、Prevotella和Butyricicoccus——显示出与海马中神经可塑性和免疫信号标记的显著关联。例如,一些细菌与炎症和细胞增殖相关基因的较高表达相关,而另一些则表现出相反的模式。这些模式在接受健康供体粪便与接受厌食患者粪便的大鼠之间存在差异,提示不同的微生物“指纹”可能会将大脑修复过程推向不同方向。
这对厌食症和未来治疗意味着什么
这项研究表明,尽管来自厌食患者的粪菌移植本身并不会在大鼠中重现该疾病,但它们确实影响海马在微生物组遭受重大干扰后的应对方式。抗生素似乎抑制了大脑的可塑性和支持细胞功能,只有健康供体的微生物群能够可靠地恢复与生长及炎症相关的信号。通俗来说,肠道群落似乎能够在遭受打击后将大脑推向恢复或远离恢复的方向。这些发现支持了这样一种观点:厌食症并非纯粹的心理疾病,还涉及肠脑环路。研究指出,定制的微生物混合物——或它们产生的有益分子——结合精心的营养支持和直接针对饥饿的策略,可能在未来成为对现有治疗的有益补充。
引用: Korten, N.M., Blischke, L., Thelen, A.C. et al. From gut to brain: effects of fecal microbiota transplants from humans to rats on hippocampal gene regulation - a study on anorexia nervosa. Transl Psychiatry 16, 238 (2026). https://doi.org/10.1038/s41398-026-04056-9
关键词: 神经性厌食症, 肠道微生物组, 粪菌移植, 海马, 神经炎症