Clear Sky Science · it
Dall’intestino al cervello: effetti dei trapianti di microbiota fecale da esseri umani a ratti sulla regolazione genica dell’ippocampo - uno studio sull’anoressia nervosa
Perché il tuo intestino potrebbe contare per la tua mente
L’anoressia nervosa è spesso considerata un disturbo dei pensieri e delle emozioni legati al cibo e all’immagine corporea, ma evidenze crescenti suggeriscono che i piccoli organismi presenti nell’intestino possano avere un ruolo. Questo studio indaga se i batteri intestinali di persone con anoressia possano influenzare la biologia del cervello quando vengono trasferiti in ratti. Monitorando i cambiamenti nelle comunità intestinali degli animali e in una regione cerebrale fondamentale per la memoria, l’ippocampo, i ricercatori pongono una domanda semplice ma di ampia portata: rimischiare il microbioma può aiutare — o danneggiare — il cervello nei disturbi alimentari?
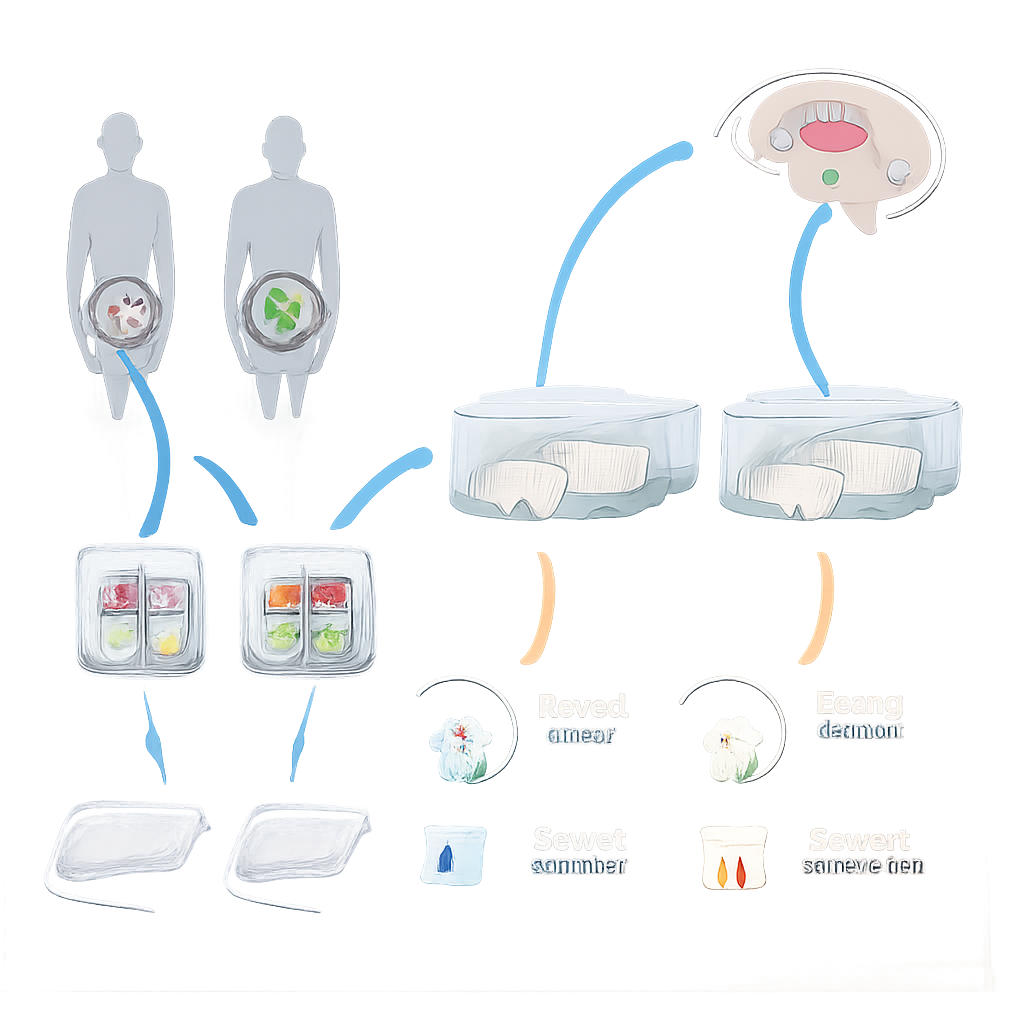
Spostare i microbi dalle persone ai ratti
Il team ha lavorato con campioni di feci provenienti da ragazze adolescenti con anoressia e da coetanee sane di età e sesso simili. Questi campioni sono stati processati per preservare i batteri vivi e poi congelati. Giovani ratti femmina hanno ricevuto inizialmente per una settimana un cocktail di antibiotici nell’acqua da bere per ridurre drasticamente i loro batteri intestinali. Dopo questa fase di “pulizia”, alcuni ratti hanno ricevuto trapianti ripetuti di microbiota fecale (FMT) da donatrici sane, altri da donatrici con anoressia e altri ancora solo acqua. Tutti gli animali avevano accesso illimitato a cibo, acqua e ruote per correre, e gli scienziati hanno monitorato il loro peso, l’assunzione di cibo e l’attività per diverse settimane.
Cosa è cambiato nell’intestino
Il trattamento antibiotico ha profondamente disturbato gli ecosistemi intestinali dei ratti, abbassando la biomassa microbica complessiva e modificando i gruppi batterici presenti. Nel tempo, l’FMT ha parzialmente ricostruito queste comunità: i batteri di origine umana si sono insediati con successo nei ratti, soprattutto in quelli che hanno ricevuto feci da donatrici sane. Tuttavia, il trasferimento è stato tutt’altro che completo: solo una frazione modesta dei tipi batterici umani si è stabilita. Importante, nonostante questi cambiamenti del microbioma, i ratti che hanno ricevuto feci da pazienti con anoressia non hanno sviluppato caratteristiche classiche della malattia: peso corporeo, assunzione di cibo e attività alla ruota sono rimasti simili a quelli delle altre coorti.
Cosa è cambiato nel cervello
Per valutare come i cambiamenti intestinali potessero influire sul cervello, i ricercatori hanno esaminato l’ippocampo, una regione essenziale per apprendimento, memoria e pensiero flessibile — capacità spesso compromesse nell’anoressia. Hanno misurato sia la presenza di tipi cellulari chiave sia l’attività di geni legati alla crescita cellulare, alle cellule di supporto e all’infiammazione. Gli antibiotici da soli hanno ridotto l’attività di geni associati agli oligodendrociti, cellule che aiutano a isolare le fibre nervose. Hanno inoltre ridotto l’espressione di Bdnf, un fattore di crescita cruciale per il mantenimento di circuiti cerebrali sani, e attenuato un marcatore di nuova produzione cellulare (Mki67). Quando i ratti hanno ricevuto FMT da donatrici sane, questi effetti negativi sono stati in gran parte invertiti: l’espressione di Bdnf e Mki67 è risalita e le molecole di segnalazione infiammatoria nell’ippocampo sono aumentate secondo uno schema consistente con processi di riparazione e rimodellamento attivi. Al contrario, l’FMT proveniente da donatrici con anoressia non è riuscito a ripristinare pienamente queste misure, lasciando segnali legati alla crescita e all’infiammazione relativamente attenuati.
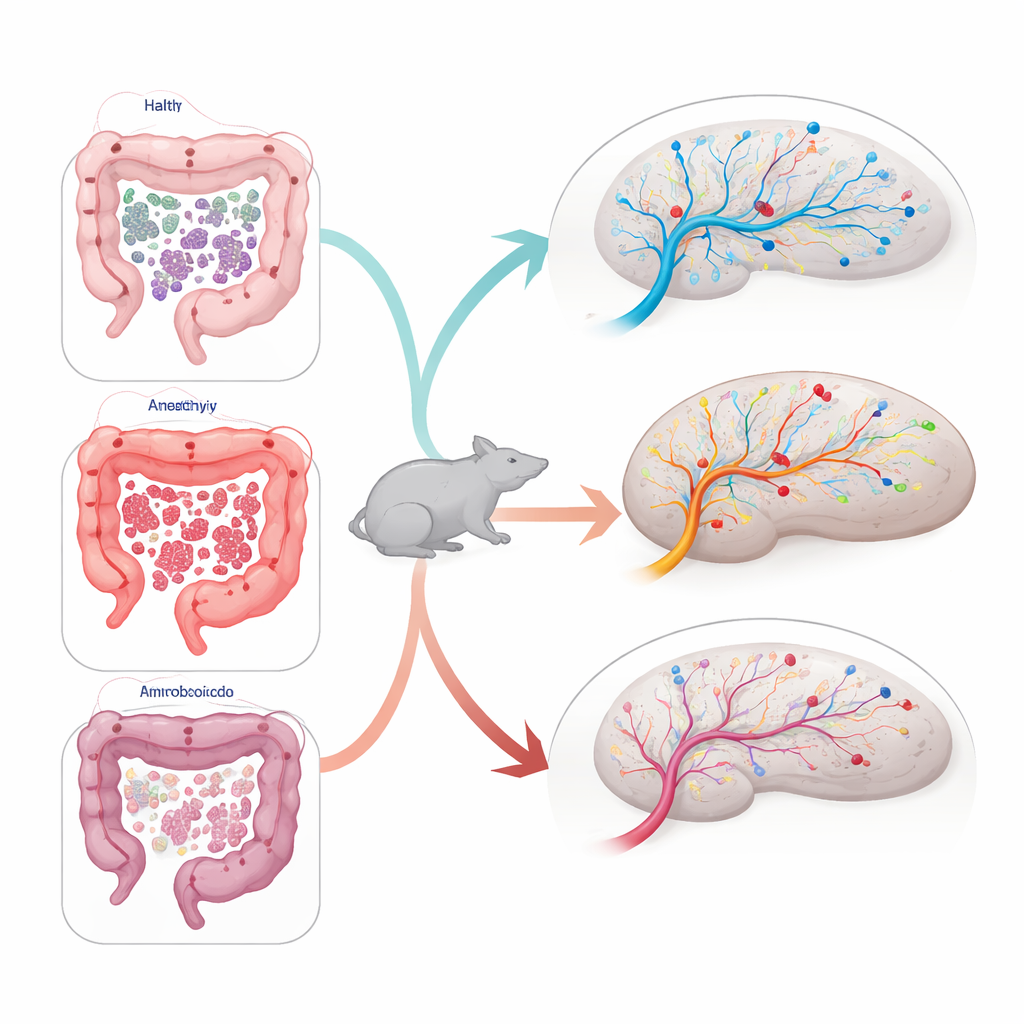
Legami tra batteri e segnali cerebrali
Approfondendo, gli scienziati hanno esplorato come gruppi batterici specifici si correlassero con l’attività genica cerebrale. Alcuni generi implicati nell’umore, nel metabolismo o nell’infiammazione — come Akkermansia, Blautia, Prevotella e Butyricicoccus — hanno mostrato associazioni notevoli con marcatori di neuroplasticità e segnalazione immunitaria nell’ippocampo. Per esempio, alcuni batteri erano legati a una maggiore espressione di geni coinvolti nell’infiammazione e nella proliferazione cellulare, mentre altri mostravano il pattern opposto. Questi schemi differivano tra i ratti che avevano ricevuto feci da donatrici sane e quelli che avevano ricevuto campioni da pazienti con anoressia, suggerendo che “firme” microbiche distinte possano spingere i processi di riparazione cerebrale in direzioni diverse.
Cosa significa per l’anoressia e per i trattamenti futuri
Lo studio mostra che, sebbene i trapianti fecali da persone con anoressia non ricreino da soli il disturbo nei ratti, essi modulano il modo in cui l’ippocampo risponde a una grande perturbazione del microbioma. Gli antibiotici sembravano attenuare la plasticità cerebrale e la funzione delle cellule di supporto, e solo il microbiota da donatrici sane ha ripristinato in modo affidabile i segnali legati alla crescita e all’infiammazione. In termini semplici, la comunità intestinale sembra in grado di spingere il cervello verso o lontano dal recupero dopo un danno. Questi risultati supportano l’idea che l’anoressia non sia puramente una malattia psicologica ma coinvolga anche un anello intestino‑cervello. Indicano una prospettiva in cui mix microbici su misura — o le molecole benefiche che essi producono — potrebbero integrare le terapie esistenti, soprattutto se combinati con un supporto nutrizionale attento e strategie che affrontino direttamente la denutrizione.
Citazione: Korten, N.M., Blischke, L., Thelen, A.C. et al. From gut to brain: effects of fecal microbiota transplants from humans to rats on hippocampal gene regulation - a study on anorexia nervosa. Transl Psychiatry 16, 238 (2026). https://doi.org/10.1038/s41398-026-04056-9
Parole chiave: anoressia nervosa, microbioma intestinale, trapianto di microbiota fecale, ippocampo, neuroinfiammazione