Clear Sky Science · zh
精神活性大麻素 THC 通过靶向 NaV1.7 和 NaV1.8 疼痛性钠通道抑制外周伤害感受器
一种著名的大麻化合物如何在源头麻痹疼痛
许多人知道大麻可以缓解疼痛,通常会假设它主要通过改变大脑对不适的感知来起作用。本研究揭示了另一个、不太为人熟知的方面:大麻中的主要精神活性成分 THC 也可以直接作用于我们皮肤和组织中的微小痛觉神经。研究显示 THC 通过一种类似于局麻药的机制使这些神经末梢沉默,这一发现暗示可以从大麻化学成分出发设计新的止痛药,而不必仅依赖其改变意识的作用。
从全身“亢奋”到局部疼痛控制
THC 最为人所知的是它与大脑和脊髓中的大麻受体结合,从而产生“兴奋”感和部分镇痛效应。但疼痛信号实际上起始于远离大脑的地方,即称为伤害感受器(nociceptors)的专门神经细胞,它们能检测有害的热、压或化学刺激。这些细胞通过称为钠通道的微小分子门来发放向脊髓传送的电信号。早期研究表明,非精神活性的大麻素如 CBD 和 CBG 能抑制这些钠通道,尤其是与疼痛密切相关的两种亚型 NaV1.7 和 NaV1.8。但此前尚不清楚 THC 本身是否也能作用于外周神经中的这些同样的通道。 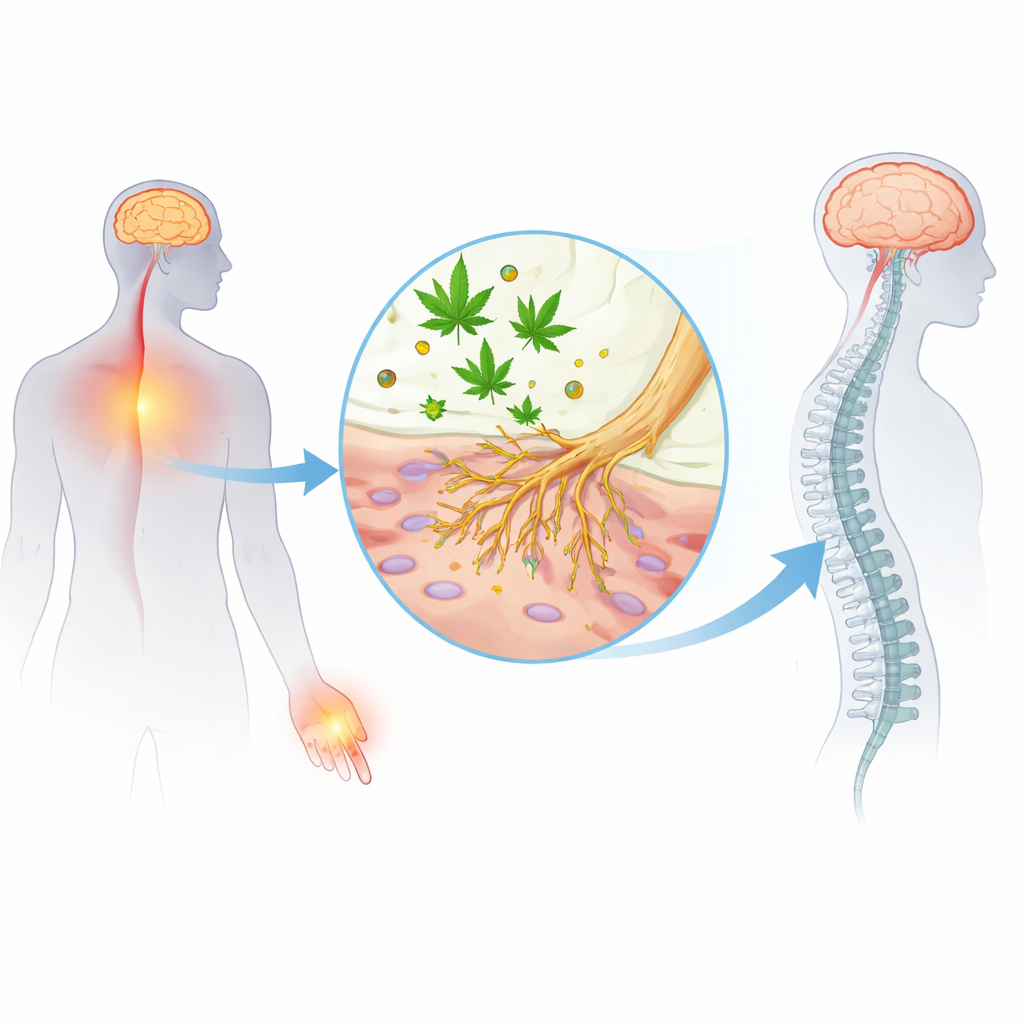
在痛觉神经上测试 THC 的作用
为此,研究人员分离了大鼠三叉神经节的痛觉神经元——一群传递面部和头部疼痛的神经细胞。他们用精细的玻璃电极记录这些神经元在受刺激时发放电尖峰(动作电位)的难易程度。即使在经典钠通道阻滞剂(河豚毒素)存在的情况下,加入 THC 仍显著减少了神经元的发放,并且作用发生在与使用大麻后组织中可能达到的微摩尔浓度范围内。这表明 THC 能直接抑制伤害感受器,且其效应在对河豚毒素有抵抗性的那类钠通道上尤其明显——这些通道在持续性疼痛期间维持重复放电方面至关重要。
锁定两个关键的钠通道阀门
研究团队随后在培养细胞中表达了单一的人类钠通道类型,以便明确 THC 作用的具体通道。他们发现 THC 有效抑制 NaV1.7 和 NaV1.8——这两种与疼痛密切相关的亚型——而对其他主要钠通道类型基本不受影响。THC 使这些通道更容易处于“失活”的非传导状态,这种状态是局麻药类常见的行为。当研究者改变构成局麻药经典结合口袋的特定氨基酸时,THC 的效力明显下降且失去了对通道状态的依赖性。这一结果将 NaV1.8 上的相同结合口袋确定为 THC 的重要停靠位点,强烈表明 THC 在这些与疼痛相关的通道上作为类似局麻药的阻断剂发挥作用。 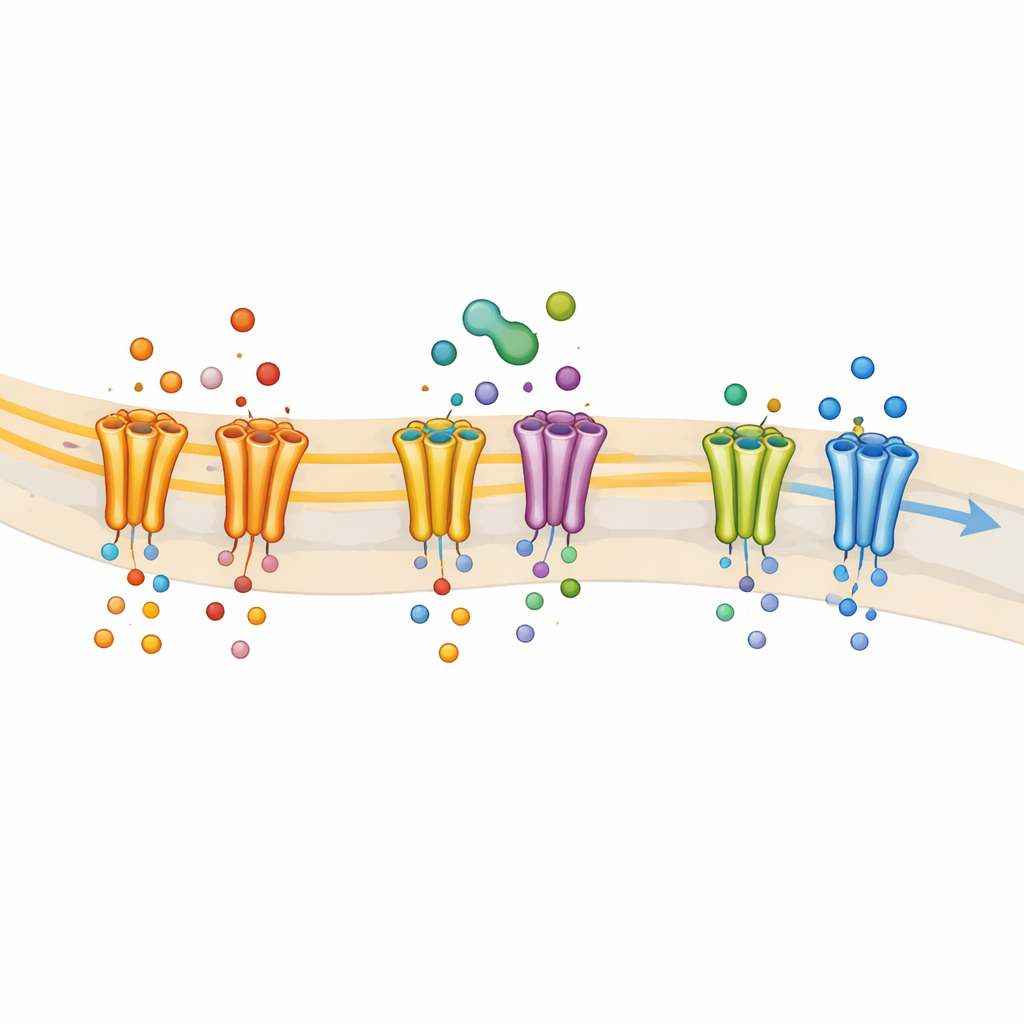
将 THC 与其非精神活性“表亲”比较
科学家还比较了 THC 与其他几种植物来源的大麻素。所有这些化合物,包括 CBD、CBG 和大麻喹啉(CBC),都能以相似程度抑制 NaV1.7。然而 NaV1.8 更具选择性:CBD 和 CBG 对其有较强阻滞作用,而 THC 和 CBC 的作用较弱。这些差异很可能源于每种分子在结构上的细微差异以及它们与局麻药结合口袋契合的程度。由于 NaV1.8 在维持伤害感受器重复放电中起主要作用,这种选择性有助于解释为什么非精神活性大麻素在抑制疼痛信号传导方面有时看起来比 THC 更有效,尽管它们具有相关的化学骨架。
对未来止痛治疗的意义
总体来看,研究表明 THC 不仅是作用于大脑的药物;它还能通过像局麻药那样堵塞关键钠通道直接使痛觉神经末梢沉默。通过在外周选择性靶向 NaV1.7 和 NaV1.8 而相对保留其他钠通道,THC 有助于在疼痛信号到达脊髓之前减弱其强度。这一认识澄清了大麻缓解疼痛的部分机制,并提出了一个有前景的方向:设计受 THC 启发但主要停留在外周、专门作用于伤害感受器的化合物。此类药物或能在减少精神活性副作用的同时提供实质性的止痛效果,将现代离子通道药理学的精确性与大麻类药物的历史传统相结合。
引用: Maatuf, Y., Iskimov, A., Binshtok, A.M. et al. The psychoactive cannabinoid THC inhibits peripheral nociceptors by targeting NaV1.7 and NaV1.8 nociceptive sodium channels. Neuropsychopharmacol. 51, 1091–1099 (2026). https://doi.org/10.1038/s41386-026-02355-9
关键词: THC, 疼痛信号传导, 钠通道, 周围神经, 大麻素镇痛