Clear Sky Science · ar
الكانابينويد النفسي الفعَّال THC يثبط مستقبلات الألم المحيطية عن طريق استهداف قنوات الصوديوم النوكيسبتيفية NaV1.7 وNaV1.8
كيف قد يُخَمِّد مركب قنَّب مشهور الألم عند مصدره
يعرف كثير من الناس أن القنَّب يمكن أن يخفف الألم، وغالبًا ما يفترضون أنه يعمل بصورة أساسية بتغيير كيفية إدراك الدماغ للانزعاج. تكشف هذه الدراسة جانبًا آخر أقل شهرة: المكوّن النفسي الفعّال الرئيسي في القنّب، THC، يمكنه أن يؤثر مباشرة على الأعصاب الحسّاسة للألم الصغيرة في الجلد والأنسجة. من خلال إظهار أن THC يُهدّئ نهايات هذه الأعصاب عبر آلية تشبه مخدِّرات موضعية، تشير الدراسة إلى سبل جديدة لتصميم أدوية مسكنة للألم تستفيد من كيمياء القنّب دون الاعتماد فقط على تأثيراته المحوِّلة للوعي.
من تأثير شامل على الجسم إلى تحكّم موضعي بالألم
يُعرف THC بارتباطه بمستقبلات الكانابينويد في الدماغ والحبل الشوكي، ما ينتج عنه كلٌّ من النشوة وبعض تأثيرات تخفيف الألم. لكن إشارات الألم تبدأ في الواقع بعيدًا عن الدماغ، في خلايا عصبية متخصِّصة تُسمى النوكيسبتورات التي تكشف عن الحرارة الضارة أو الضغط أو المواد الكيميائية. تستخدم هذه الخلايا بوابات جزيئية صغيرة تُدعى قنوات الصوديوم لإطلاق نبضات كهربائية نحو الحبل الشوكي. أظهرت أبحاث سابقة أن مركبات القنّب غير النفسانية مثل CBD وCBG يمكن أن تخفف نشاط هذه القنوات، لا سيما شكلين معروفين هما NaV1.7 وNaV1.8 المرتبطين بشكلٍ قوي بالألم. وحتى الآن، لم يكن واضحًا ما إذا كان THC نفسه يمكن أن يؤثر على هذه البوابات نفسها في الأعصاب المحيطية. 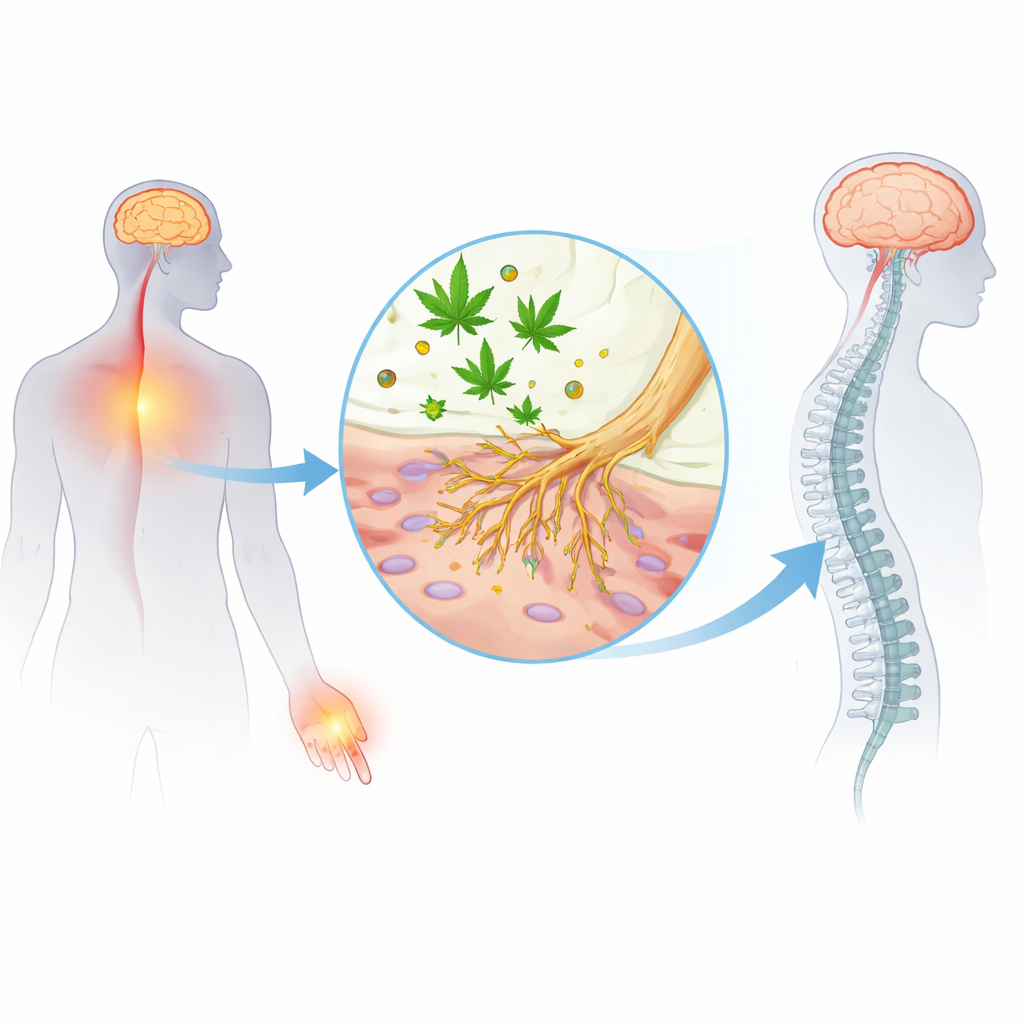
اختبار THC على الأعصاب الحسّاسة للألم
للإجابة عن ذلك، عزل الباحثون خلايا عصبية حسّاسة للألم من عقدٍ ثلاثية التوائم في الجرذان، وهي مجموعة من خلايا الأعصاب التي تنقل ألم الوجه والرأس. باستخدام أقطاب زجاجية دقيقة، سجّلوا مدى سهولة إطلاق هذه الخلايا لنبضات كهربائية—إمكانات الفعل—عند تحفيزها. حتى عندما كان مُثبِّط كلاسيكي لقنوات الصوديوم (تترودوتوكسين) حاضرًا، أدَّى إضافة THC إلى خفضٍ حاد في تكرار إطلاق الخلايا للنبضات، وذلك بتركيزات ميكرومولارية واقعية للأنسجة بعد استخدام القنّب. أظهر هذا أن THC يمكنه كبح النوكيسبتورات مباشرة، وأن تأثيره قوي بشكل خاص على فئة من قنوات الصوديوم المقاومة للتترودوتوكسين، والتي تُعدُّ أساسية لإطلاق نبضات متكررة أثناء الألم المستمر.
التركيز على بوابتين حيويتين للصوديوم
ثم عبَّر الفريق عن أنواع قنوات الصوديوم البشرية الفردية في خلايا مزروعة حتى يتمكّنوا من رؤية أيها يتأثر بالضبط بواسطة THC. وجدوا أن THC يثبط بقوة NaV1.7 وNaV1.8—الشكلين المترابطين بالألم—فيما ترك الأنواع الرئيسية الأخرى من قنوات الصوديوم بلا تأثير يُذكر. جعل THC هذه القنوات أكثر ميلاً للبقاء في حالة "مُعطَّلة" غير ناقِلة، وهي سلوك يُميّز الأدوية التي تعمل كمخدِّرات موضعية. عندما غيّر الباحثون أحماضًا أمينية محددة تشكّل الجيب الكلاسيكي لارتباط أدوية المخدِّر الموضعي، أصبح THC أقل فعالية وفقد سلوكه المعتمد على الحالة. حدَّد هذا الجيب نفسه كموقع ارتكاز رئيسي لـTHC على NaV1.8، مما يشير بقوة إلى أن THC يعمل كمانع شبيه بالمخدِّر الموضعي عند هذه القنوات المرتبطة بالألم. 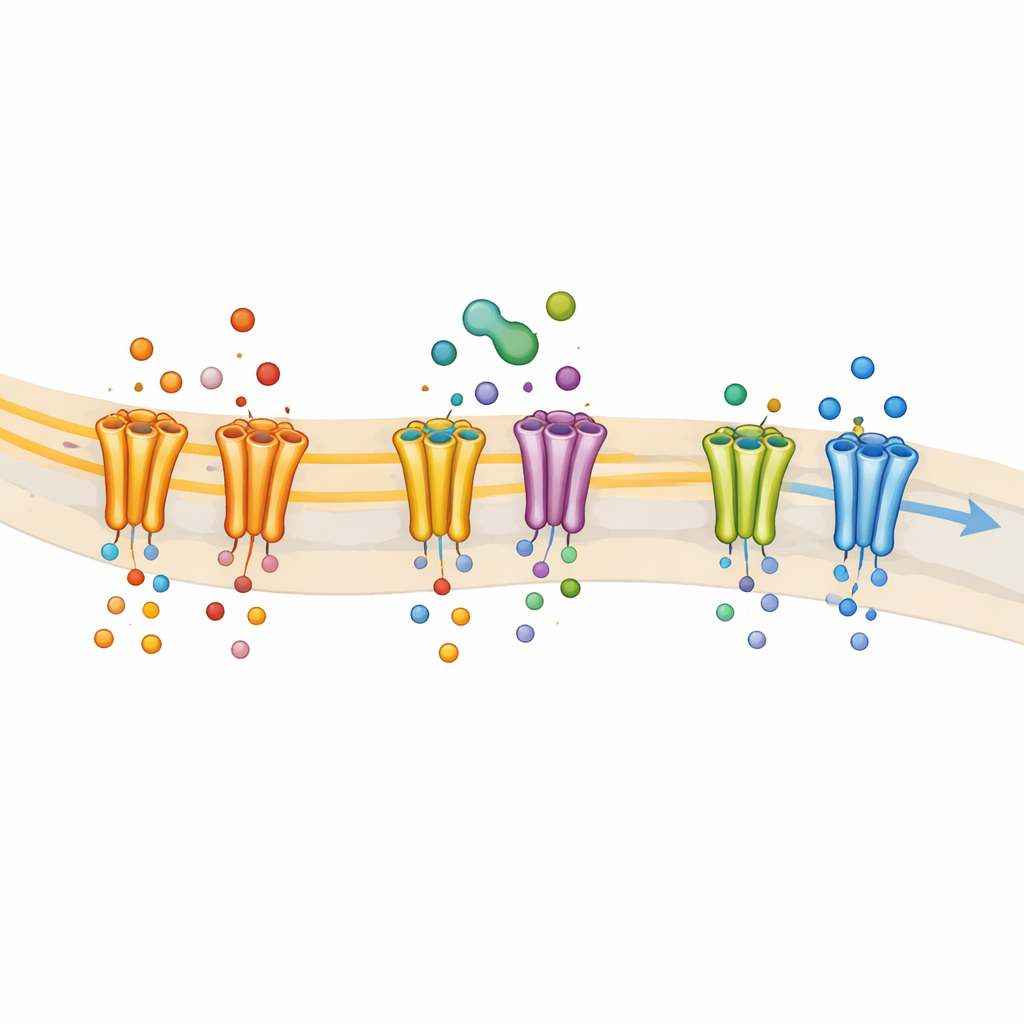
مقارنة THC بأقربائه غير النفسيين
قارن الباحثون أيضًا THC بعدد من الكانابينويدات النباتية الأخرى. جميعها، بما في ذلك CBD وCBG وكانابيكرو مين (CBC)، كانت قادرة على تثبيط NaV1.7 بدرجة مماثلة. أما NaV1.8 فكان أكثر انتقائية: فقد حُجِز بقوة بواسطة CBD وCBG لكن بدرجة أقل بواسطة THC وCBC. من المرجح أن تنشأ هذه الاختلافات من فروق هيكلية دقيقة في كل جزيء ومدى توافقها مع الجيب الخاص بالمخدِّر الموضعي. ونظرًا للدور الكبير الذي تلعبه NaV1.8 في الحفاظ على إطلاق نبضات متكررة في النوكيسبتورات، تساهم هذه الانتقائية في تفسير سبب ظهور الكانابينويدات غير النفسانية أحيانًا أقوى من THC في كبح حركة إشارات الألم، رغم تشاركها في بنى كيميائية ذات صِلة.
ما الذي يعنيه هذا لعلاجات الألم في المستقبل
تُظهِر الدراسة مجملًا أن THC ليس دواءً فاعلًا فقط في الدماغ؛ بل يمكنه أيضًا إسكات نهايات الأعصاب الحسّاسة للألم مباشرة عن طريق سد قنوات الصوديوم الرئيسية بطريقة تشبه المخدِّر الموضعي. من خلال استهداف NaV1.7 وNaV1.8 في المحيط مع حفظ بقية قنوات الصوديوم، يساعد THC في تقليل شدة إشارات الألم قبل أن تصل حتى إلى الحبل الشوكي. يوضّح هذا الاكتشاف جزءًا من كيفية تخفيف القنّب للألم ويقترح مسارًا واعدًا للمستقبل: تصميم مركبات مستوحاة من THC تبقى إلى حد كبير خارج الدماغ لكنها تستهدف النوكيسبتورات المحيطية. قد تُوفّر مثل هذه الأدوية تخفيف ألم مهمًا مع آثار جانبية نفسية أقل، جامعًة بين دقة علوم قنوات الأيونات الحديثة وتاريخ طويل من الطب المستند إلى القنّب.
الاستشهاد: Maatuf, Y., Iskimov, A., Binshtok, A.M. et al. The psychoactive cannabinoid THC inhibits peripheral nociceptors by targeting NaV1.7 and NaV1.8 nociceptive sodium channels. Neuropsychopharmacol. 51, 1091–1099 (2026). https://doi.org/10.1038/s41386-026-02355-9
الكلمات المفتاحية: THC, إشارات الألم, قنوات الصوديوم, الأعصاب المحيطية, تسكين الكانابينويد