Clear Sky Science · fr
Le cannabinoïde psychoactif THC inhibe les nocicepteurs périphériques en ciblant les canaux sodiques nociceptifs NaV1.7 et NaV1.8
Comment un composé célèbre du cannabis peut engourdir la douleur à sa source
Beaucoup savent que le cannabis peut atténuer la douleur, en supposant souvent qu’il agit principalement en modifiant la perception de l’inconfort par le cerveau. Cette étude révèle un autre volet, moins connu : le principal ingrédient psychoactif du cannabis, le THC, peut aussi agir directement sur les minuscules nerfs détecteurs de douleur dans la peau et les tissus. En montrant que le THC calme ces terminaisons nerveuses par un mécanisme semblable à celui des anesthésiques locaux, le travail ouvre la voie à de nouvelles approches pour concevoir des médicaments analgésiques s’inspirant de la chimie du cannabis sans se limiter à ses effets psychoactifs.
Du « high » généralisé au contrôle local de la douleur
Le THC est surtout connu pour se lier aux récepteurs cannabinoïdes du cerveau et de la moelle épinière, ce qui produit à la fois le « high » et une partie de son effet antalgique. Mais les signaux douloureux démarrent en réalité loin du cerveau, dans des neurones spécialisés appelés nocicepteurs qui détectent la chaleur nocive, la pression ou des substances chimiques dommageables. Ces cellules utilisent de minuscules portes moléculaires, appelées canaux sodiques, pour déclencher des impulsions électriques vers la moelle épinière. Des travaux antérieurs avaient montré que des composés non psychoactifs du cannabis comme le CBD et le CBG pouvaient atténuer ces canaux sodiques, en particulier deux formes connues sous les noms NaV1.7 et NaV1.8, fortement liées à la douleur. Jusqu’à présent, on ignorait si le THC lui‑même pouvait agir sur ces mêmes portes dans les nerfs périphériques. 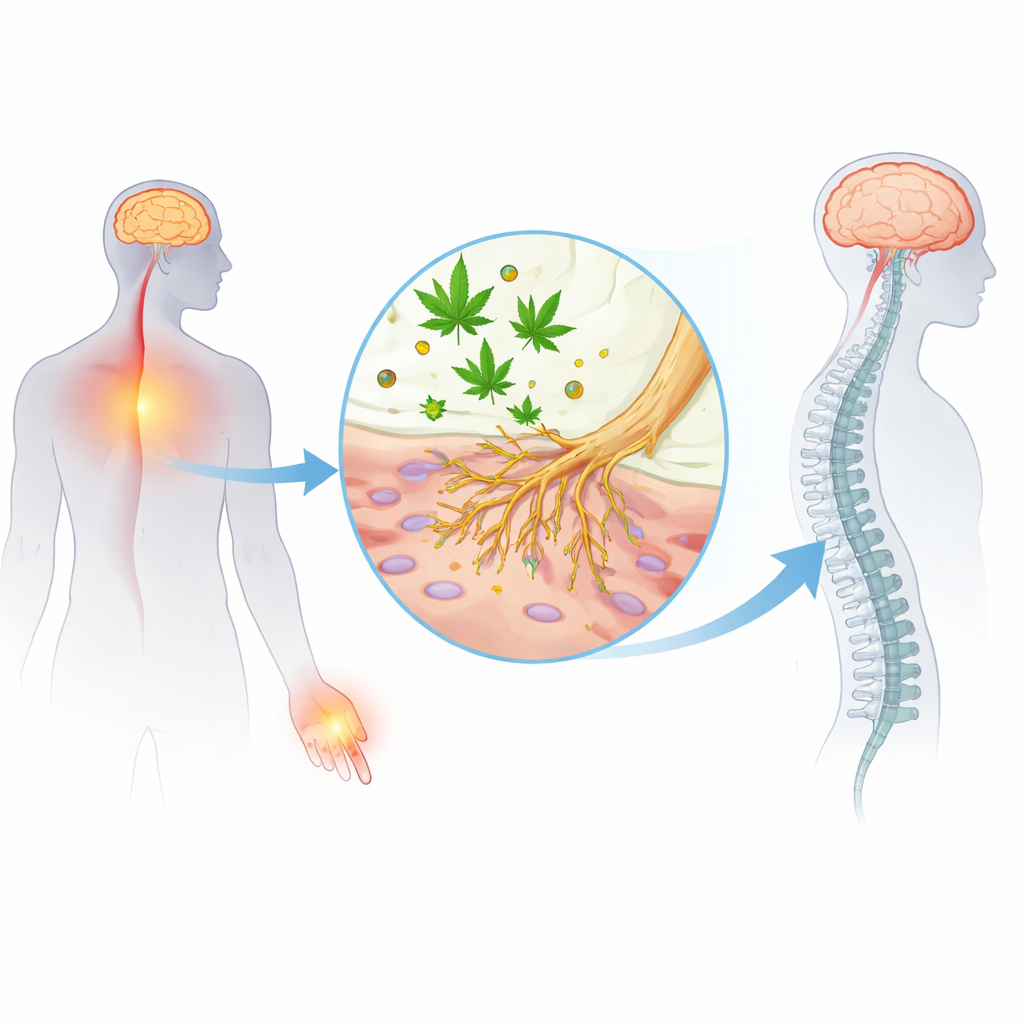
Tester le THC sur les nerfs détecteurs de douleur
Pour répondre à cette question, les chercheurs ont isolé des neurones détecteurs de douleur issus des ganglions trigéminés de rat, un amas de cellules nerveuses qui transmet la douleur faciale et crânienne. À l’aide de fines électrodes en verre, ils ont enregistré la facilité avec laquelle ces neurones déclenchaient des pointes électriques—des potentiels d’action—lorsqu’ils étaient stimulés. Même en présence d’un bloqueur classique des canaux sodiques (tétrodotoxine), l’ajout de THC a fortement réduit l’activité de décharge des neurones, et ce à des concentrations micromolaires compatibles avec celles observées dans les tissus après consommation de cannabis. Cela montre que le THC peut directement calmer les nocicepteurs, et que son effet est particulièrement marqué sur une sous‑population de canaux sodiques résistants à la tétradotoxine, essentiels au déchargement répétitif pendant une douleur soutenue.
Se concentrer sur deux verrous sodiques critiques
L’équipe a ensuite exprimé des types de canaux sodiques humains isolés dans des cellules en culture pour identifier précisément lesquels sont affectés par le THC. Ils ont trouvé que le THC inhibait puissamment NaV1.7 et NaV1.8—les formes fortement impliquées dans la douleur—tout en épargnant essentiellement d’autres types majeurs de canaux sodiques. Le THC rendait ces canaux plus susceptibles de rester dans un état « inactivé » non conducteur, un comportement caractéristique des médicaments agissant comme des anesthésiques locaux. Lorsque les chercheurs ont modifié des acides aminés précis qui forment la poche de liaison classique des anesthésiques locaux, le THC est devenu beaucoup moins efficace et a perdu son comportement dépendant de l’état. Cela identifie la même poche comme principal site d’accrochage du THC sur NaV1.8, suggérant fortement que le THC agit comme un bloqueur de type anesthésique local sur ces canaux liés à la douleur. 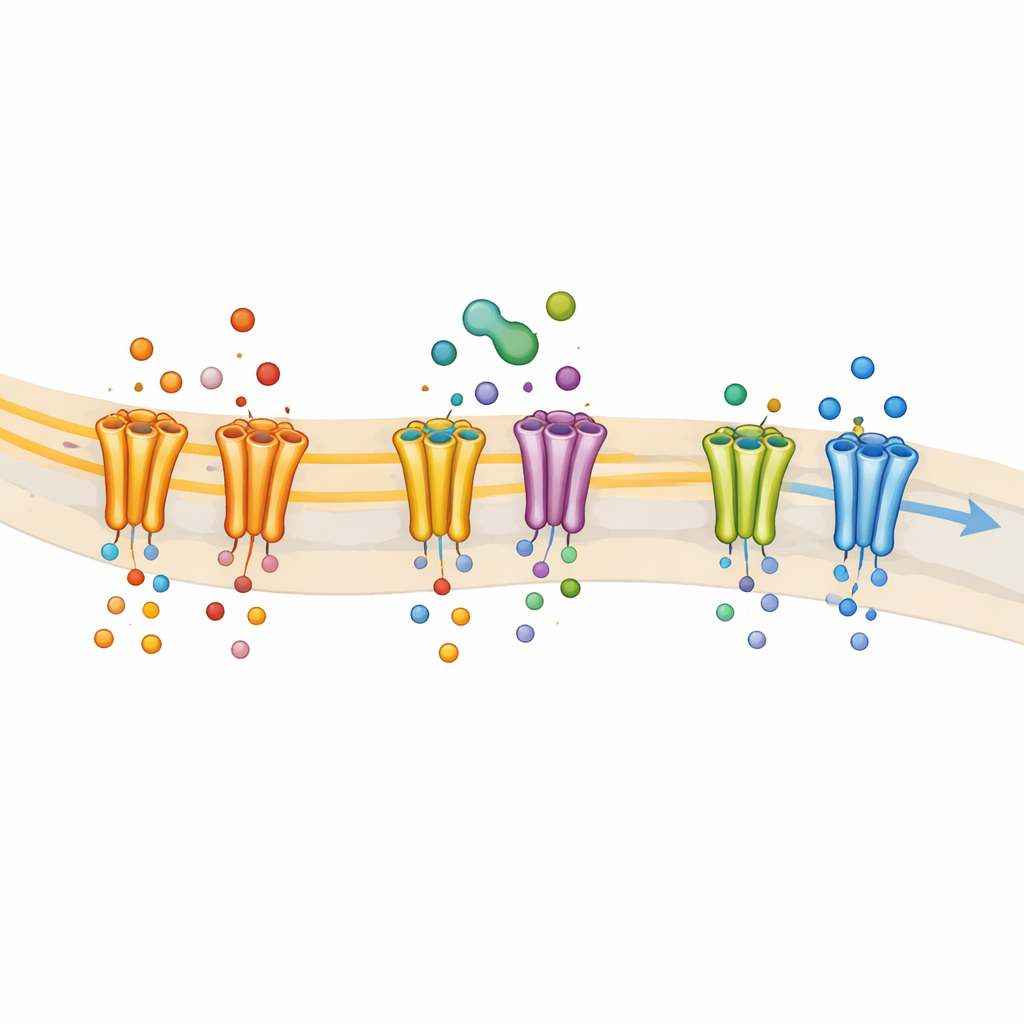
Comparaison du THC avec ses cousins non psychoactifs
Les scientifiques ont aussi comparé le THC à plusieurs autres cannabinoïdes végétaux. Tous, y compris le CBD, le CBG et le cannabichromène (CBC), pouvaient inhiber NaV1.7 dans des proportions similaires. NaV1.8, en revanche, montrait plus de sélectivité : il était fortement bloqué par le CBD et le CBG mais moins par le THC et le CBC. Ces différences proviennent vraisemblablement de caractéristiques structurelles subtiles de chaque molécule et de leur compatibilité avec la poche des anesthésiques locaux. Parce que NaV1.8 joue un rôle majeur dans le maintien du déchargement répétitif des nocicepteurs, cette sélectivité aide à expliquer pourquoi les cannabinoïdes non psychoactifs peuvent parfois sembler plus puissants que le THC pour atténuer le trafic des signaux douloureux, bien qu’ils partagent des squelettes chimiques apparentés.
Ce que cela signifie pour les traitements futurs de la douleur
Dans l’ensemble, l’étude montre que le THC n’est pas seulement un médicament agissant sur le cerveau ; il peut aussi faire taire directement les terminaisons nerveuses détectrices de douleur en bouchant des canaux sodiques clés, de façon comparable à un anesthésique local. En ciblant NaV1.7 et NaV1.8 en périphérie tout en épargnant d’autres canaux sodiques, le THC contribue à réduire l’intensité des signaux douloureux avant même qu’ils n’atteignent la moelle épinière. Cet éclairage clarifie une partie du mode d’action du cannabis sur la douleur et suggère une voie prometteuse : concevoir des composés inspirés du THC qui restent majoritairement en dehors du cerveau mais ciblent les nocicepteurs périphériques. De tels médicaments pourraient offrir un soulagement significatif avec moins d’effets psychoactifs, mariant la précision de la pharmacologie moderne des canaux ioniques à la longue histoire de la médecine à base de cannabis.
Citation: Maatuf, Y., Iskimov, A., Binshtok, A.M. et al. The psychoactive cannabinoid THC inhibits peripheral nociceptors by targeting NaV1.7 and NaV1.8 nociceptive sodium channels. Neuropsychopharmacol. 51, 1091–1099 (2026). https://doi.org/10.1038/s41386-026-02355-9
Mots-clés: THC, signalisation de la douleur, canaux sodiques, nerfs périphériques, analgésie cannabinoïde