Clear Sky Science · zh
牙源间充质干细胞异质性研究进展
为何微小的牙齿干细胞重要
牙齿表面看似简单,但内部藏着一个繁忙的干细胞世界,这些干细胞在默默构建、维护并修复我们的微笑。本文综述探讨了牙齿及其周围的一类特殊细胞——牙源间充质干细胞,阐明了它们隐含的多样性如何为治疗龋齿、牙龈疾病、颌骨缺损甚至神经损伤带来新路径。通过理解牙齿发育与愈合背后的“角色分工”,研究者希望设计出更智能、更可靠的再生疗法,而不是仅仅依赖钻牙、补牙和植入物。
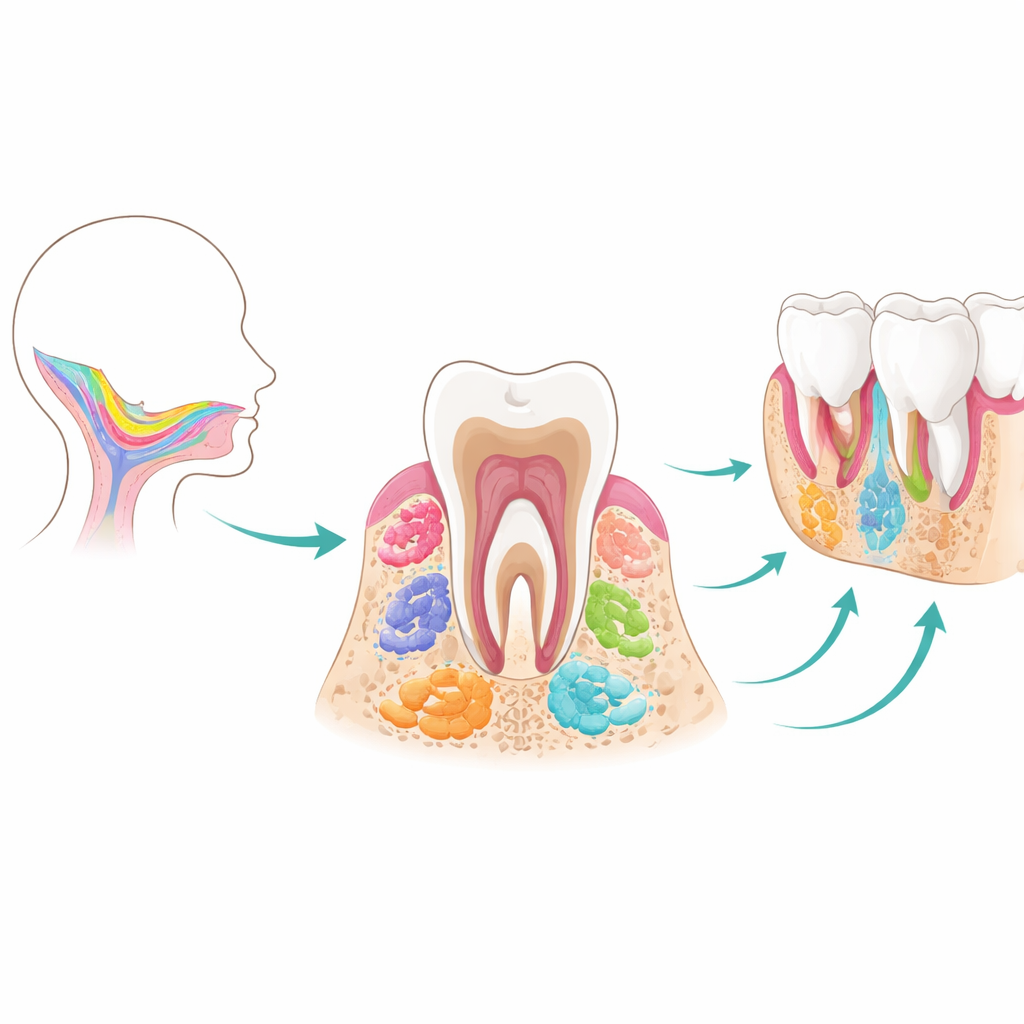
从早期牙胚到成熟牙齿
牙齿及其支持组织通过两大主要胚层之间精密配合形成:外层将来负责形成牙釉质,内层细胞则分化为牙本质、牙髓、韧带和颌骨。本综述关注的间充质干细胞都来源于早期胚胎迁移而来的颅神经嵴细胞。它们在定居于形成中的颌部后,首先产生牙胚——通过胚芽、帽盖和钟形等阶段发育的微小“芽”。在这一时间线上,若干短暂的干细胞群体按序出现。牙胚祖细胞作为早期多能构建者;牙囊干细胞参与组装固定牙齿的组织;位于根尖的根端乳头干细胞指导根的形成,并显示出向类神经细胞分化的意外潜力。随着牙根成熟,许多早期参与者消失,因而在后期研究或再利用时变得难以获取。
多种干细胞类型,构成一体化的牙齿系统
即便牙齿已完全形成,多种类型的干细胞仍藏身于受保护的利基位点,持续支持组织维护。牙髓干细胞位于牙齿内部,血管与神经在此进入;牙周韧带干细胞位于牙根与骨之间;龈源干细胞衬里牙龈;而位于牙槽(颌)骨的间充质干细胞构成锚定牙齿的“土壤”。每一类群体共享自我更新和分化为成骨或制牙本质细胞等基本特性,但并非相互可替代。例如,牙髓干细胞倾向于分化为牙本质和类神经细胞;牙周细胞擅长重建根面上的纤维附着和牙骨质;颌骨干细胞则专门用于面部快速、直接的成骨。这种内在的分工有助于解释为何口腔在牙髓、韧带或骨组织受伤时的反应各不相同。
每个干细胞库内部的隐性差异
综述的一个核心观点是,异质性不仅存在于不同干细胞类型之间,也存在于每一类型内部。诸如单细胞RNA测序等新技术可以同时描绘数千个单细胞,揭示具有独特基因活动和行为的子群。在牙髓中,例如,研究者已绘制出多个簇:一些维持储备库并驱动增殖,另一些已被预置用于牙本质生成,还有一些偏向形成血管或类神经细胞。类似的亚群也在牙周韧带干细胞、颌骨干细胞、乳牙干细胞和龈源干细胞中被发现。细胞表面与细胞核内的标志分子有助于区分这些亚群,它们在增殖能力、衰老模式以及对机械力、炎症或细菌侵袭的反应性上存在差异。
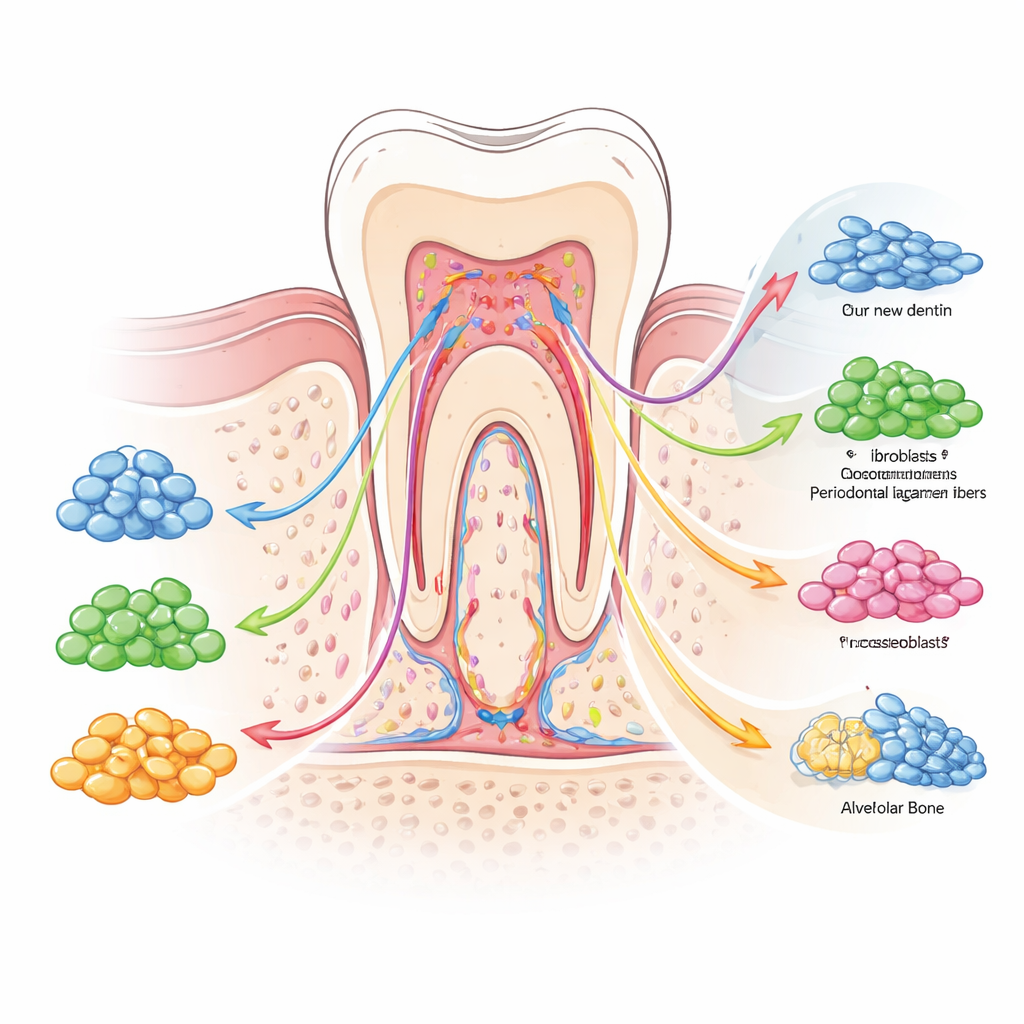
塑造干细胞行为的信号与开关
作者强调,这种多样性并非随机,而是由一张生化信号与“表观遗传”开关的网络组织起来,像交通灯和路标一样指引细胞命运。骨形态发生蛋白、Wnt信号和转化生长因子β驱动的通路促使细胞走向牙本质和骨等硬组织构建,而Notch和PI3K/AKT等通路则有助于维持干/祖细胞的平衡。同时,DNA和组蛋白等上的化学标记调整基因的可及性,使某些细胞被预设为在受损时迅速响应。咀嚼产生的机械力、感染引发的炎性分子以及来自邻近血管或神经的提示,进一步将平衡朝向修复、瘢痕形成或破坏倾斜。总体而言,这些控制层面共同构成了一个灵活但有时难以预测的愈合系统。
这对未来牙科护理意味着什么
对非专业读者而言,主要结论是:牙齿与牙龈再生不再是科幻,但能否成功将取决于对干细胞多样性的管理,而不是忽视它。综述认为,弄清哪些特定亚群构建牙本质、韧带、骨或神经——以及哪些信号引导它们——将帮助研究者改进细胞选择、生物材料和药物提示,从而实现可预测的结果。与此同时,作者也提醒大多数详尽的图谱来自动物研究和体外培养,技术噪声可能使图景模糊。他们呼吁在人类组织中采用整合的“多组学”方法、提高标准化程度并在活体系统中进行严格验证。最终,解码牙源间充质干细胞的异质性可能使牙医从用惰性材料替代受损结构,转向真正再生活的、功能性的牙齿及其支持组织。
引用: Fu, H., Chen, P., Wu, Z. et al. Research progress in heterogeneity of dental mesenchymal stem cells. Int J Oral Sci 18, 31 (2026). https://doi.org/10.1038/s41368-026-00433-8
关键词: 牙源干细胞, 牙齿再生, 牙周修复, 单细胞测序, 口腔组织工程