Clear Sky Science · nl
Onderzoek naar heterogeniteit van mesenchymale tandheelkundige stamcellen
Waarom kleine tandstamcellen ertoe doen
Tanden lijken aan de buitenkant eenvoudig, maar vanbinnen huist een levendige wereld van stamcellen die stilletjes ons gebit opbouwen, onderhouden en repareren. Dit overzichtsartikel verkent een bijzondere familie cellen in en rond tanden — mesenchymale tandstamcellen — en legt uit hoe hun verborgen diversiteit de deur kan openen naar betere behandelingen voor tandbederf, tandvleesziekten, botverlies in de kaak en zelfs zenuwletsel. Door het ‘ensemble’ achter tandontwikkeling en genezing te begrijpen, hopen onderzoekers slimme, betrouwbaardere regeneratieve therapieën te ontwerpen in plaats van alleen te vertrouwen op boren, vullingen en implantaten.
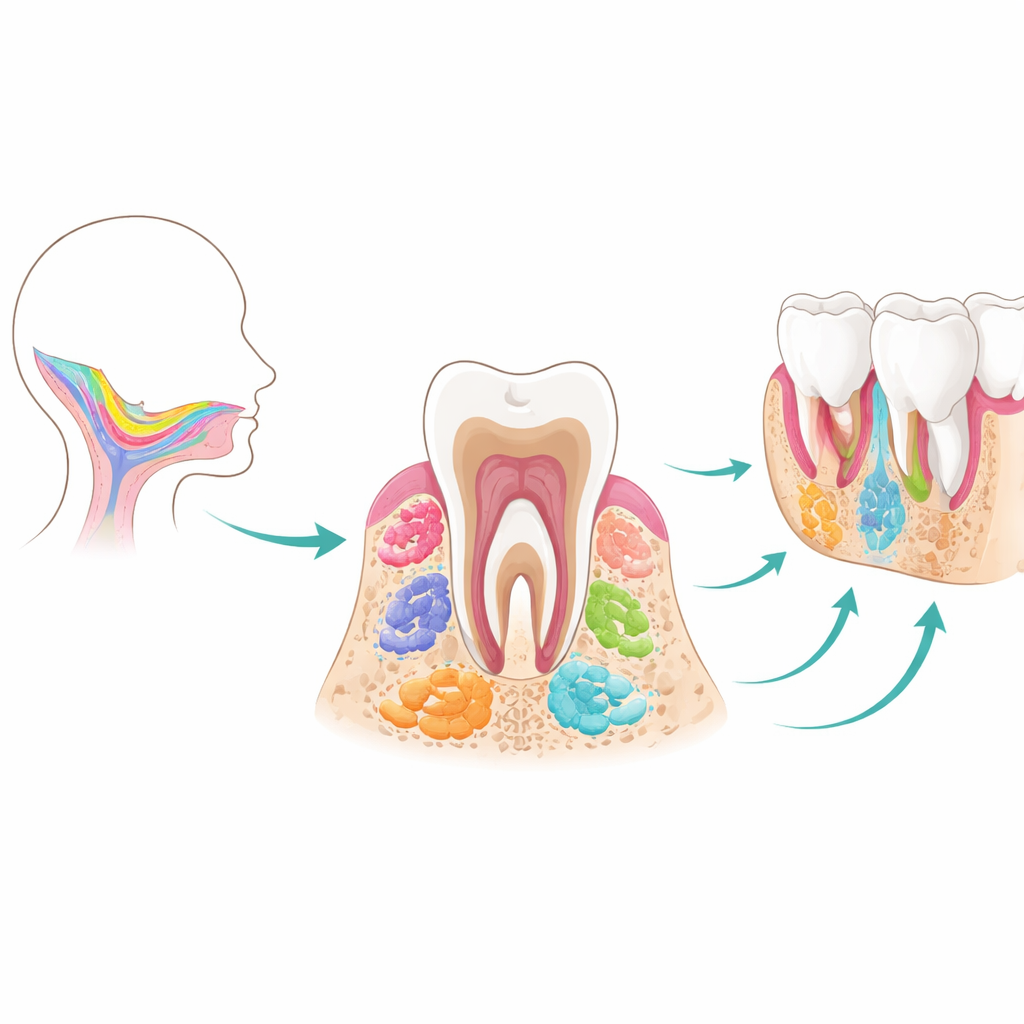
Van vroege tandknoppen tot volgroeide tanden
Tanden en hun ondersteunende weefsels ontstaan via een strak georkestreerde samenwerking tussen twee hoofdlagen: een buitenlaag die later glazuur zal vormen, en binnenste cellen die dentine, pulpa, ligament en kaakbeen voortbrengen. De mesenchymale stamcellen in het hart van dit overzicht stammen allemaal af van migrerende cellen uit het vroege embryo, de craniale neurale lijst. Wanneer zij zich in de vormende kaak vestigen, produceren deze cellen eerst tandkiem—kleine “knoppen” die de stadia knop, kap en bel doorlopen. Gedurende deze ontwikkeling verschijnen meerdere tijdelijke stamcelpopulaties opeenvolgend. Tandkiemprogenitorcellen fungeren als vroege, veelzijdige bouwers; folliculaire stamcellen helpen bij het samenstellen van de weefsels die tanden op hun plaats houden; en stamcellen in de apicale papil aan de worteltip sturen wortelvorming en tonen verrassende potentie om zenuwachtige cellen te worden. Zodra tandwortels rijpen, verdwijnen veel van deze vroege spelers, wat het moeilijk maakt ze later in het leven te bestuderen of opnieuw te gebruiken.
Verschillende stamceltypen, één geïntegreerd tandstelsel
Zelfs nadat tanden volledig gevormd zijn, blijven meerdere soorten stamcellen verscholen in beschermde niches en ondersteunen ze het onderhoud van weefsels. Pulpa-stamcellen leven binnenin de tand, waar bloedvaten en zenuwen binnenkomen; parodontaal ligament-stamcellen zitten tussen tandwortel en bot; gingivale stamcellen bekleden het tandvlees; en mesenchymale stamcellen in het alveolaire (kaak) bot vormen de “bodem” die tanden verankert. Elke populatie deelt basale eigenschappen zoals zelfvernieuwingsvermogen en de capaciteit om bot- of dentineproducerende cellen te worden, maar ze zijn niet uitwisselbaar. Zo hebben pulpacellen de neiging dentine en zenuwachtige rijpingen te bevorderen, parodontale cellen blinken uit in het herbouwen van de vezelige bevestiging en cementum op het worteloppervlak, en kaakbeencellen zijn gespecialiseerd in snelle, directe botvorming in het aangezicht. Deze ingebouwde taakverdeling helpt verklaren waarom de mond verschillend reageert op letsel in pulpa, ligament of bot.
Verborgen verschillen binnen elk stamcelbestand
Een kernboodschap van de review is dat heterogeniteit niet alleen bestaat tussen verschillende stamceltypen, maar ook binnen elk type. Nieuwe technieken zoals single-cell RNA-sequencing kunnen duizenden individuele cellen tegelijk profileren en subgroepen met onderscheidende genactiviteit en gedrag onthullen. In de tandpulpa bijvoorbeeld hebben onderzoekers meerdere clusters in kaart gebracht: sommige behouden de reservestam en stimuleren proliferatie, andere zijn voorbereid op dentineproductie, en weer andere neigen naar de vorming van bloedvaten of zenuwachtige cellen. Vergelijkbare subgroepen zijn gevonden in parodontale ligament-stamcellen, kaakbeenstamcellen, stamcellen uit melktanden en gingivale stamcellen. Merkmoleculen op het celoppervlak en in de kern helpen deze subpopulaties te onderscheiden; ze verschillen in groeicapaciteit, verouderingspatroon en responsiviteit op mechanische krachten, ontsteking of bacteriële aanval.
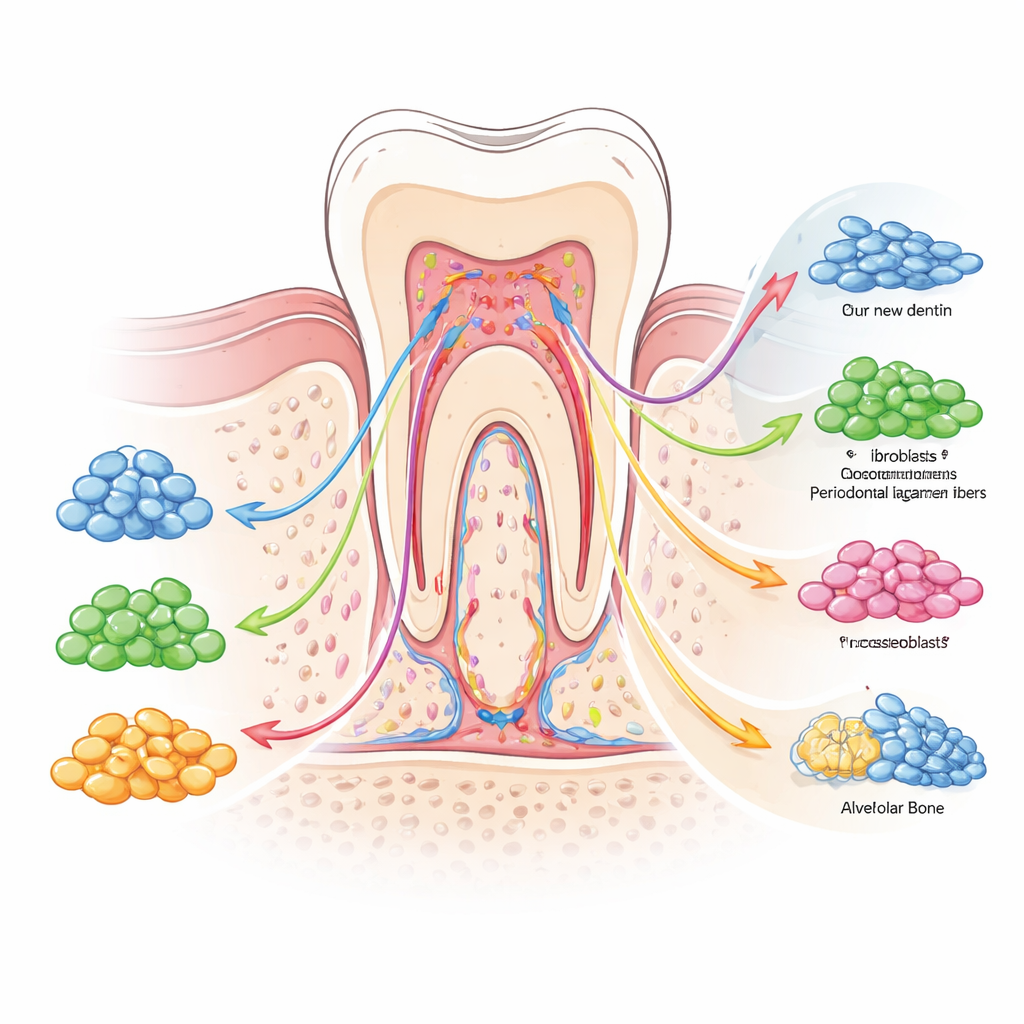
Signalen en schakelaars die stamcelgedrag vormen
De auteurs benadrukken dat deze diversiteit niet willekeurig is. Ze wordt georganiseerd door een netwerk van biochemische signalen en epigenetische schakelaars die als verkeerslichten en wegwijzers voor celdifferentiatie fungeren. Paden aangedreven door bone morphogenetic proteins, Wnt-signalen en transforming growth factor beta duwen cellen richting de bouw van harde weefsels zoals dentine en bot, terwijl andere routes, waaronder Notch en PI3K/AKT, helpen een gebalanceerde pool van stam- en progenitorcellen te behouden. Tegelijkertijd passen chemische labels op DNA en verpakkingsproteïnen aan welke genen toegankelijk zijn, waarmee bepaalde cellen vooringesteld worden voor een snelle respons bij schade. Mechanische krachten door kauwen, ontstekingsmoleculen door infectie en signalen van nabijgelegen bloedvaten of zenuwen kantelen de balans verder richting reparatie, littekenvorming of afbraak. Samen creëren deze controlelagen een flexibel, maar soms onvoorspelbaar, genezingssysteem.
Wat dit betekent voor toekomstige tandzorg
Voor niet-specialisten is de belangrijkste conclusie dat tand- en tandvleesregeneratie geen sciencefiction meer is, maar dat het succes ervan zal afhangen van het managen van stamceld diversiteit in plaats van die te negeren. De review stelt dat weten welke specifieke subpopulaties dentine, ligament, bot of zenuwen bouwen — en welke signalen hen sturen — onderzoekers zal helpen bij het verfijnen van celkeuze, biomaterialen en farmacologische aanwijzingen voor voorspelbare uitkomsten. Tegelijkertijd waarschuwen de auteurs dat de meeste gedetailleerde kaarten afkomstig zijn van dierstudies en kweekmodellen, en dat technische ruis het beeld kan vertroebelen. Ze pleiten voor geïntegreerde “multi-omics” benaderingen in menselijk weefsel, betere standaardisatie en rigoureuze testen in levende systemen. Uiteindelijk zou het ontcijferen van de heterogeniteit van mesenchymale tandheelkundige stamcellen tandartsen in staat kunnen stellen te verschuiven van het vervangen van beschadigde structuren met inerte materialen naar het daadwerkelijk regenereren van levende, functionele tanden en hun ondersteunende weefsels.
Bronvermelding: Fu, H., Chen, P., Wu, Z. et al. Research progress in heterogeneity of dental mesenchymal stem cells. Int J Oral Sci 18, 31 (2026). https://doi.org/10.1038/s41368-026-00433-8
Trefwoorden: tandheelkundige stamcellen, tandreconstructie, parodontale reparatie, single-cell sequencing, orale weefseltechniek