Clear Sky Science · es
Progresos en la investigación sobre la heterogeneidad de las células madre mesenquimales dentales
Por qué importan las diminutas células madre dentales
Los dientes parecen simples a primera vista, pero en su interior albergan un mundo activo de células madre que silenciosamente construyen, mantienen y reparan nuestras sonrisas. Este artículo de revisión explora una familia especial de células dentro y alrededor de los dientes—las células madre mesenquimales dentales—y explica cómo su diversidad oculta puede abrir la puerta a mejores tratamientos para la caries, la enfermedad de las encías, la pérdida ósea en la mandíbula e incluso las lesiones nerviosas. Al comprender el “reparto de personajes” detrás del desarrollo y la reparación dental, los investigadores esperan diseñar terapias regenerativas más inteligentes y fiables en lugar de depender solo del taladro, empastes e implantes.
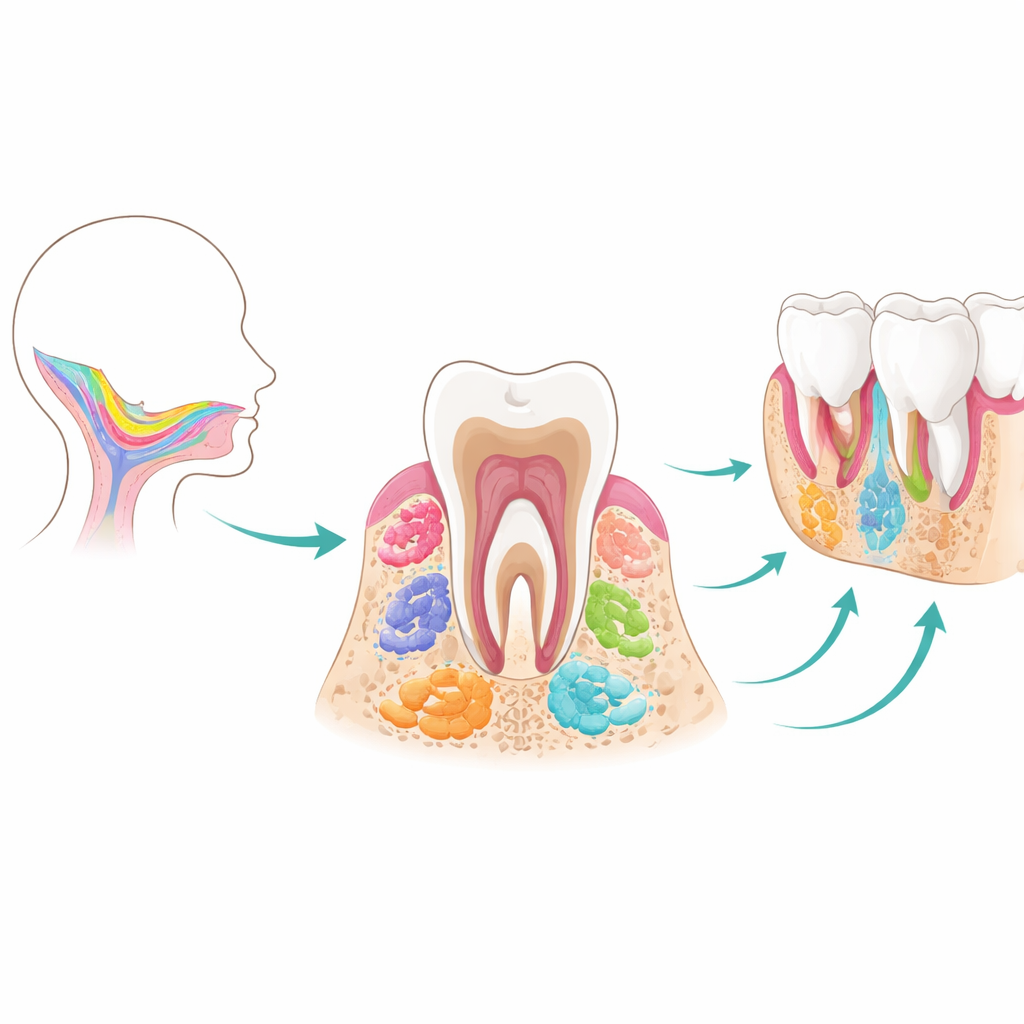
Desde los primeros brotes dentales hasta los dientes desarrollados
Los dientes y sus tejidos de sostén se forman mediante una asociación coreografiada entre dos capas principales: una cubierta externa que más tarde formará el esmalte, y células internas que darán lugar a la dentina, la pulpa, el ligamento y el hueso mandibular. Las células madre mesenquimales que constituyen el núcleo de esta revisión proceden en su mayoría de células migratorias del embrión temprano denominadas cresta neural craneal. Al asentarse en la mandíbula en formación, estas células primero producen los gérmenes dentales—pequeños “brotes” que atraviesan las fases de botón, casquete y campana. A lo largo de esta línea temporal aparecen por secuencia varias poblaciones temporales de células madre. Las células progenitoras del germen dental actúan como constructores tempranos y versátiles; las células madre del folículo dental ayudan a montar los tejidos que sostienen los dientes; y las células madre de la papila apical, en la punta de la raíz, guían la formación de la raíz y muestran un sorprendente potencial para convertirse en células de tipo nervioso. Una vez que las raíces dentales maduran, muchos de estos protagonistas iniciales desaparecen, lo que dificulta estudiarlos o reutilizarlos más adelante en la vida.
Muchos tipos de células madre, un sistema dental integrado
Incluso después de que los dientes están completamente formados, permanecen múltiples tipos de células madre alojadas en nichos protegidos y continúan apoyando el mantenimiento tisular. Las células madre de la pulpa dental viven dentro del diente, donde entran vasos sanguíneos y nervios; las células madre del ligamento periodontal se ubican entre la raíz dental y el hueso; las células madre gingivales recubren las encías; y las células madre mesenquimales en el hueso alveolar (mandíbula) forman el “suelo” que ancla los dientes. Cada población comparte rasgos básicos como la capacidad de autorrenovación y de diferenciarse en células formadoras de hueso o dentina, pero no son intercambiables. Por ejemplo, las células de la pulpa tienden a favorecer destinos hacia dentina y fenotipos similares a neuronas, las células periodontales sobresalen en reconstruir la unión fibrosa y el cemento en la superficie radicular, y las células del hueso mandibular están especializadas en la formación ósea rápida y directa en el rostro. Esta división del trabajo integrada ayuda a explicar por qué la boca puede responder de forma distinta a lesiones en la pulpa, el ligamento o el hueso.
Diferencias ocultas dentro de cada reserva de células madre
Un mensaje clave de la revisión es que la heterogeneidad existe no solo entre distintos tipos de células madre, sino también dentro de cada uno. Nuevas técnicas como la secuenciación de ARN unicelular pueden perfilar miles de células individuales a la vez, revelando subgrupos con actividad génica y comportamientos distintos. En la pulpa dental, por ejemplo, los investigadores han cartografiado múltiples clústeres: unos mantienen la reserva y promueven la proliferación, otros están preparados para la producción de dentina, y otros más están sesgados hacia formar vasos sanguíneos o células de tipo nervioso. Se han encontrado subgrupos similares en las células madre del ligamento periodontal, del hueso mandibular, de dientes de leche y de las encías. Moléculas marcadoras en la superficie celular y en el núcleo ayudan a distinguir estas subpoblaciones, que difieren en su capacidad de crecimiento, patrón de envejecimiento y respuesta a fuerzas mecánicas, inflamación o ataque bacteriano.
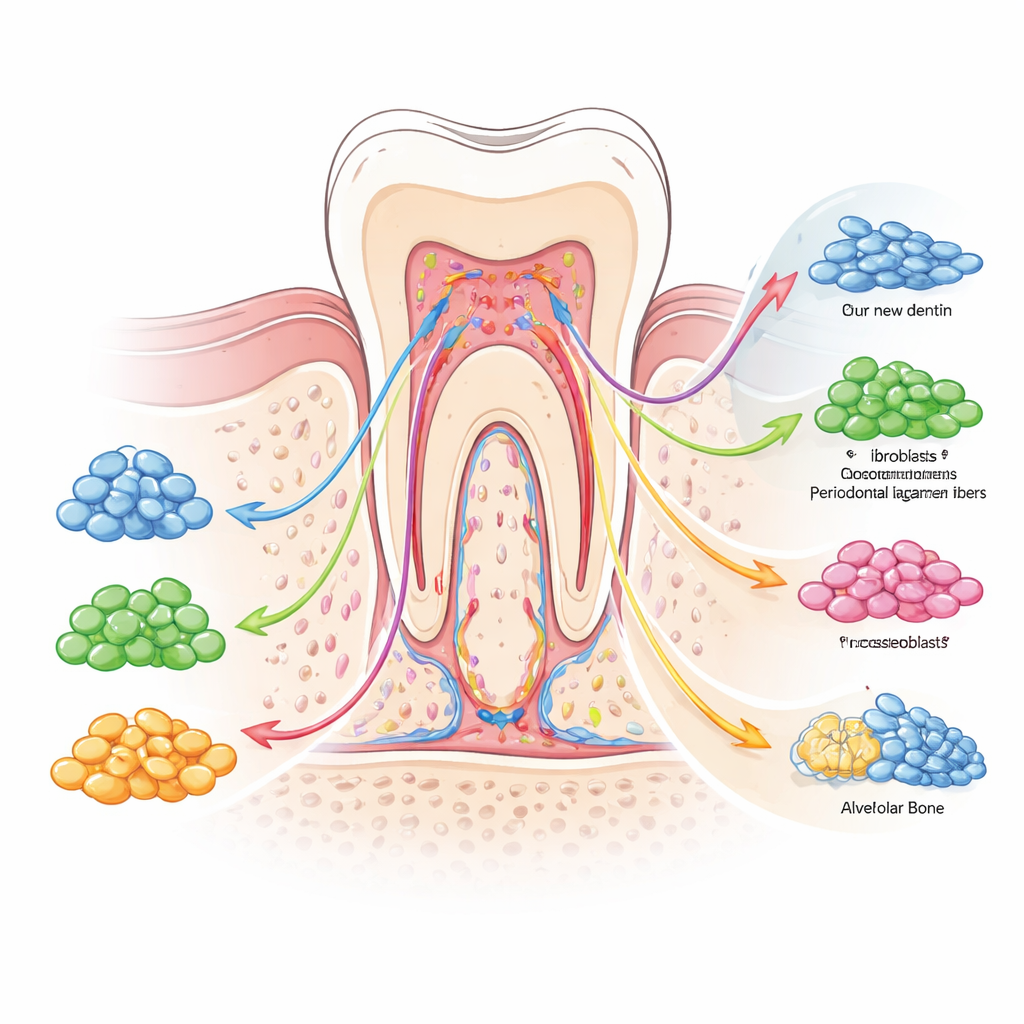
Señales e interruptores que moldean el comportamiento de las células madre
Los autores subrayan que esta diversidad no es aleatoria. Está organizada por una red de señales bioquímicas e interruptores “epigenéticos” que actúan como semáforos y señales de tráfico para el destino celular. Vías impulsadas por proteínas morfogenéticas óseas (BMP), señales Wnt y el factor de crecimiento transformante beta empujan a las células hacia la construcción de tejidos duros como la dentina y el hueso, mientras que otras, incluidas Notch y PI3K/AKT, ayudan a mantener un equilibrio entre células madre y progenitoras. Al mismo tiempo, etiquetas químicas sobre el ADN y las proteínas de empaquetamiento ajustan qué genes están accesibles, predisponiendo a ciertas células a responder rápidamente cuando ocurre una lesión. Las fuerzas mecánicas de la masticación, las moléculas inflamatorias de una infección y las señales procedentes de vasos sanguíneos o nervios cercanos inclinan además la balanza hacia la reparación, la cicatrización o la degradación. En conjunto, estas capas de control crean un sistema de curación flexible, pero a veces impredecible.
Qué significa esto para la atención dental futura
Para un público no especialista, la conclusión principal es que la regeneración de dientes y encías ya no es ciencia ficción, pero su éxito dependerá de gestionar la diversidad celular en lugar de ignorarla. La revisión sostiene que conocer qué subpoblaciones específicas construyen dentina, ligamento, hueso o nervios—y qué señales las dirigen—ayudará a los investigadores a afinar la selección celular, los biomateriales y las señales farmacológicas para obtener resultados predecibles. Al mismo tiempo, los autores advierten que la mayoría de los mapas detallados provienen de estudios en animales y cultivos de laboratorio, y que el ruido técnico puede difuminar la imagen. Abogan por enfoques integrados de “multi-ómica” en tejido humano, mejor estandarización y ensayos rigurosos en sistemas vivos. En última instancia, descifrar la heterogeneidad de las células madre mesenquimales dentales podría permitir a los dentistas pasar de reemplazar estructuras dañadas con materiales inertes a regenerar realmente dientes vivos y funcionales y sus tejidos de sostén.
Cita: Fu, H., Chen, P., Wu, Z. et al. Research progress in heterogeneity of dental mesenchymal stem cells. Int J Oral Sci 18, 31 (2026). https://doi.org/10.1038/s41368-026-00433-8
Palabras clave: células madre dentales, regeneración dental, reparación periodontal, secuenciación unicelular, ingeniería de tejidos orales